
- •Введение
- •Электронное строение элементов-органогенов. Химическая связь в органических молекулах
- •Химическая связь в органических молекулах
- •Классификация химических реакций. Химические свойства алканов, алкенов и алкадиенов
- •Реакционная способность алканов
- •Реакционная способность алкенов
- •Химические свойства алкенов
- •Общий механизм реакций электрофильного присоединения
- •Реакции электрофильного присоединения к несимметричным алкенам
- •Реакции присоединения к алкадиенам
- •Сопряжённые системы. Ароматичность. Электронные эффекты. Реакции электрофильного замещения в бензоле и его производных
- •Химические свойства бензола
- •Взаимное влияние атомов в молекулах органических соединений. Электронные эффекты
- •Реакции электрофильного замещения в нафталине
- •Реакции окисления гомологов бензола
- •Химические свойства галогеналканов, спиртов и фенолов
- •Медико-биологическое значение галогеналканов
- •Спирты и фенолы
- •Медико-биологическое значение спиртов и фенолов
- •Кислотные и основные свойства органических соединений. Реакционная способность аминов
- •Кислоты Бренстеда
- •Основания Бренстеда
- •Реакционная способность оксосоединений
- •Классификация и номенклатура оксосоединений
- •Названия алифатических альдегидов
- •Реакционные центры в молекулах оксосоединений
- •Примеры реакций нуклеофильного присоединения
- •Медико-биологическое значение альдегидов и кетонов
- •Химические свойства карбоновых кислот и их функциональных производных
- •Названия предельных алифатических монокарбоновых кислот
- •Реакционные центры в молекулах карбоновых кислот
- •Кислотные свойства карбоновых кислот
- •Реакции нуклеофильного замещения
- •Реакции карбоновых кислот по радикалу
- •Названия насыщенных алифатических дикарбоновых кислот
- •Медико-биологическое значение карбоновых кислот и их производных
- •Гетерофункциональные соединения алифатического ряда – метаболиты и биорегуляторы
- •Аминоспирты
- •Аминокислоты
- •Гидроксикислоты (оксикислоты)
- •Оксокислоты
- •Медико-биологическое значение гетерофункциональных производных карбоновых кислот
- •Оптическая изомерия
- •Стереоизомерия молекул с несколькими центрами хиральности
- •Стереоизомерия и биологическая активность
- •Гетерофункциональные производные бензольного ряда
- •Производные сульфаниловой кислоты
- •Сульфаниламидные препараты
- •Салициловая кислота и ее производные
- •Гетероциклические соединения. Производные пятичленных гетероциклов
- •Пятичленные гетероциклы с одним гетероатомом
- •Свойства пиррола и его производных
- •Свойства фурана и его производных
- •Пятичленные гетероциклы с двумя гетероатомами
- •Шестичленные гетероциклические соединения
- •Шестичленные гетероциклы с двумя гетероатомами
- •Углеводы. Моносахариды
- •Цикло-оксо-таутомерия моносахаридов
- •Углеводы. Ди- и полисахариды
- •Природные α-аминокислоты. Пептиды, белки
- •Строение и классификация природных α-аминокислот
- •Стереоизомерия α-аминокислот
- •Химические свойства
- •Реакции α-аминокислот in vivo
- •Нуклеиновые кислоты
- •Нуклеиновые основания
- •Нуклеозиды
- •Названия нуклеозидов
- •Нуклеотиды
- •Нуклеиновые кислоты
- •Омыляемые липиды
- •Фосфолипиды
- •Неомыляемые липиды
- •Алкалоиды
- •Литература
- •Оглавление
- •305041, Г. Курск, ул. К. Маркса, 3.
- •305041, Г. Курск, ул. К. Маркса, 3. Заказ № 313.
Омыляемые липиды
К липидам относятся разнородные в химическом отношении природные соединения. Их объединяют в один класс по признаку растворимости: липиды нерастворимы в воде и растворимы в неполярных органических растворителях (бензол, диэтиловый эфир).
В зависимости от способности к гидролизу липиды делят на омыляемые (подвергаются гидролизу) и неомыляемые (не подвергаются гидролизу).
К омыляемым липидам относятся жиры, фосфолипиды и воски.
Основу омыляемых липидов составляют высшие карбоновые кислоты и спирты (глицерин в случае жиров и фосфолипидов и высшие спирты – в случае восков).
Жиры
В организме жиры играют роль структурного компонента клетки и роль запасного питательного вещества.
Ж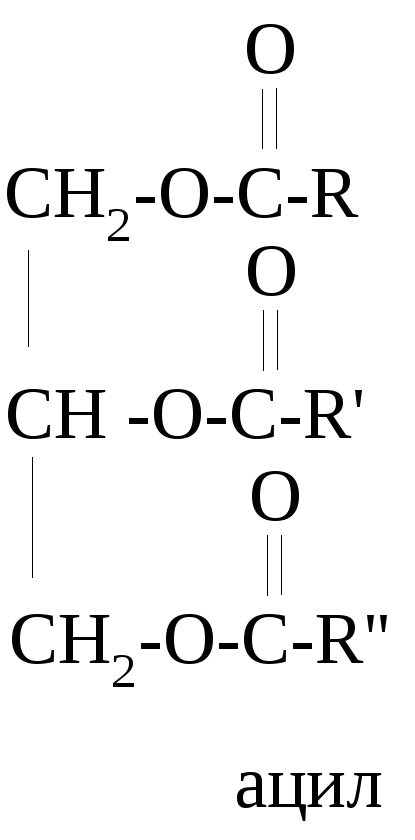 иры
являются сложными эфирами глицерина и
высших карбоновых кислот, т.е.
триацилглицеринами.
иры
являются сложными эфирами глицерина и
высших карбоновых кислот, т.е.
триацилглицеринами.
Природные жиры являются смесью различных триацилглицеринов.
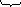
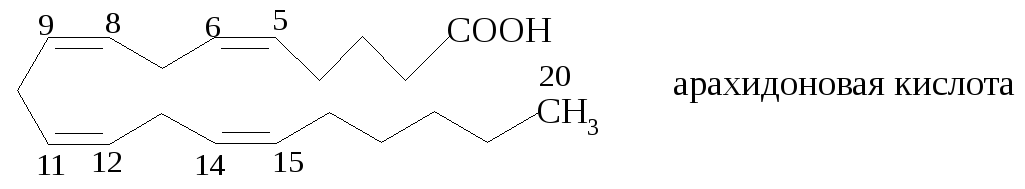
В структуре жиров присутствуют остатки насыщенных высших карбоновых кислот (стеариновой и пальмитиновой) и ненасыщенных кислот (олеиновой, линолевой, линоленовой, арахидоновой).
У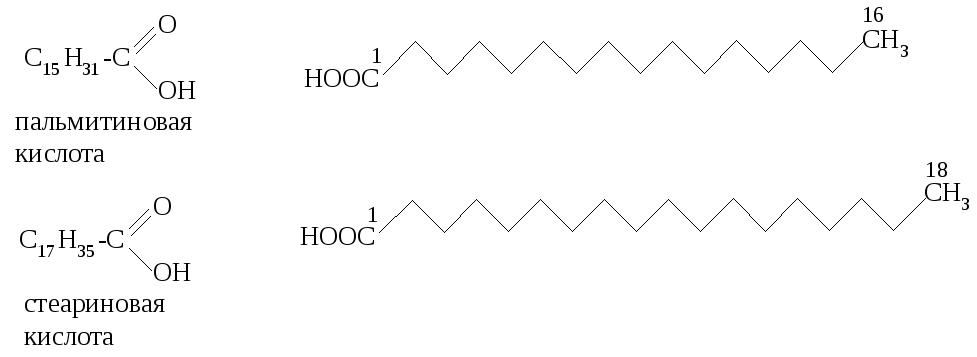 глеводородные
радикалы высших карбоновых кислот
нелинейны. Они существуют в зигзагообразной
конформации:
глеводородные
радикалы высших карбоновых кислот
нелинейны. Они существуют в зигзагообразной
конформации:
Высшие ненасыщенные кислоты способствуют снижению содержания в крови холестерина – фактора развития атеросклероза. Смесь сложных эфиров ненасыщенных жирных кислот под названием «Линетол» применяется в медицине.
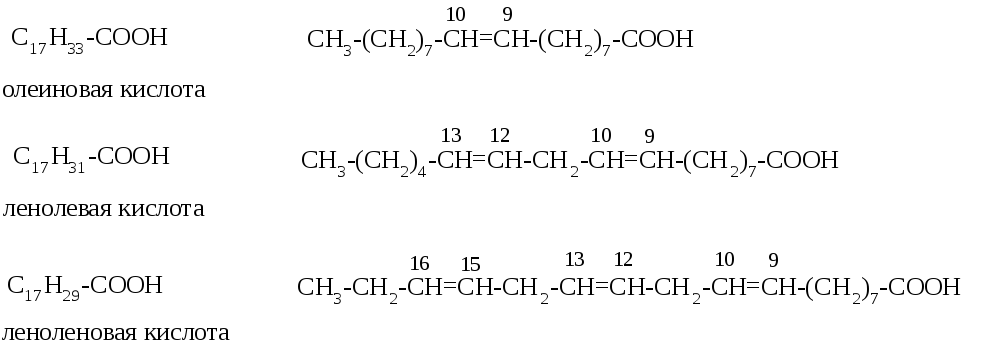
Д ля
ненасыщенных карбоновых кислот характерна
цис-транс-изомерия. В структуру жиров
и фосфолипидов они входят в цис-конфигурации.
ля
ненасыщенных карбоновых кислот характерна
цис-транс-изомерия. В структуру жиров
и фосфолипидов они входят в цис-конфигурации.
Если в структуре жира преобладают остатки насыщенных карбоновых кислот, то жир твердый, если преобладают остатки ненасыщенных кислот, то жир жидкий (масло). Как правило, животные жиры твердые, растительные – жидкие.
Жиры, включающие остатки одинаковых кислот, называют простыми, остатки разных жирных кислот – смешанными.
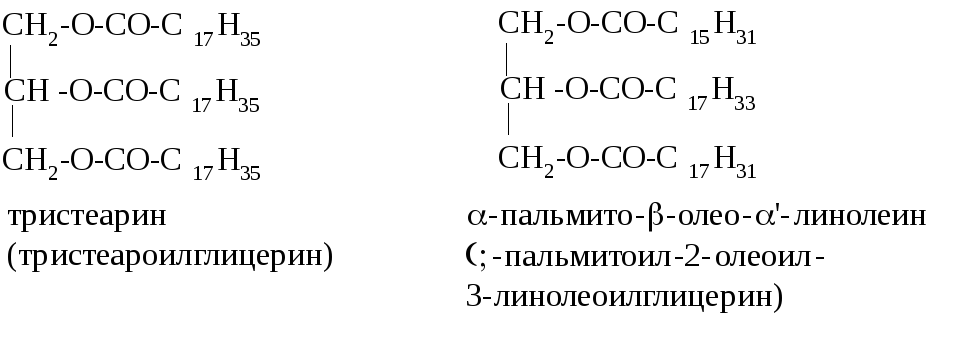
Жиры называют по тривиальной номенклатуре, заменяя суффикс «-овая» в названии кислоты на «-ин» (тристеарин, трипальмитин), и по систематической номенклатуре как сложные эфиры глицерина, используя суффикс «-оил» (тристеароилглицерин, трипальмитоилглицерин). Например:
Так как жиры являются сложными эфирами, то для них характерны реакции гидролиза как в кислой, так и в щелочной среде.
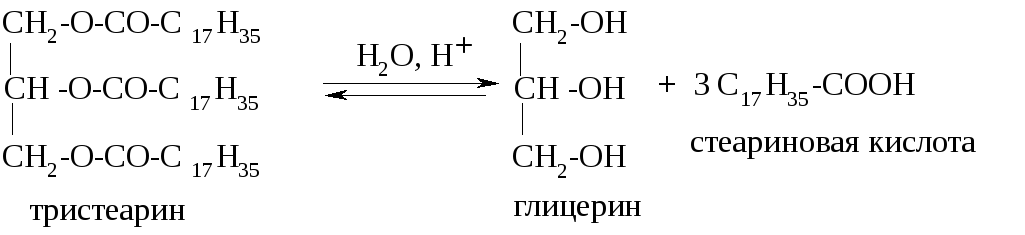
Кислотный гидролиз обратим, в результате образуются глицерин и соответствующие карбоновые кислоты:
П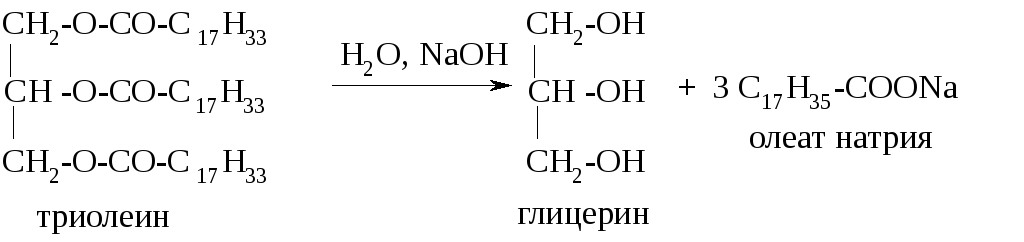 ри
щелочном гидролизе жиров образуются
глицерин и соли высших карбоновых
кислот:
ри
щелочном гидролизе жиров образуются
глицерин и соли высших карбоновых
кислот:
Соли высших карбоновых кислот нзываются мылами. Вот почему жиры относят к омыляемым липидам. Натриевые и каливые мыла растворимы в воде, кальциевые, магниевые – нет. Моющее действие мыл основано на дифильности их структуры. Молекулы мыл включают полярную часть – карбоксилатную группу с гидрофильными свойствами и неполярный углеводородный радикал – с гидрофобными (липофильными).
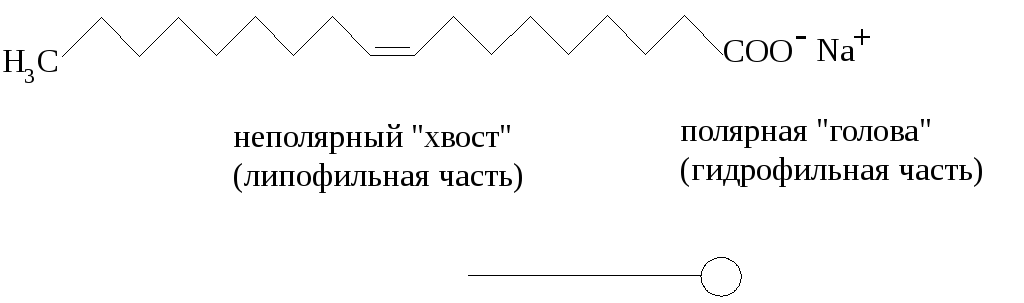
Р ассмотрим
механизм моющего действия мыл. Загрязнения
имеют жироподобную природу. По принципу
«подобное растворяется в подобном»
липофильная часть молекулы мыла
растворяется в капельке жира, а
гидрофильная остается на поверхности.
Образуется так называемая мицелла. В
целом она гидрофильна (на ее поверхности
гидрофильная пленка) и может быть вымыта
водой. Кроме того, на поверхности мицеллы
сосредоточен отрицательный заряд,
значит, отдельные капельки жира
отталкиваются друг от друга и не
сливаются. Таким образом, мыло способствует
образованию эмульсии жира в воде,
обладает эмульгирующим
действием.
Таким действием обладают и молекулы
других соединений, имеющие дифильную
структуру (фосфолипиды, желчные кислоты).
ассмотрим
механизм моющего действия мыл. Загрязнения
имеют жироподобную природу. По принципу
«подобное растворяется в подобном»
липофильная часть молекулы мыла
растворяется в капельке жира, а
гидрофильная остается на поверхности.
Образуется так называемая мицелла. В
целом она гидрофильна (на ее поверхности
гидрофильная пленка) и может быть вымыта
водой. Кроме того, на поверхности мицеллы
сосредоточен отрицательный заряд,
значит, отдельные капельки жира
отталкиваются друг от друга и не
сливаются. Таким образом, мыло способствует
образованию эмульсии жира в воде,
обладает эмульгирующим
действием.
Таким действием обладают и молекулы
других соединений, имеющие дифильную
структуру (фосфолипиды, желчные кислоты).
Мыла как моющие средства имеют ряд недостатков. Они не эффективны в жесткой воде, т.к. кальциевые и магниевые соли высших жирных кислот не растворимы в воде. Растворы натриевых и калиевых мыл имеют щелочную реакцию (они образованы сильными основаниями и слабыми кислотами), поэтому сушат и раздражают кожу.
В настоящее время используются также синтетические моющие средства – детергенты. В их структурах также имеются гидрофильная и липофильная части, т.е. они являются поверхностно-активными соединениями.
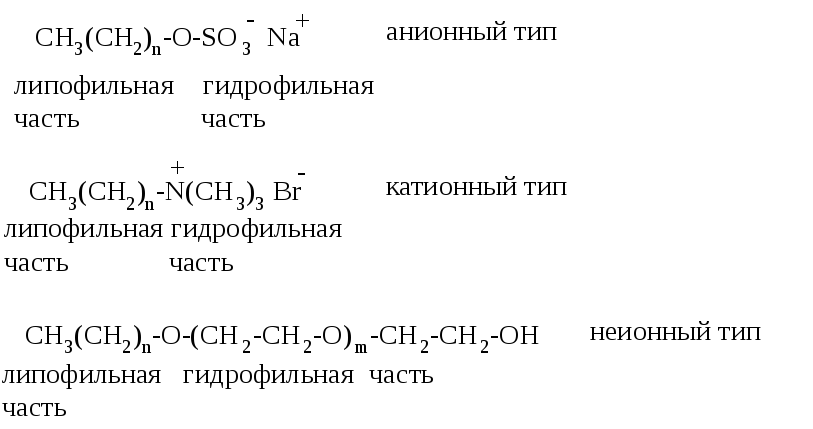
Синтетические моющие средства имеют нейтральную реакцию, эффективны в жесткой воде, но плохо подвергаются биологическому распаду и загрязняют окружающую среду.
Для жиров, содержащих остатки непредельных карбоновых кислот, характерны реакции гидрирования:
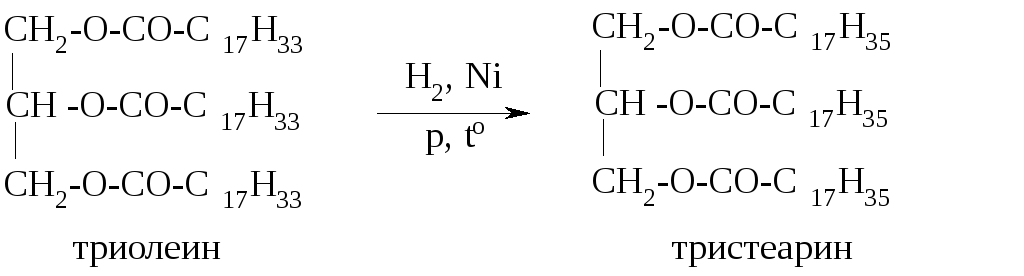
В результате этой реакции можно получить из более дешевых жидких растительных масел твердые жиры. Это свойство используют в производстве маргарина.
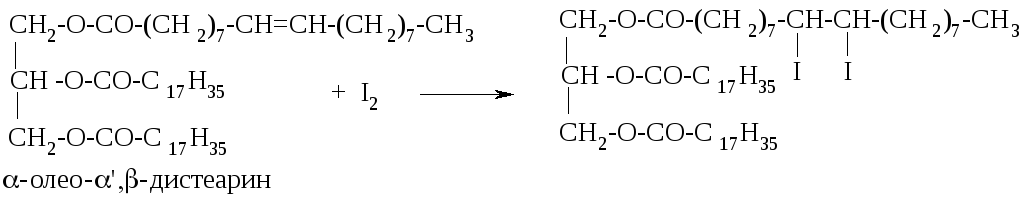
Наличие остатков непредельных карбоновых кислот в структуре жиров можно подтвердить реакцией с бромной водой:
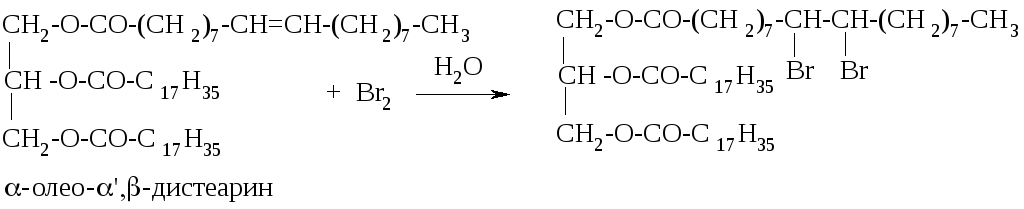
Бромная вода обесцвечивается.
Ненасыщенные жиры способны к реакциям окисления в различных условиях. Окисление раствором перманганата калия в мягких условиях приводит к образованию диольного фрагмента по месту разрыва двойной связи, качественным признаком этой реакции является исчезновение розовой окраски перманганата калия и выпадение бурого осадка диоксида марганца:
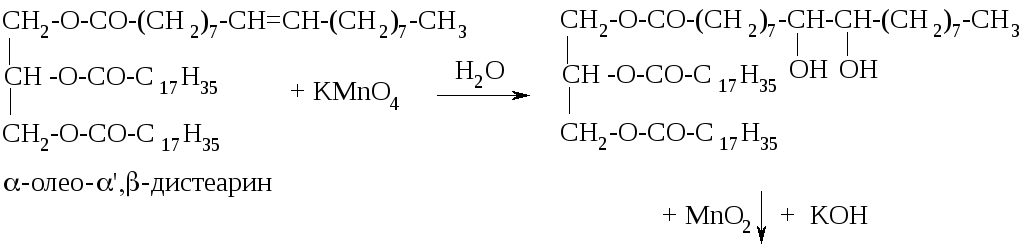
При окислении в жестких условиях происходит расщепление молекулы по месту двойной связи:

Сходным образом (но медленно) протекает реакция окисления жиров и под действием кислорода воздуха (так называемое автоокисление). В результате автоокисления образуются низшие карбоновые кислоты, имеющие неприятный запах и вкус, – жир «прогоркает».
Некоторые лекарственные препараты используются в медицине в виде масляных растворов (камфора, эстрадиола дипропионат, прогестерон и т.д.), поэтому важно уметь контролировать качество этих масел. С этой целью используют специальную характеристику – иодное число жира. Иодное число – это количество граммов иода, способное присоединиться к 100 граммам жира.
Чем более ненасыщенный жир, тем выше его иодное число. В результате автоокисления иодное число жира снижается по сравнению со стандартом, т.к. уменьшается количество двойных связей в молекуле.
Е ще
один вид окисления жиров (а также
фосфолипидов) – пероксидное окисление,
протекающее с участием свободных
радикалов, которые постоянно образуются
в организме:
ще
один вид окисления жиров (а также
фосфолипидов) – пероксидное окисление,
протекающее с участием свободных
радикалов, которые постоянно образуются
в организме:
Реакция пероксидного окисления начинается по α-положению по отношению к двойной связи, т.к. радикалы аллильного типа устойчивы (см. стр. 32), далее образуются пероксид и гидропероксид, который расщепляется с образованием соответствующих альдегидов, которые в свою очередь окисляются в карбоновые кислоты. В результате пероксидного окисления нарушается структура жиров и фосфолипидов, которые являются составляющими клеточных мембран, т.е. нарушаются функции мембран. С этим явлением связывают и процессы старения, и вредное воздействие радиации на организм (один из механизмов возникновения лучевой болезни). Кроме того предполагают, что промежуточные продукты пероксидного окисления липидов обладают мутагенным действием.
Воски
Воски – сложные эфиры высших жирных кислот и одно- или двухатомных высших спиртов. В восках содержатся также свободные карбоновые кислоты, высшие спирты, углеводороды. Воски делятся на животные (спермацет, пчелиный воск, ланолин) и растительные (карнаубский воск). Они образуют защитную смазку на коже человека и животных и предотвращают растения от высыхания. Воски используют при приготовлении косметических средств, мазей, водоотталкивающих пропиток для тканей.
Главным компонентом спермацета (содержится в спермацетовом масле, получаемом из головы кашалота) является цетиловый эфир пальмитиновой кислоты:
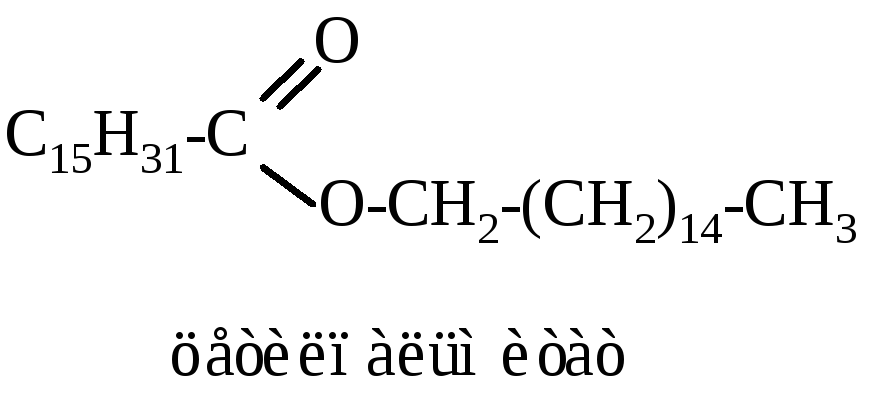
Д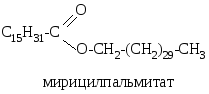 ругой
эфир пальмитиновой кислоты –
мирицилпаль-
митат – содержится в
пчелином воске:
ругой
эфир пальмитиновой кислоты –
мирицилпаль-
митат – содержится в
пчелином воске:
Как сложные эфиры, воски способны к гидролизу. Их относят к омыляемым липидам.
