
- •5. Биологические функции и классификация белков.
- •6. Значение и специфичность действия ферментов.
- •7. Строение фермента.
- •8. Активный центр.
- •9. Определение активности ферментов.
- •10. Локализация ферментов в клетке, маркёрные и органоспецифические ферменты.
- •11. Механизм действия ферментов.
- •12 . Кинетика ферментативных реакций.
- •13. Регуляция активности ферментов.
- •14. Ингибирование ферментов.
- •15 . Номенклатура и классификация. Изоферменты. Изменение активности в энтогенезе.
- •15 . Энзимопатия.
- •16. Обмен веществ. Ката- и анаболизм .
- •17.Биологическое окисление.
- •18. Природа макроэргичности атф.
- •19. Цикл кребса.
- •20 . Тканевое дыхание.
- •21 . Дыхательная цепь.
- •22. Механизм сопряжения окислительного фосфорилирования.
- •23 . Термогенез.
- •24 . Микросомальная дыхательная цепь.
- •25 . Перекисное окисление и антиоксидантная защита.
- •26 . Углеводы и их переваривание.
- •1) Гиалуроновая кислота.
- •2) Кондратин – сульфат
- •3) Гепарин
- •27 . Биологические функции углеводов.
- •28 . Переваривание углеводов .
- •Галактоза
- •Фруктоза
- •29 . Пути метаболизма глюкозы.
- •30 . Синтез и распад гликогена.
- •31.Гликогенозы.
- •32 . Гликогенолиз и гликолиз.
- •33. Механизм гликолитической оксидоредукции. Субстратное фосфорилирование.
- •34 . Спиртовое брожение и метаболизм этанола.
- •34.Эробный распад глюкозы. Окислительное декарбоксилиро -
- •35. Глюконеогенез.
- •36. Гипо - и гипергликемия.
- •37.Регуляция уровня глюкозы в крови.
- •38. Сахарный диабет.
- •39. Липиды . Строение , классификация , биологическая роль .
- •40.Переваривание и всасывание липидов .
- •41. Ресинтез липидов в стенке кишечника .
- •42 . Метаболизм липидов .
- •45. Пути обмена ацетил-КоА . Обмен кетоновых тел .
- •46. Биосинтез триглицеридов.
- •47. Интеграция углеводного и липидного обмена .
- •48. Белковый обмен.
- •49. Состав желудочного сока. Механизм секреции hCl .
- •9. Ряд аминокислот, имеющих диагностическое значение .
- •50. Панкреатический сок.
- •51. Кишечный сок.
- •1.Энтерокиназа .
- •9. Фосфолипаза и липаза .
- •52 . Переваривание белков .
- •53. Гниение белков в толстом кишечнике .
- •54. Механизм всасывания аминокислот и пути их утилизации .
- •55.Трансаминирование аминокислот .
- •56. Токсичность аммиака и пути его обезвреживания .
- •57. Биосинтез мочевины .
- •58. Цикл кребса-гензеляйта .
- •59. Пути вступления аминокислот в цтк .
- •60. Декарбоксилирование аминокислот .
- •61.Метаболизм серина и глицина .
- •62. Нарушение обмена глицина .
- •63. Обмен серосодержащих аминокислот и триптофана.
- •64. Метаболизм триптофана.
- •65. Обмен фенилаланина и тирозина.
- •66. Обмен гистидина, глутамина, аспарагина, пролина.
- •67. Интеграция углеводного, белкового и липидного обмена.
- •72. Распад пуриновых нуклеотидов. Подагра.
- •73. Синтез и распад пиримидиновых оснований.
12 . Кинетика ферментативных реакций.
Любая химическая реакция характеризуется константой термодинамического равновесия (Кр).
R +1 {C}{D}
А + В ==== C + D; Кр =------------ Кр = R+1/ R – 1
R – 1 {A}{B}
Величину, обратную константе равновесия (Кр), принято называть константой диссоциации фермент – субстратного комплекса (Кs).
R+1 {E} {S}
E + S ==== ES ; Ks = ------------ = R-1 / R+1
R-1 {ES}
Чем ниже Ks, тем выше сродство фермента к субстрату. При низкой концентрации субстрата зависимость скорости реакции от {S} является почти линейной и подчиняется кинетике 1-го порядка. Это означает, что скорость реакции S -------- P прямо пропорциональна {S} и определяется следующим уравнением:
V= R` {S}, где R` - константа скорости.
При высокой концентрации субстрата скорость реакции максимальна и становится постоянной, независящей от {S}.
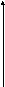 V = R``(реакция
нулевого прядка)
V = R``(реакция
нулевого прядка)
---------------
-
реакция первого порядка
-
реакция смешанного порядка
-
реакция нулевого порядка

Теория ферментативной кинетики.
R+1 R+2
E+S =====ES ------- E+P
R-1
Уравнение Михаэлиса-Ментена:
Vmax {S}
V= --------------
Ks + {S}
Отсюда видно, что при высокой {S} и низкой Ks V=Vmax (нулевой порядок); при низкой {S} – V=R`{S} (первый порядок). Однако уравнение Михаэлиса - Ментена не учитывает влияние на скорость ферментативного процеса продуктов реакции, поэтому его несколько усовершенствовали:
Vmax {S}
V= ---------------
Km +{S}
Km – константа Михаэлиса – это такая концентрация субстрата (моль/л), при которой скорость данной ферментативной реакции составляет половину от максимальной. Её определение необходимо для количественной оценки степени сродства фермента к субстрату. Чем ниже Km, тем выше степень сродства фермента к субстрату. Km – генетически детерминированная константа, является средством регуляции интенсивности метаболических процессов. В разных тканях ферменты имеют разные значения Km.
 Km мозга < Km
мышечной ткани < Km
жировой ткани .
Km мозга < Km
мышечной ткани < Km
жировой ткани .
Для 1-го фермента V реакции = 50%
Для 2-го фермента V реакции =20%
Для 3-го фермента V реакции = 10%
Л айнцивер
и Бэри преобразовали предыдущее
уравнение по методу двойных обратных
величин. Исходя из того принципа,
что если существует равенство между
двумя какими-либо величинами, то и
обратные величины также будут равны:
айнцивер
и Бэри преобразовали предыдущее
уравнение по методу двойных обратных
величин. Исходя из того принципа,
что если существует равенство между
двумя какими-либо величинами, то и
обратные величины также будут равны:
Vmax {S} Km + {S} Km
если V=---------------- , то 1/ V=-------------- или 1/V = ------------- + 1/Vmax
Km + {S} Vmax {S} Vmax {S}
Факторы, влияющие на скорость ферментативной реакции.
1) Концентрация фермента (чем выше концентрация фермента, тем выше скорость реакции)
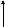


-
Концентрация субстрата

Для простых ферментов зависимость имеет вид гиперболы.


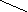

3) Температура
Согласно правилу Вант-Гоффа, при повышении температуры на каждые 10 С скорость реакции возрастает в 2-3 раза. То есть, с одной стороны, по мере увеличения температуры увеличивается средняя энергия молекул, при этом они активизируются, выше частота их соударений, выше подвижность отдельных элементов активного центра фермента и скорость реакции увеличивается, но до известного предела. При дальнейшем повышении температуры (выше 45С) скорость реакции понижается. Это объясняется белковой природой фермента, который может пдвергаться тепловой денатурации, что резко понижает эффективную концентрацию фермента и соответственно скорость реакции.
При низких температурах (0 и ниже) ферменты не денатурируются, хотя активность их падает почти до нуля. Исходя из этого, существует температурный оптимум, в пределах которого ферменты нормально работают.
4) Величина рН
При действии рН происходит 3 явления:
1)изменение ионизации и заряда на поверхности аллофермента;
2) изменение степени ионизации функциональных групп активного центра;
3) изменение ионизации самого субстрата.
Так, при сдвиге рН в кислую сторону происходит следующее:
СООН== СОО + Н СОО + Н ---- СООН
NH3 === NH2 +H рН <7 NH3 + H ---- NH4 нет взаимодействия
При сдвиге рН в основную сторону:
СООН+ ОН ==== СОО + НО
NH3 + OH === NH2 + Н2О рН>7
То есть и в этом и в другом случае происходит перезарядка функциональных групп активного центра. Поэтому здесь тоже существует свой оптимум рН. Для разных ферментов он разный: пепсин - рН = 1,5-2,5; сахароза – рН = 4; трипсин – рН = 7,7-7,8; ариназа- рН = 8,5-10,0.
5) Концентрация продукта
Оказывает влияние на скорость реакции по принципу обратной связи, то есть тормозит. При наполнении продукта вся система блокируется на последней стадии (ретроингибирование). Так, например, накопление молочной кислоты, образующейся при распаде глюкозы, приводит к снижению последней и формированию утомления.
