
- •5. Биологические функции и классификация белков.
- •6. Значение и специфичность действия ферментов.
- •7. Строение фермента.
- •8. Активный центр.
- •9. Определение активности ферментов.
- •10. Локализация ферментов в клетке, маркёрные и органоспецифические ферменты.
- •11. Механизм действия ферментов.
- •12 . Кинетика ферментативных реакций.
- •13. Регуляция активности ферментов.
- •14. Ингибирование ферментов.
- •15 . Номенклатура и классификация. Изоферменты. Изменение активности в энтогенезе.
- •15 . Энзимопатия.
- •16. Обмен веществ. Ката- и анаболизм .
- •17.Биологическое окисление.
- •18. Природа макроэргичности атф.
- •19. Цикл кребса.
- •20 . Тканевое дыхание.
- •21 . Дыхательная цепь.
- •22. Механизм сопряжения окислительного фосфорилирования.
- •23 . Термогенез.
- •24 . Микросомальная дыхательная цепь.
- •25 . Перекисное окисление и антиоксидантная защита.
- •26 . Углеводы и их переваривание.
- •1) Гиалуроновая кислота.
- •2) Кондратин – сульфат
- •3) Гепарин
- •27 . Биологические функции углеводов.
- •28 . Переваривание углеводов .
- •Галактоза
- •Фруктоза
- •29 . Пути метаболизма глюкозы.
- •30 . Синтез и распад гликогена.
- •31.Гликогенозы.
- •32 . Гликогенолиз и гликолиз.
- •33. Механизм гликолитической оксидоредукции. Субстратное фосфорилирование.
- •34 . Спиртовое брожение и метаболизм этанола.
- •34.Эробный распад глюкозы. Окислительное декарбоксилиро -
- •35. Глюконеогенез.
- •36. Гипо - и гипергликемия.
- •37.Регуляция уровня глюкозы в крови.
- •38. Сахарный диабет.
- •39. Липиды . Строение , классификация , биологическая роль .
- •40.Переваривание и всасывание липидов .
- •41. Ресинтез липидов в стенке кишечника .
- •42 . Метаболизм липидов .
- •45. Пути обмена ацетил-КоА . Обмен кетоновых тел .
- •46. Биосинтез триглицеридов.
- •47. Интеграция углеводного и липидного обмена .
- •48. Белковый обмен.
- •49. Состав желудочного сока. Механизм секреции hCl .
- •9. Ряд аминокислот, имеющих диагностическое значение .
- •50. Панкреатический сок.
- •51. Кишечный сок.
- •1.Энтерокиназа .
- •9. Фосфолипаза и липаза .
- •52 . Переваривание белков .
- •53. Гниение белков в толстом кишечнике .
- •54. Механизм всасывания аминокислот и пути их утилизации .
- •55.Трансаминирование аминокислот .
- •56. Токсичность аммиака и пути его обезвреживания .
- •57. Биосинтез мочевины .
- •58. Цикл кребса-гензеляйта .
- •59. Пути вступления аминокислот в цтк .
- •60. Декарбоксилирование аминокислот .
- •61.Метаболизм серина и глицина .
- •62. Нарушение обмена глицина .
- •63. Обмен серосодержащих аминокислот и триптофана.
- •64. Метаболизм триптофана.
- •65. Обмен фенилаланина и тирозина.
- •66. Обмен гистидина, глутамина, аспарагина, пролина.
- •67. Интеграция углеводного, белкового и липидного обмена.
- •72. Распад пуриновых нуклеотидов. Подагра.
- •73. Синтез и распад пиримидиновых оснований.
73. Синтез и распад пиримидиновых оснований.

 АТФ
АДФ NH2
АСП
COOH
АТФ
АДФ NH2
АСП
COOH
C

 O2
+ (ГЛИ) NH3
|
/
O2
+ (ГЛИ) NH3
|
/
карбомаилфосфат C =O Фн NH2 CH2
синтетаза-2 | | |
O – Ф O = C CH – COOH
карбомаилфосфат \ /
O O NH
|| || карбомаиласпартат

 C
НАД
НАД*Н2 C
ФРПФ
ФФн
C
НАД
НАД*Н2 C
ФРПФ
ФФн
дигидрооротаза / \ / \


 HN CH2O
HN
CH оротатфосфорилозин
HN CH2O
HN
CH оротатфосфорилозин
| | дегидрооротаза-2 | || трансфераза
 O = C
CH – COOH
C
C – COOH
O = C
CH – COOH
C
C – COOH
\ / \ /
NH NH
Дигидрооротовая кислота оротовая кислота
O
|| O
 C
||
C
||
/ \




 NH CH
NH
NH CH
NH
 | ||
//
| ||
//
O = C C – COOH O N
\ / |
N риб – Ф
| уридин-5-фосфат
риб – Ф
оротидин-5-фосфат
В клетках печени донатором NH2-группы для синтеза карбомаилфосфата является как ГлН, так и свободный аммиак, в то время как во всех остальных клетках донатором NH2-группы является только ГлН.

 УМФ + АТФ УДФ
+ АДФ
УМФ + АТФ УДФ
+ АДФ
 УДФ + АТФ УТФ
+ АДФ
УДФ + АТФ УТФ
+ АДФ

Первые три реакции катализируются одним белком с тремя активными центрами. Поэтому образующийся карбомаилфосфат не идёт на синтез мочевины. При недостаточности последних двух ферментов синтеза, происходит накопление оротовой кислоты, возникает состояние пиримидинового голода, нарушается синтез нуклеиновых кислот.
74. ДНК, ПЕРВИЧНАЯ И ВТОРИЧНАЯ СТРУКТУРА, ВИДЫ ДНК,ПРАВИЛО ЧАРГАФФА.
Нуклеиновые кислоты – высокомолекулярные соединения, построенные из мономерных единиц – мононуклеотидов. При их полном гидролизе образуются:
Д НК
Н3РО4,
дезоксирибоза, аденин, гуанин, цитозин
и тимин.
НК
Н3РО4,
дезоксирибоза, аденин, гуанин, цитозин
и тимин.
Р НК
Н3РО4,
рибоза, аденин, гуанин, цитозин, урацил.
НК
Н3РО4,
рибоза, аденин, гуанин, цитозин, урацил.
Мононуклеотиды – структурные единицы нуклеиновых кислот. То есть, нуклеиновые кислоты представляют собой полинуклеотиды, последовательность расположения мононуклеотидов в которых определяется в строгом соответствии с программой, заложенной в молекуле-матрице.
Мононуклеотид состоит из трёх компонентов:
-
азотистого основания
-
углевода (рибоза или дезоксирибоза)
-
остаток Н3РО4
Соединение азотистого основания и углевода называется нуклеозидом. Нуклеозид содержит азотистое основание, связанное с углеводом N-гликозидной связью. Имеются два типа нуклеозидов: а и в. В состав нуклеиновых кислот входят только в.
Углеводы нуклеиновых кислот:
СН2ОН СН2ОН









 О
ОН О ОН
О
ОН О ОН





ОН ОН ОН ОН
в-D-рибоза в-D-дезоксирибоза
Азотистые основания:
а) пиримидиновые
O O NH2



 || || |
|| || |


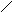


 CH3
CH3






 NH
NH N
NH
NH N
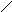

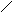
 O =
O = O =
O =
O = O =
NH NH NH
Урацил Тимин цитозин
Кроме этих трёх, в составе нуклеиновых кислот обнаруживаются минорные основания: метилцитозин, псевдоуридин, 1-метилурацил и другие.
б) пуриновые
NH2 O
| ||
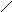


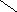

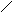


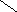 N
N
N
N











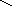
 N
NH
N
NH



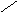


N NH H2N N NH
Аденин Гуанин
Минорные основания: 1-метилгуанин, 1-метиладенин, 1-метилгипоксантин, и другие.
Минорные основания играют важную роль, они определяют взаимодействия с белками и ферментами (в ряде случаев защищают ДНК и РНК от литических ферментов). Они определяют механизм воспроизведения и передачи наследственной информации; механизм памяти.
Примеры мононуклеотидов:
NH2 NH2
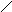











 |
|
|
|

 N
N

 N
N
N
N

 O
=
O
=



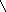
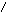
 N
N
N
N
N
N
 O
O OH
O
O OH
|| || /
HC – P – O – H2C 1,9-N-гликозидная O – P 1,1-N- глико
 | связь
| \
зидная связь
| связь
| \
зидная связь
 OH O
CH2
OH
OH O
CH2
OH
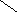
 O
O

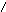




 OH
X
OH
X
АМФ ОН Х
ЦМФ
Встречаются и другие нуклеотиды: ГТФ, АТФ, УГФ, цАМФ.
Роль нуклеотидов: помимо того, что они входят в состав аминокислот, они выполняют ряд важных физиологических функций.


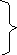 ГТФ
ТДД
ГТФ
ТДД

 АТФ
АДФ участвуют в
трансформации энергии окисления
веществ в энер
АТФ
АДФ участвуют в
трансформации энергии окисления
веществ в энер
гию, используемую в эндергонических процессах.
 ГТФ
ГДФ
ГТФ
ГДФ

Остаток АМФ входит в состав НАД, НАДФ, ФАД и КоА. УТФ, ЦТФ, ГТФ являются коферментами в реакциях переноса моносахаридных остатков (ЦТФ – кофермент холинтрансферазы).
 ц – 3,5 – АМФ
ц – 3,5 – АМФ
ц – 3,5 – ГМФ выполняют роль мессенджеров гормональных сигналов.
Молекула ДНК имеет гигантские размеры, длина ДНК 25 пар хромосом составляет около 1,5 м. 4 11
М (НК) = от 2х10 - 10 дальтон (определялось гидродинамическим и электрономикроскопиче
скими методами).
По локализации выделяют
- ядерную ДНК (больше всего)
-
митохондриальную
-
эписомальную
-
центриольную
-
хлоропластную
По функции: рибосомальная и сателлитная.
Существуют также ДНК вирусов и фагов, но её значительно меньше, чем у бактерий. Количество ДНК в клетке измеряется в ПГ.
Первичная структура нуклеиновых кислот: последовательность мононуклеотидов, связанных 5’3’ фосфатной связью.
ОН OH
| A | А

 O
= P – O – CH2
O = P – O – CH2
O
= P – O – CH2
O = P – O – CH2
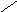



 |
O
| O
|
O
| O

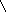 OH
OH
OH
OH





O OH O OH
| Г | У

 O = P – O – CH2
O = P – O – CH2
O = P – O – CH2
O = P – O – CH2

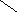


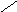
 | O
| O
| O
| O
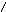


 OH
OH
OH
OH





O OH O OH
| У | Т




 O = P – O –
CH2
O = P – O –
CH2
O = P – O –
CH2
O = P – O –
CH2
| O O


 OH
OH





 ОН ОН
OH
OH
ОН ОН
OH
OH
РНК ДНК
В молекуле ДНК доминирует правило Чаргаффа:
-
Сумма пуринов = сумме пиримидинов.
А+Г = Ц+Т(У)
А +Г
+Г
Т+Ц = 1
-
Количество А и Ц = количеству Г и Т:
А +
Ц = Г+Т или А+Ц
+
Ц = Г+Т или А+Ц
Г+Т = 1
-
В молекуле ДНК: А = Т; Г = Ц.
-
Коэффициент видовой специфичности ДНК:
Г + Ц
К с
= А + Т
с
= А + Т
Он лежит в пределах от 0,4 до 2,5. Кс для человека и животных = 0,5 – 0,8. Для РНК Кс >1, для растений 0,3 – 0,9.
Вторичная структура.
В соответствии с моделью Уотсона и Крика молекула ДНК состоит из двух цепей, образуя правовращающую спираль, в которой обе цепи закручены вокруг одной и той же оси. Удерживаются цепи благодаря водородным связям между азотистыми основаниями, а также за счёт гидрофобных взаимодействий.
Водородные связи возникают между комплементарными азотистыми основаниями: А…Т и Г…Ц. Стабильность А…Т обеспечивается 2-мя водородными связями, а Г…Ц – 3-мя водородными
связями. Длина водородных связей равна 0,3 нм. Обе цепи в молекуле ДНК имеют противоположную направленность, то есть полярность. Это означает, что межнуклеотидная связь в одной цепи имеет направление 5’ 3’, а в другой – 3’ 5’.
HO – P = O
 | CH3
O -------------------------H2N
N HO – P = O
| CH3
O -------------------------H2N
N HO – P = O





 O \ //
\ |
O \ //
\ |





 |
NH------------------N N O
|
NH------------------N N O




 5’
CH2
O N
N
5’
CH2
O N
N


 \\
\\


 3’
O
3’
3’
O
3’

O
O CH2 5’
| |
HO – P = O O

 |
NH2
--------------------------- O N |
|
NH2
--------------------------- O N |




 O /
\\ HO – P = O
O /
\\ HO – P = O
| N |




 CH2
N
------------------------- HN
O
CH2
N
------------------------- HN
O



 O N \\
/ N |
O N \\
/ N |



 O
------------------------------H2N
O
------------------------------H2N
