
- •5. Биологические функции и классификация белков.
- •6. Значение и специфичность действия ферментов.
- •7. Строение фермента.
- •8. Активный центр.
- •9. Определение активности ферментов.
- •10. Локализация ферментов в клетке, маркёрные и органоспецифические ферменты.
- •11. Механизм действия ферментов.
- •12 . Кинетика ферментативных реакций.
- •13. Регуляция активности ферментов.
- •14. Ингибирование ферментов.
- •15 . Номенклатура и классификация. Изоферменты. Изменение активности в энтогенезе.
- •15 . Энзимопатия.
- •16. Обмен веществ. Ката- и анаболизм .
- •17.Биологическое окисление.
- •18. Природа макроэргичности атф.
- •19. Цикл кребса.
- •20 . Тканевое дыхание.
- •21 . Дыхательная цепь.
- •22. Механизм сопряжения окислительного фосфорилирования.
- •23 . Термогенез.
- •24 . Микросомальная дыхательная цепь.
- •25 . Перекисное окисление и антиоксидантная защита.
- •26 . Углеводы и их переваривание.
- •1) Гиалуроновая кислота.
- •2) Кондратин – сульфат
- •3) Гепарин
- •27 . Биологические функции углеводов.
- •28 . Переваривание углеводов .
- •Галактоза
- •Фруктоза
- •29 . Пути метаболизма глюкозы.
- •30 . Синтез и распад гликогена.
- •31.Гликогенозы.
- •32 . Гликогенолиз и гликолиз.
- •33. Механизм гликолитической оксидоредукции. Субстратное фосфорилирование.
- •34 . Спиртовое брожение и метаболизм этанола.
- •34.Эробный распад глюкозы. Окислительное декарбоксилиро -
- •35. Глюконеогенез.
- •36. Гипо - и гипергликемия.
- •37.Регуляция уровня глюкозы в крови.
- •38. Сахарный диабет.
- •39. Липиды . Строение , классификация , биологическая роль .
- •40.Переваривание и всасывание липидов .
- •41. Ресинтез липидов в стенке кишечника .
- •42 . Метаболизм липидов .
- •45. Пути обмена ацетил-КоА . Обмен кетоновых тел .
- •46. Биосинтез триглицеридов.
- •47. Интеграция углеводного и липидного обмена .
- •48. Белковый обмен.
- •49. Состав желудочного сока. Механизм секреции hCl .
- •9. Ряд аминокислот, имеющих диагностическое значение .
- •50. Панкреатический сок.
- •51. Кишечный сок.
- •1.Энтерокиназа .
- •9. Фосфолипаза и липаза .
- •52 . Переваривание белков .
- •53. Гниение белков в толстом кишечнике .
- •54. Механизм всасывания аминокислот и пути их утилизации .
- •55.Трансаминирование аминокислот .
- •56. Токсичность аммиака и пути его обезвреживания .
- •57. Биосинтез мочевины .
- •58. Цикл кребса-гензеляйта .
- •59. Пути вступления аминокислот в цтк .
- •60. Декарбоксилирование аминокислот .
- •61.Метаболизм серина и глицина .
- •62. Нарушение обмена глицина .
- •63. Обмен серосодержащих аминокислот и триптофана.
- •64. Метаболизм триптофана.
- •65. Обмен фенилаланина и тирозина.
- •66. Обмен гистидина, глутамина, аспарагина, пролина.
- •67. Интеграция углеводного, белкового и липидного обмена.
- •72. Распад пуриновых нуклеотидов. Подагра.
- •73. Синтез и распад пиримидиновых оснований.
61.Метаболизм серина и глицина .
Глицин – единственная аминокислота у которой отсутствует ассиметрический атом углерода.В результате распада 2 аминокислот образуется 7 молекул :
-ацетилКоА -фумарат
-ацетоацетилКоА - сукцинилКоА
-ПВК - ЩУК
-аКГК
То есть аминокислоты , которые идут на биосинтез белка , н могут запасаться и идут на образование интермедиатов промежуточного обмена .
Глицин и серин – заменимые аминокислоты , синтезируются из метаболитов гликолиза :
CH2 – O – PO3H2 НАД НАД*Н2 СH2 – O – PO3H2 ГЛУ аКГК CH2 – O – РО3Н2

 |
|
|
|
|
|
C

 H
– OH C = O
CH – NH2
H
– OH C = O
CH – NH2
| 3-фосфоглицератдегидрогеназа | трансаминирование |
COOH COOH COOH
3-фосфоглицериновая кислота 3-фосфооксиПВК 3-фосфосерин
CH2 – OH
Фн | В6


 - CH – NH2
ПВК
АЛА
- CH – NH2
ПВК
АЛА
фосфатаза | -NH3
COOH
серин
Глицин связан с серином через ТГФК ( тетрагидрофолиевую кислоту ) – это и есть путь биосинтеза глицина .
CH2 – NH2 N5 , N10 – CH2OH – ТГФК CH2 – OH

 |
|
|
|
COOH сериноксиметилаза CH – NH2 + ТГФК
глицин |
COOH
серин
Пути метаболизма .




 Глутатион
ГЛИ
пурины
Глутатион
ГЛИ
пурины







 Глюкуровая кислота
белки
Глюкуровая кислота
белки
Креатин щавелевая кислота
Треонин серин желчные гем
кислоты
Оксидазы L-аминокислот глицин не дезаминирует . В тканях открыт специфический флавопротеид – глициноксидаза , который осуществляет эту реакцию :
O
//
 CH2
– COOH + O2 + HOH
C – H + NH3
+ H2O2
CH2
– COOH + O2 + HOH
C – H + NH3
+ H2O2
| |
NH2 C = O
\
ОН глиоксиловая кислота
Глиоксиловая кислота окисляется до муравьиной кислоты :

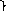 О
О
 СОН
– СООН
НСООН
+ СО2
СОН
– СООН
НСООН
+ СО2
НАДФ*Н2 НАДФ
Н
 СООН
+ ТГФК N5,N10
– CH2
– OH – ТГФК
СООН
+ ТГФК N5,N10
– CH2
– OH – ТГФК
формильное производное ТГФК ,
которое служит донатором оксиметильной
группы при взаимопревращении ГЛИ и СЕР
Возможно и такие взаимопревращения ГЛИ и ТРЕ :
O
// треонинальдолаза CH3
С
 интез
ТРЕ CH3
– C – H2N
– CH2
– COOH |
интез
ТРЕ CH3
– C – H2N
– CH2
– COOH |
\ CH – OH
H |
CH – NH2
|
COOH
Основным путём метаболизма ГЛИ считается его распад на СО2 и NH3 :
H 2N
– CH2 – COOH + ТГФК
CO2
+ NH3 + N5,N10
– CH2 – ТГФК
2N
– CH2 – COOH + ТГФК
CO2
+ NH3 + N5,N10
– CH2 – ТГФК
М еханизм
этой реакции включает участие
глицинрасщепляющей ферментной системы
, состоящей из 4 белков : Р-белка ,
содержащего пиридоксальфосфат ; Н-белка
, содержащего липоевую кислоту ; Т-белка
, содержащего ТГФК и L-белка
( липоамиддегидрогеназа ) . Биологический
смысл данного пути метаболизма ГЛИ
состоит в том , что образуется
активный одноуглеродный фермент
N5,N10
– CH2
– ТГФК , который используется в
уникальных реакциях биосинтеза
метионина , пуриновых полипептидов .
Глицин входит в состав коллагена (
30-35% ). Коллаген составляет 50% общего
белка организма и из этого количества
1/3 – глицин . Глицин участвует в синтезе
ацетилхолина ( основной медиатор
парасимпатической нервной системы )
основной
стимулирующий
агент
CH3
еханизм
этой реакции включает участие
глицинрасщепляющей ферментной системы
, состоящей из 4 белков : Р-белка ,
содержащего пиридоксальфосфат ; Н-белка
, содержащего липоевую кислоту ; Т-белка
, содержащего ТГФК и L-белка
( липоамиддегидрогеназа ) . Биологический
смысл данного пути метаболизма ГЛИ
состоит в том , что образуется
активный одноуглеродный фермент
N5,N10
– CH2
– ТГФК , который используется в
уникальных реакциях биосинтеза
метионина , пуриновых полипептидов .
Глицин входит в состав коллагена (
30-35% ). Коллаген составляет 50% общего
белка организма и из этого количества
1/3 – глицин . Глицин участвует в синтезе
ацетилхолина ( основной медиатор
парасимпатической нервной системы )
основной
стимулирующий
агент
CH3
N5,N10-CH2OH-ТГФК - СО2 SAM |
Г

 лицин
серин H2N
– CH2 – CH2
– OH HO – CH2
– CH2 – N – CH3
лицин
серин H2N
– CH2 – CH2
– OH HO – CH2
– CH2 – N – CH3
этаноламин O холин |
|| CH3
+ CH3 – COSKoA
(CH3)3N
– (CH2)2
– O – C – CH3 + HS-KoA
CH3 – COSKoA
(CH3)3N
– (CH2)2
– O – C – CH3 + HS-KoA
ацетилхолин
Глицин играет роль в синтезе креатина . Реакция синтеза протекает в две стадии : первая стадия образования гуанидинацетата (гликоциамина ) – осуществляется в почках при участии глицинтрансаминазы :
HN = C – NH2 HN = C – NH2 NH2
| | |
NH H2N NH + (CH2)3
| + | | |
 (CH2)3
CH2
– COOH
CH2
– COOH CH –
NH2
(CH2)3
CH2
– COOH
CH2
– COOH CH –
NH2
| глицин гликоциамин |
CH – NH2 COOH
| орнитин
COOH
Лизин
Вторая стадия протекает в печени при участии гуанидинацетатметилтрансферазы :
HN = C – NH2
|

 NH SAM
NH SAM
|
CH2 – COOH
гликоциамин
аденин
H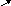 N
= C – NH2
N
= C – NH2
 | S –
аденозилгалоцистеин CH2
– SH
| S –
аденозилгалоцистеин CH2
– SH
N – CH3 |

 |
CH2
|
CH2
CH2 – COOH АТФ |
Креатин CH – NH2
|
OH креатинфосфокиназа COOH
|
NH = C – NH – P = O
 | | АДФ
HN = C – NH
| | АДФ
HN = C – NH
H3C – N OH |
 | фосфатаза
H3C –
N
| фосфатаза
H3C –
N
CH2 – COOH - Фн |
Креатинфосфат CH2 – CO
креатинин
Креатинфосфат – буфер макроэргов мыщцы ( главный энергетический ресурс мышц ). Креатинин обладает седативным действием , эндогенный фактор нейрогуморального контроля , при депрессии концентрация креатинина возрастает . Креатин при помощи микросомального окисления в печени превращается в бензойную кислоту , которая в свою очередь взаимодействуя с глицином даёт гиппуровую кислоту :





 COOH
CO
– NH – CH2
COOH
CO
– NH – CH2








 + H2N
– CH2
– COOH
|
+ H2N
– CH2
– COOH
|
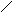
 - HOH
COOH
- HOH
COOH
бензойная кислота гиппуровая кислота
В данном случае глицин играет детоксикационную функцию . Эта реакция лежит в основе пробы Квика .
Глицин принимает участие в синтезе пуринового кольца .



 CO2
глицин
CO2
глицин
CH N






N5,N10-CH2-ТГФК



 АСП N
C
CH
метиленовое
АСП N
C
CH
метиленовое

 производное
ТГФК
производное
ТГФК
 HC
C
HC
C




Формильное
производное N NH

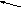 ТГФК
ТГФК
N5,N10-CH2OH-ТГФК амидный азот ГЛИ
Глицин поддерживает SH-группы активных центров ферментов в восстановленном состоянии, тем самым поддерживает активность этих ферментов.
Г лутатион
– антиоксидант, входит в систему
защиты эритроцитов от окисляющего
воздействия О2:
ЦТК
лутатион
– антиоксидант, входит в систему
защиты эритроцитов от окисляющего
воздействия О2:
ЦТК
 HbFe(2) G-S-S-G
НАД*Н2 ПЦ
HbFe(2) G-S-S-G
НАД*Н2 ПЦ


 НАДФ*Н2
НАДФ*Н2
 О2
О2
Ферменты:
1.метгемоглобинредуктаза
HbFe(3) 2GSH НАД 2.глутатионредуктаза
НАД
Синтез глутатиона .
COOH
| COOH O
CH – NH2 | ||

 |
+ CH – NH2
АТФ
COOH – CH
– (CH2)2
– C – NH –
CH – COOH
|
+ CH – NH2
АТФ
COOH – CH
– (CH2)2
– C – NH –
CH – COOH
(CH2)2 | Mg |
| CH2 – SH CH2
COOH ЦИС |
 ГЛУ
SH
ГЛУ
SH
O O
|| ||
HOOC – CH – (CH2)2 – C – NH – CH – C – NH – CH2 – COOH
| |
NH2 CH2 – SH
Глутатион определяет ОВП клетки. При диабете, алкогольной интоксикации уровень глутатиона падает. Глицин принимает участие в синтезе ГЕНа ( смотри биохимию крови ):


 Глицин
+ сукцинилКоА аминолевулиновая
кислота порфобилиноген ГЕН
Глицин
+ сукцинилКоА аминолевулиновая
кислота порфобилиноген ГЕН
Глицин обеспечивает синаптическую передачу на уровне спинного мозга, его антагонистом является стрихнин.
