
- •Виробничі процеси та обладнання об’єктів автоматизації конспект лекцій доцента кафедри нгтт і т Гаєвої Любов Іванівни
- •1.1 Зміст і задачі дисципліни
- •1.2 Класифікація технологічних процесів
- •1.3 Хімічний і фракційний склади нафти
- •1.3.1 Парафінові вуглеводні
- •1.3.2 Нафтенові вуглеводні
- •1.3.3 Ароматичні вуглеводні
- •1.3.4 Фракційний склад нафти
- •2 Основні поняття масообмінних процесів
- •2.1 Загальні ознаки масообмінних процесів
- •2.2 Способи визначення складу фаз
- •2.3 Основне рівняння масопередачі
- •3.1 Призначення і суть процесу абсорбції
- •3.2 Використання абсорбції в нафтогазовій промисло-вості
- •3.3 Робота системи абсорбер-десорбер неперервної дії
- •3.4 Параметри контролю і регулюванню при абсорбції та десорбції
- •3.4.1 Температура в абсорбері
- •3.4.2. Тиск в абсорбері
- •3.4.3 Питома витрата абсорбенту
- •3.4.4 Рівень рідини в низу абсорбера і десорбера
- •3.4.5 Температура в десорбері
- •3.4.6 Тиск в десорбері
- •3.4.7 Рушійна сила абсорбції
- •3.4.8 Площа контакту і час контакту абсорбенту і газової суміші
- •3.5 Вимоги до абсорбентів
- •3.6 Типи абсорберів
- •4 Процес адсорбції
- •4.1 Призначення і суть процесу
- •4.2 Використання адсорбції в нафтогазовій промисло-вості
- •4.3 Робота системи адсорбер-десорбер періодичної дії
- •4.4 Робота системи адсорбер-десорбер неперервної дії
- •4.5 Параметри контролю і регулювання при адсорбції і десорбції
- •4.5.1 Температура в адсорбері
- •4.5.2 Тиск в адсорбері
- •4.5.3 Питома витрата адсорбенту
- •4.5.4 Температура в десорбері
- •4.5.5 Тиск в адсорбері
- •4.5.6 Природа газової суміші і властивості адсорбенту
- •5 Процес ректифікації
- •5.1 Призначення і суть процесу
- •5.2 Використання процесу в нафтогазовій промисло-вості
- •5.3 Будова і робота простої ректифікаційної колони
- •5.4 Будова і робота складної ректифікаційної колони
- •5.5 Параметри контролю і регулювання при ректифікації
- •5.5.1 Температура верха колони
- •5.5.2 Температура низу колони
- •5.5.3 Тиск в колоні
- •5.5.4 Температура і витрата сировини
- •5.5.5 Рівень залишку в колоні
- •5.5.6 Температура на тарілках виводу бокових фракцій
- •5.6 Матеріальний баланс ректифікаційної колони
- •5.7 Крива рівноваги фаз: її побудова та рівняння
- •5.8 Ізобарні температурні криві
- •5.9 Графічний метод визначення кількості тарілок в колоні
- •5.10 Визначення температурного режиму простої ректифікаційної колони
- •5.11 Визначення геометричних розмірів колони: діаметра і висоти
- •6 Процес екстракції
- •6.1 Призначення і суть процесу
- •6.2 Використання в нафтогазовій промисловості
- •6.3 Методи екстракції
- •6.3.1 Однократна екстракція
- •6.3.2 Багатократна екстракція
- •6.3.3 Протитічна екстракція
- •6.4 Будова і робота екстракційної колони
- •6.5 Параметри контролю і регулювання при екстракції
- •6.5.1 Температура
- •6.5.2 Співвідношення розчинник: сировина
- •6.5.3 Якість розчинника
- •6.5.4 Рівень границі розділу фаз
- •6.6 Визначення складу фаз за допомогою трикутної діаграми
- •7 Теплові процеси
- •7.1 Теплообмінні апарати
- •7.1.1 Кожухотрубні теплообмінники з нерухомим трубними решітками
- •7.1.2 Теплообмінні апарати з температурними компенсаторами
- •7.1.3 Теплообмінні апарати з плаваючою головкою (з рухомою трубною решіткою)
- •7.1.4 Теплообмінні апарати з u-подібними трубками
- •7.1.5 Теплообмінники типу «труба в трубі»
- •7.1.6 Випарники з паровим простором
- •7.1.7 Апарати повітряного охолодження
- •7.2 Класифікація і маркування апо
- •7.3 Маркування та розрахунок кожухотрубчастих теплообмінників
- •7.3.1 Маркування кожухотрубчастих теплообмінників
- •7.3.2 Розрахунок кожухотрубчастих теплообмінників
- •7.4 Трубчасті печі
- •7.5 Умовні позначення типових трубчастих печей
- •8 Товарні нафтопродукти
- •8.1 Технологічна класифікація нафт
- •8.2 Основні напрями переробки нафти
- •8.3 Класифікація і характеристика товарних нафтопродуктів
- •8.4 Палива
- •8.4.1 Карбюраторні палива
- •8.4.2 Реактивні палива
- •8.4.3 Дизельні палива
- •8.4.4 Газотурбінні палива
- •8.4.5 Котельні палива
- •8.5 Нафтові оливи
- •8.5.1 Моторні оливи
- •8.5.2 Трансмісійні оливи
- •8.5.3 Індустріальні оливи
- •8.5.4 Турбінні і компресорні оливи
- •8.5.5 Спеціальні оливи
- •8.6 Пластичні мастила
- •8.7 Парафіни, церезини, вазеліни
- •8.8 Нафтові розчинники та ароматичні вуглеводні
- •8.9 Нафтові бітуми
- •8.10 Нафтовий кокс
- •8.11 Технічний вуглець
- •8.12 Присадки до палив та олив
- •9.2 Методи руйнування нафтових емульсій
- •9.3 Будова і робота електродегідраторів
- •9.3.2 Горизонтальні електродегідратори
- •9.4 Схема електрознесолювальної установки та її опис
- •9.5 Параметри контролю і регулювання на установці
- •9.5.1 Температура і тиск в електродегідраторі
- •10.2 Первинна переробка нафти
- •10.2.1 Призначення первинної переробки і класифікація установок авт
- •10.2.2 Сировина і одержувані продукти
- •10.2.3 Принципова технологічна схема авт з трьохкратним випаровуванням і їх опис
- •10.3 Термічні процеси переробки нафти (коксування)
- •10.3.1 Призначення, і суть процесу
- •10.3.2 Механізми реакцій
- •10.3.3 Сировина і одержувані продукти
- •10.3.4 Технологічна схема установки сповільненого коксування і її опис
- •10.3.5 Параметри контролю і регулювання на установці
- •10.3.5.1 Якість сировини
- •10.3.5.2 Температура входу сировини в реактор
- •10.3.5.3 Тиск в реакторі
- •10.3.5.4 Час перебування сировини в реакторі
- •10.3.5.5 Коефіцієнт рециркуляції
- •10.4 Каталітичні процеси
- •10.4.1 Каталітичний реформінг
- •10.4.1.1 Призначення, суть і хімізм процесу
- •10.4.1.2 Сировина і одержувані продукти
- •10.4.1.3 Каталізатори
- •10.4.1.4 Принципова технологічна схема установки каталітичного риформінгу і її опис
- •10.4.2 Параметри контролю і регулювання на установці
- •10.4.2.1 Якість сировини
- •10.4.2.2 Температура на вході в реактори
- •10.4.2.3 Об’ємна швидкість подачі сировини
- •10.4.2.4 Тиск в реакторах
- •10.4.2.5 Кратність циркуляції водневмісного газу
- •10.5.2 Сировина і одержувані продукти
- •10.5.3 Каталізатор
- •10.5.4 Принципова технологічна схема установки каталітичного крекінгу з ліфт- реактором і її опис
- •10.5.5 Параметри, що впливають на процес
- •10.5.5.1 Якість сировини
- •10.5.5.2 Температура в реакторі
- •10.5.5.3 Час контакту сировини і каталізатора
- •10.5.5.4 Кратність циркуляції каталізатора
- •10.5.5.5 Тиск в реакторі
- •11 Процеси очищення продуктів
- •11.1 Процес гідроочищення
- •11.1.1 Призначення установки, суть і хімізм процесу
- •11.1.2 Сировина і одержувані продукти
- •11.1.3 Умови проведення процесу
- •11.1.4 Каталізатори
- •11.1.5 Принципова технологічна схема гідроочищення дизельного палива в паровій фазі і її опис
- •11.1.6 Параметри контролю і регулювання на установці
- •11.1.6.1 Якість сировини
- •11.1.6.2 Температура в реакторі
- •11.1.6.3 Тиск в реакторі
- •11.1.6.4 Об’ємна швидкість подачі сировини і кратність циркуляції водневмісного газу
- •11.2 Процес карбамідної депарафінізації
- •11.2.1 Призначення і суть процесу
- •11.2.2 Сировина і одержувані продукти
- •11.2.3 Параметри, що впливають на процес
- •11.2.3.1 Якість сировини
- •11.2.3.2 Склад і концентрація карбаміду
- •11.2.3.3 Співвідношення карбамід-сировина
- •11.2.3.4 Температура
- •11.2.3.5 Склад і кількість активатора та розчинника
- •11.2.3.6 Час контакту сировини з карбамідом
- •11.3 Опис технологічної схеми установки карбамідної депарафінізації дизельного палива
1.3.4 Фракційний склад нафти
Нафта складається з великої кількості вуглеводів, які мають різну температуру кипіння. Виділяти з нафти окремі вуглеводні непотрібно і тому їх розділяють на фракції, що мають певні температурні межі.
При перегонці нафту розділяють на такі фракції:
-
газ (С2 – С4);
-
бензин (початок кипіння - 180 °С);
-
гас (140 – 280 °С);
-
дизельне паливо (180 – 350 °С).
Фракції, які википають до 350 °С називаються світлими нафтопродуктами і їх одержують в атмосферних колонах. Залишок атмосферної перегонки називається мазут (фракції більше 350 °С).
Для
подальшого одержання фракцій олив, які
википають в межах 350![]() 500
°С або вакуумного газойлю, мазут
переганяють у вакуумних колонах. Залишком
вакуумних колон є гудрон (температура
кипіння більше 500 °С). Нафтопродукти,
які википають при температурі 350 °С і
більше, називаються темними.
500
°С або вакуумного газойлю, мазут
переганяють у вакуумних колонах. Залишком
вакуумних колон є гудрон (температура
кипіння більше 500 °С). Нафтопродукти,
які википають при температурі 350 °С і
більше, називаються темними.
2 Основні поняття масообмінних процесів
2.1 Загальні ознаки масообмінних процесів
Масообмінні процеси володіють загальними ознаками, які коротко можна сформулювати наступним чином:
-
вони використовуються для розділення сумішей;
-
в любому процесі приймають участь по крайній мірі дві фази: рідка і парова (перегонка, ректифікація), рідка і газова (абсорбція), тверда і парогазова (адсорбція, екстракція), дві рідких (екстракція);
-
перехід речовини з однієї в іншу фазу проходить за рахунок дифузії;
-
рушійною силою масообмінних процесів є різниця концентрацій компонентів у фазах. При цьому перенесення маси речовини здійснюється за рахунок різниці концентрацій фактично в одній фазі G і рівноважної з фактичною в іншій фазі L. Процес протікає в напрямі тої фази, в якій концентрація компоненту менша (рис. 1.1);
![]()


![]()
![]()
![]()


![]()
![]()
![]()
![]()
![]()
![]()
а б
а – з фази G в фазу L; б – з фази L в фазу G
Рисунок 1.1 Схема перенесення речовини між двома фазами
-
перенесення речовини з однієї фази в іншу проходить через границю фаз;
-
дифузійні процеси зворотні, тобто напрям процесу визначається законами фазової рівноваги, фактичними концентраціями компонентів в обох фазах і зовнішніми умовами (температура, тиск);
-
перехід речовини з однієї фази в іншу закінчується при досягненні динамічної рівноваги.
2.2 Способи визначення складу фаз
Однорідна фізично виділена густина системи називається фазою. До загальноприйнятих ознак за якими розрізняють фази в системі відносяться: колір, оптична густина, текстура і загальний вигляд. Системи, які містять одну фазу називаються гомогенними, а які містять дві і більше – гетерогенними.
Склад багатокомпонентних сумішей в газовому і рідкому стані може задаватися масовими, мольними, об’ємними частками, масово-об’ємними, відносними масовими або молярними концентраціями.
Якщо
маса всієї фази буде G,
а маси компонентів, що знаходяться в
ній
![]() ,
то масові частки компо-нентів визначаються:
,
то масові частки компо-нентів визначаються:
![]() (в
газовій фазі);
(в
газовій фазі);
![]() (в рідкій фазі); (2.1)
(в рідкій фазі); (2.1)
Так
як
![]() ,
то
,
то
![]() (2.2)
(2.2)
Якщо
суміш складається з
![]() кмолей, а кількість кмолей компонентів
-
кмолей, а кількість кмолей компонентів
-
![]() ,
то мольні частки компонентів визначаються:
,
то мольні частки компонентів визначаються:
![]() (в
газовій фазі);
(в
газовій фазі);
![]() (в
рідкій фазі) (2.3)
(в
рідкій фазі) (2.3)
При цьому кількість кмоль суміші і окремих компонентів визначається:
![]() (2.4)
(2.4)
де
![]() - молярні маси суміші і окремих компонентів,
кг/кмоль.
- молярні маси суміші і окремих компонентів,
кг/кмоль.
Так
як
![]() ,
то
,
то
![]() (2.5)
(2.5)
Відношення об’єму компонента, який входить в суміш, до загального об’єму суміші називається об’ємною часткою компонента в суміші.
![]() (2.6)
(2.6)
Так
як
![]() ,
то
,
то
![]() (2.7)
(2.7)
Для газових сумішей об’ємний склад співпадає з мольним оскільки об’єми 1 кмоля любого газу при однакових умовах рівні.
Для сумішей рідин об’ємна частка визначається:
![]() ;
(2.8)
;
(2.8)
Запишемо взаємозв’язок між масовими, об’ємними і мольними частками.
![]() -
для одного компонента
-
для одного компонента
![]() -
для суміші
-
для суміші
![]() ,
,
так
як
![]() ,
то
,
то
![]() ,
(2.9)
,
(2.9)
де
![]() - густина компонента і суміші, кг/м
- густина компонента і суміші, кг/м![]() ;
;
Молярна маса суміші визначається за формулами
![]() ,
(2.10)
,
(2.10)
або через масові частки
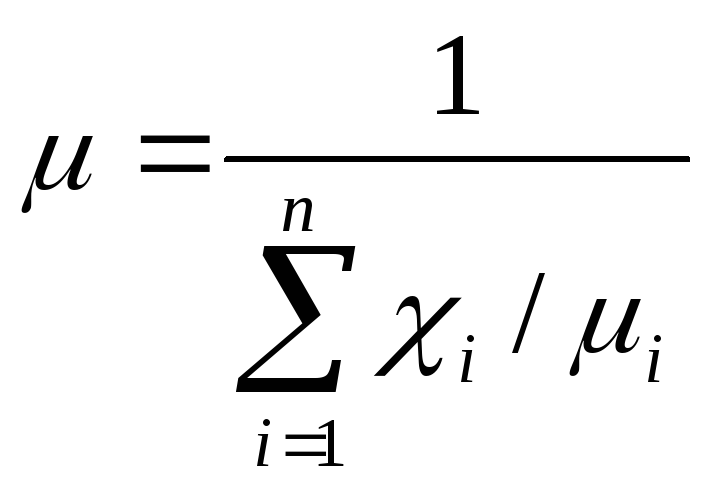 ,
(2.11)
,
(2.11)
Склад
сумішей можна визначити через маси
компонентів, що містяться в 1 м![]() суміші. В цьому випадку визначений склад
суміші називається масово-об’ємною
концентрацією:
суміші. В цьому випадку визначений склад
суміші називається масово-об’ємною
концентрацією:
![]() ,
(2.12)
,
(2.12)
Якщо підсумувати масово-об’ємні концентрації усіх компонентів, то одержимо масу суміші в одиниці її об’єму, тобто густину суміші:
![]() (2.13)
(2.13)
Рівняння (2.13) можна видозмінити якщо чисельник і знаменник поділити на масу суміші
![]() (2.14)
(2.14)
Склад бінарної суміші зручно визначити у відносних концентраціях, тобто у вигляді відношення маси або кількості кмолей одного компонента до маси або кількості молей іншого.
Якщо вміст одного компонента складає x, а другого 1-x, то відносний масовий склад дорівнює:
![]() (2.15)
(2.15)
Для визначення відносних мольних концентрацій необхідно знайти кількість кмолей двох компонентів в суміші і взяти їх відношення:
![]() (2.16)
(2.16)
