
УЧЕБНИК ВНУТРЕННИЕ БОЛЕЗНИ
.pdf
Рентгенологические признаки ОА (табл. 2-2).
1. Рентгенологические характеристики, определяющие стадию
ОА:
а) величина остеофитов; б) сужение суставной щели;
в) склероз субхондральной кости; г) маленькие ложные кисты со склеротическими стенками, обычно
расположенные в субхондральной кости; д) измененные размеры концов кости, в частности головки бедра.
Основные рентгенологические признаки ОА: сужение суставной щели, остеофитоз, субхондральный остеосклероз (рис. 2-2) .
|
|
|
|
|
|
Таблица 2-2 |
|
Рентгенографические критерии для определения |
|||||
|
|
ОА(Kellgren - Lawrence, 1975). |
|
|||
Стадия 0 |
|
нет ОА |
отсутствуют |
рентгенологические |
||
|
|
|
признаки. |
|
|
|
Стадия 1 |
|
сомнительный ОА |
мелкий |
остеофит, |
сомнительное |
|
|
|
|
значение. |
|
|
|
Стадия 2 |
|
минимальный ОА |
четкий |
остеофит, |
неизмененная |
|
|
|
|
суставная щель. |
|
|
|
Стадия 3 |
|
средний ОА |
умеренное сужение суставной щели, |
|||
|
|
|
множественные остеофиты. |
|||
Стадия 4 |
|
выраженный ОА |
значительное сужение сус тавной щели |
|||
|
|
|
(почти не прослеживается) со |
|||
|
|
|
склерозом |
субхондральной кости, |
||
|
|
|
грубые остеофиты |
|
|
|
Рис. 2-2. Остеоартроз коленных суставов (3 ст. по Келлегрену).
31

Лабораторных критериев для данного заболевания не существует. Для дифференциальной диагностики: клинический анализ крови, ревматоидный фактор, уровень мочевой кислоты.
Перед началом лечения: общий анализ крови, мочи, креатинин сыворотки, сывороточные аминотрансферазы с целью определения возможных противопоказаний для назначения противовоспалительной терапии.
Анализ синовиальной жидкости. В целях дифференциальной диагностики - только при наличии синовита. Для ОА характерен невоспалительный характер синовиальной жидкости: прозрачная, вязкая, с
концентрацией лейкоцитов менее 2000/мм3. |
|
|
|
||||||
Критерии диагностики. |
|
|
|
|
|
|
|
||
Диагноз |
«ОА» |
ставят |
на |
основании |
клинических |
и |
|||
рентгенологических критериев (Альтман и др., 1991) (табл. 2-3.). |
|
||||||||
|
|
|
|
|
|
|
|
Таблица 2-3 |
|
Диагностические критерии остеоартроза (по Altmanet., 1991) |
|
||||||||
Клинические критерии |
|
|
Клинические, |
лабораторные |
и |
||||
|
|
|
|
рентгенологические критерии |
|
||||
|
|
Коленные суставы |
|
|
|
||||
1. Боль и |
|
|
|
1. Боль и |
|
|
|
|
|
2а. Крепитация |
|
|
|
2. Остеофиты или |
|
|
|
||
26. Утренняя скованность <30 мин |
|
За. СЖ, характерная для остеоартроза (или возраст |
|||||||
2в. Возраст >38 лет или |
|
|
≥40 лет) |
|
|
|
|
||
За. Крепитация |
|
|
|
36. Утренняя скованность <30 мин |
|
||||
36. Утренняя скованность ≤30 мин |
|
Зв. Крепитация |
|
|
|
||||
Зв. Костные разрастания или |
|
|
|
|
|
|
|
|
|
4а. Отсутствие крепитации |
|
|
|
|
|
|
|
|
|
46. Костные разрастания |
|
|
|
|
|
|
|
|
|
Чувствительность — 89% |
|
|
Чувствительность — 94% |
|
|
||||
Специфичность — 88% |
|
|
Специфичность — 88% |
|
|
|
|||
|
|
Тазобедренные суставы |
|
|
|
||||
1. Боль и |
|
|
|
1. Боль и не менее двух критериев из трѐх |
|
||||
2а. Внутренняя ротация <15° |
|
|
2а. СОЭ <20 мм/ч |
|
|
|
|||
26. СОЭ <15 мм/ч |
|
|
|
26. Остеофиты |
|
|
|
||
(или сгибание в |
тазобедренном |
2в. Сужение суставной щели |
|
|
|||||
суставе >115°) или |
|
|
|
|
|
|
|
|
|
3а. Внутренняя ротация <15° |
|
|
|
|
|
|
|
|
|
3б. Утренняя скованность <60 мин |
|
|
|
|
|
|
|
||
3в. Возраст >50 лет |
|
|
|
|
|
|
|
|
|
3г. Боль при внутренней ротации |
|
|
|
|
|
|
|
||
Чувствительность — 86% |
|
|
Чувствительность — 89% |
|
|
||||
Специфичность — 75% |
|
|
Специфичность — 91% |
|
|
|
|||
|
|
|
Суставы кистей |
|
|
|
|||
1. Боль продолжительная или скованность
2. Костные разрастания двух и более суставов из 10 оцениваемых*
3. Менее двух припухших пястно-фаланговых суставов
4а. Костные разрастания, включающие 2 и более дистальных межфаланговых сустава (2-й и 3-й дистальные межфаланговые суставы могут приниматься во внимание в двух критериях: 2 и 4а) или
32
46. Деформация одного и более суставов из 10 оцениваемых*
Чувствительность — 93%
Специфичность — 91%
* 2-й и 3-й дистальные межфаланговые суставы; 2-й и 3-й проксимальные межфаланговые суставы; 1-й запястно-пястный сустав обеих кистей.
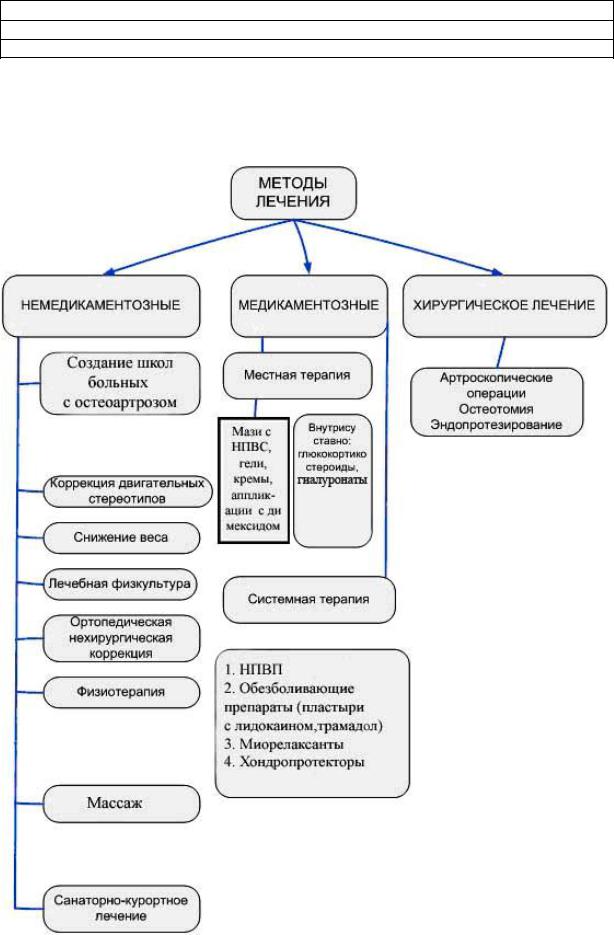
Лечение ОА.
33
Цели лечения:
•Обеспечить понимание больным своего заболевания и умение управлять им: изменение образа жизни, применение физических упражнений, поддерживающих функцию суставов, защита суставов.
•Уменьшить боль.
•Улучшить функциональное состояние суставов и предотвратить развитие деформации суставов и инвалидизации больного.
•Улучшить качество жизни больных.
•Предотвратить дальнейшее разрушение суставного хряща.
•Избежать побочных эффектов фармакотерапии и обострения
сопутствующих заболеваний.
Нефармакологические методы.
1. Обучение больных должно быть обязательным компонентом всех терапевтических программ при ОА, проводиться с учетом индивидуальных особенностей больного и включать рекомендации по изменению образа жизни, снижению веса и необходимости выполнения физических упражнений (уровень доказательности А, В).
2.Больным ОА с избыточным весом (ИМТ более 25 кг/м2) рекомендуется уменьшение веса (уровень доказательности В,С).
3.Больным ОА коленных суставов необходимы регулярные физические упражнения, направленные на укрепление силы четырехглавой
мышцы бедра и увеличение объема движений, а также аэробные нагрузки (уровень доказательности А). При ОА тазобедренных суставов тоже требуется выполнение лечебной физкультуры, особенно силовых упражнений (уровень доказательности С).
4. При поражении медиального отдела коленного сустава, варусной деформации или нестабильности коленного сустава могут использоваться коленные ортезы (уровень доказательности В) и клиновидные ортопедические стельки (уровень доказательности С). Рекомендуется хождение с тростью в руке, противоположной поражѐнной нижней конечности (уровень доказательности С). При ОА 1–го запястно -пястного сустава применяются шинирование и ортезы (уровень доказательности В).
5. Физиотерапевтические методы. При ОА коленных суставов с признаками воспаления можно рекомендовать применение холодовых аппликаций (пакеты со льдом, массаж льдом) (уровень доказательности В). Для уменьшения боли при ОА коленных и суставов кистей рекомендуются тепловые процедуры (уровень доказательности В), чрезкожная электронейростимуляция (уровень доказательности А,В). У некоторых больных может использоваться акупунктура (уровень доказательности В).
Лекарственная терапия.
Главный симптом ОА - боль. Поэтому анальгетическая терапия, как эффективный контроль над болью, является важным направлением в лечении ОА.
34

Симптоматические лекарственные средства быстрого действия. Нестероидные противовоспалительные препараты (НПВП).
НПВП показаны при ОА в случае неэффективности парацетамола, а также при наличии признаков воспаления (уровень доказательности А). При сильной боли в суставах лечение следует начинать сразу с НПВП (уровень доказательности А). НПВП применяются в минимальной эффективной дозе назначаются на максимально короткие сроки (уровень доказательности А).
Неселективные НПВП.
Ибупрофен 1200-2400 мг/сут в 4 приема.
Аркетал (кетопрофен) 100-400 мг/сут в 3-4 приема. Флурбипрофен 100-300 мг/сут в 3-4 приема. НАКЛОФЕН (диклофенак)75 мг в/м – 1 раз в сутки
КСЕФОКАМ (лорноксикам) (8 мг) по 1 т. 1-2 раза в день; в/в или в/м в дозе 8-16 мг.
Селективные НПВП.
Мелоксикам 7,5 в/м - 15 мг/сут в 1 прием. НАЙЗ(нимесулид) (100 мг) по 1 т – 2 раза в день.
Специфические ингибиторы ЦОГ 2.
Целекоксиб 100-200 мг/сут в 1-2 приема;эторикоксиб 60-120 мг/сут. Для профилактики НПВП-гастропатии необходимо назначить
ингибиторы протонной помпы –пантопразол 40 мг - 1 раз в сутки.
Базисная терапия остеоартроза (уровень доказательности А)
представлена в таблице 2-4
|
|
Таблица 2-4 |
|
Базисная терапия остеоартроза |
|||
Препарат |
Суточная доза |
Длительность |
|
|
|
приема |
|
|
|
|
|
ХОНДРОКСИД |
750 мг 2 раза/сут |
1-2 года |
|
(Хондроитин сульфат) |
первые 3 нед., затем |
|
|
|
по 500 мг 2 раза в |
|
|
|
сутки |
|
|
|
|
|
|
СТОПАРТРОЗ |
1500 мг 1 раз в день |
1-2 года |
|
(Глюкозамина сульфат) |
|
|
|
|
|
|
|
хондроитин сульфат 400 |
2 капс. 3 раза в день |
1-2 года |
|
мг+глюкозамина сульфат |
|
|
|
500 мг, глюкозамин сульфат |
|
|
|
250 мг + ибупрофен 100 мг + |
2 капс. 3 раза в день |
1-2 года |
|
хондроитина сульфат 200 мг) |
|
|
|
Диацереин (диафлекс) |
50 мг. 2 раза в день |
не менее 4 мес. |
|
|
|
|
|
Пиаскледин |
1 капс. в сутки |
1-2 года |
|
|
|
|
|
35
АЛФЛУТОП - стерильный экстракт морских организмов, стимулирующий синтез гиалуроновой кислоты и тормозящий синтез гиалуронидазы.
Внутрисуставные инъекции алфлутопа эффективны, даже при наличии признаков синовита. Они выполняются курсами по 5 инъекций в каждый сустав, 1 инъекция в 3 дня, 2-3 раза в течение года.
Прекрасно переносится и сопоставимо по эффективности с внутрисуставным введением, в/м введениеалфлутопа ( 2 мл ) ежедневно в течение 10 дней.
Внутрисуставное введение глюкокортикоидов (ГЛК) показано при ОА коленных суставов с симптомами воспаления (уровень доказательности А). При ОА ГКС вводят в коленные суставы для уменьшения боли и симптомов воспаления. Рекомендуется использовать однократные инъекции метилпреднизолона (40 мг) или триамцинолона (20 мг или 40 мг). Не рекомендуется выполнять более 2–3 инъекций в год в один и тот же сустав.
Симптоматические лекарственные средства медленного действия.
Препараты-ортезы. Препараты, содержащие хондроитин сульфат и глюкозамин сульфат рекомендуются при ОА для уменьшения боли, улучшения функции суставов; эффект сохраняется в течение нескольких месяцев после их отмены, хорошо переносятся больными ( уровень доказательности А).
Гиалуроновая кислота (демпфер и лумбрикант), применяется только для внутрисуставных инъекций); по 5 инъекций в каждый коленный сустав
(уровень доказательности А).
Хирургическое лечение: эндопротезирование суставов (уровень доказательности А).
Показания: ОА с выраженным болевым синдромом, не подающимся консервативному лечению; нарушение функции сустава (до развития значительной деформации, нестабильности сустава, контрактуры и мышечной атрофии).
Артроскопические манипуляции : лаваж коленных суставов, удаление «суставной мыши».
36
ГЛАВА 3. ПОДАГРА.
Подагра–системное тофусное заболевание, развивающееся в связи с воспалением в местах отложения кристаллов моноурата натрия (МУН) у лиц с гиперурикемией, обусловленным внешнесредовыми и/или генетическими факторами.
Термин ―подагра‖ имеет греческое происхождение и составлен из слов ―podus‖ - нога и ―agrios‖ – жестокий.
В книге "Болезни древних людей" Рохлин Д.Г. описывает обнаруженные им плюсневые кости со следами подагры при раскопках богатых погребений в Новгороде ("...вот следствие постоянных пиров с объеданием и возлияниями"). В древности люди умоляли подагру о пощаде: "Будь милостива к нам, ты, всему миру известная и всех устрашающая подагра, пусть причиняемая тобою боль будет легкой и кратковременной, а не ужасной и невыносимой, пусть она не превращает нас в калек" (Лукиан).
Эпидемиология.
По экспертным оценкам подагрой страдает не менее 0,1-1% взрослого населения. Частота подагрического артрита в различных популяциях колеблется и составляет от 5 до 50 на 1000 мужчин и 1 —9 на 1000 женщин, а число новых случаев в год - соответственно 1 —3 на 1000 у мужчин и 0,2 на 1000 у женщин. Соотношение мужчин и женщин составляет 2-7:1.
Пик заболеваемости: 40—50 лет у мужчин, 60 лет и старше у женщин.
Этиология.
Подагра возникает вследствие различных по происхождению нарушений метаболизма мочевой кислоты (синтеза и/или выведения), приводящих к стойкому повышению еѐ уровня в крови – гиперурикемии. Европейская лига по борьбе с ревматизмом рекомендует считать гиперурикемией уровень мочевой кислоты выше 360 ммоль/л.
Выделяют первичную и вторичную подагру (гиперурикемию).
Вторичной подагра признается тогда, когда она является лишь одним из синдромов другого заболевания, при котором по тем или иным причинам (врожденным или приобретенным) возникают нарушения метаболизма мочевой кислоты.
Источником мочевой кислоты являются пуриновые основания (аденин и гуанин) – составные части нуклеиновых кислот, а также пуриновые нуклеозиды, из которых образованы АТФ и подобные соединения. Метаболизм пуриновых оснований регулируется несколькими ферментами.
Среди больных первичной подагрой, причиной заболевания являются нарушения выведения мочевой кислоты почками.
Выведение уратов через почки включает четыре фазы: фильтрацию в клубочках, реабсорбцию в проксимальных канальцах, секрецию уратов,
37
постсекреторную реабсорбцию. У больных подагрой наблюдаются как изолированные дефекты различных фаз выведения мочевой кислоты (снижение секреции, повышение реабсорбции), так и комбинированных нарушений.
Стойкая многолетняя гиперурикемия является обязательным и главным условием развития подагры, максимальной выраженности достигает уже к 25 годам. Однако средний возраст начала подагры составляет только 47 лет, т.к. для развития первичной подагры, как правило, необходимо сочетание гиперурикемии с такими приобретенными факторами, как употребление в пищу большого количества продуктов, содержащих много пуринов; избыточная масса тела.
Известен афоризм: ―Партнерами гиперурикемии являются друзья изобилия‖.
Причины развития вторичной подагры обусловлены повышенным образованием уратов, замедлением выведения уратов почками или комбинацией этих нарушений.
Причины повышенного образования мочевой кислоты:
истинная полицитемия, вторичная полицитемия у больных с врожденными ―синими‖ пороками сердца и с хроническими заболеваниями легких;
острые и хронические лейкозы, множественная миелома, лимфомы, карцинома почек и другие злокачественные опухоли;
гиперпаратиреоз;
псориаз (гиперурикемия связана с площадью поражения кожи);
гемоглобинопатии (серповидно-клеточная анемия, талассемия и др.), врожденная гемолитическая анемия, пернициозная анемия и другие мегалобластные анемии;
некоторые врожденные дефекты коаг уляции (болезнь Виллебранда);
инфекционный мононуклеоз (гиперурикемия в первые 10 дней);
гипоксемия;
значительная перегрузка скелетных мышц;
избыточное употребление в пищу продуктов, богатых пуринами;
злоупотребление алкогольными напитками;
гликогеноз I, III, V и VII типа.
Причины замедления выведения мочевой кислоты почками:
терминальнаяпочечная недостаточность;
заболевания почек, не сопровождающиеся почечной недостаточностью, характеризующиеся преимущественно
интерстициальными (канальцевыми) изменениями (поликистоз почек, анальгетическая нефропатия, гидронефроз);
кетоацидоз; ацидоз, обусловленный избытком молочной кислоты;
прием диуретических средств;
обезвоживание;
38
бериллиоз.
Другие (не вполне выясненные) причины:
-свинцовая интоксикация (в том числе, использование суррогатов алкогольных напитков, контакт с красителями, использование керамической посуды);
-гиперпаратиреоз;
-саркоидоз;
-гипотиреоз;
-нерациональное и неконтролируемое применение различных
медикаментов (адельфан и его аналоги, препараты, содержащие тиазиды и сам гипотиазид, малые дозы салицилатов, сульфаниламидные средства, антибиотики широкого спектра действия, кофеин, теофиллин (эуфиллин), циклоспорин, пиразинамид, этамбутамол);
- артериальная гипертензия.
Патогенетические механизмы.
1.Кристаллизация уратов
2.Фагоцитоз кристаллов мочевой кислоты лейкоцитами
3.Высвобождение большого количества лизосомальных ферментов
4.Участие кининов и простагландинов
Клиническая картина.
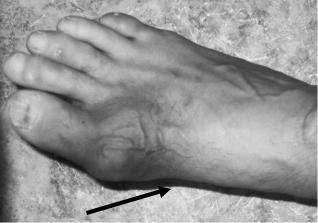
Острая подагрическая атака развивается внезапно, чаще ночью или рано утром, развивается резкая боль в одном суставе, как правило, нижней конечности. Боль быстро, в течение нескольких часов, нарастает до нестерпимой, появляется выраженная припухлость пораженного сустава с покраснением кожи над ним. Движения в воспаленном суставе становятся практически невозможными, также как и опора на пораженную конечность. Боль значительна и без движений, нередко ее усиление вызывает даже легкое касание сустава одеялом. Боль, отек сустава и гиперемия кожи над ним могут быть столь выраженными, что напоминают флегмону (рис. 3-1). Длительность атаки без лечения варьирует от 1 до 10 дней.
Рис. 3-1. Острый артрит при подагре Для первой ―атаки‖ подагры типичен моноартрит и
преимущественное поражение суставов большого пальца стопы (как
39

плюснефалангового, так и межфалангового), а также голеностопных и коленных суставов. Менее типичным для подагры считается воспаление локтевых, лучезапястных суставов и суставов кисти, и очень редким – поражение плечевых, тазобедренных суставов и др.
Особенностью подагры у женщин является значительно более частое поражение во время первой ―атаки‖ болезни суставов кистей (у одной трети больных).
Во время приступа подагры нередко отмечается умеренная лихорадка, лейкоцитоз и повышение СОЭ. Острый подагрический артрит характеризует внезапное, быстрое нарастание интенсивных болей, как правило, в одном суставе, гиперемия кожных покровов, припухлость и нарушение функции пораженного сустава.
Межприступная подагра и рецидивирующий подагрический артрит.
В отсутствие лечения повторный приступ обычно развивается в течение 1-го года.Характерно сокращение продолжительности бессимптомного периода, приступы становятся более тяжѐлыми, затрагивают новые суставы, иногда имеют полиартикулярный мигрирующий характер; отмечается воспаление периартикулярных тканей, образование единичных тофусов в тканях, обычно безболезненных.
Хроническая тофусная подагра характеризуется отложением кристаллов мочевой кислоты (тофусов) в тканях организма - в суставах, сухожилиях, мышцах, ушных раковинах, легких и др. Тофусы могут образовываться и в почках, головном мозге, сердце. В последнем случае могут изменяться клапаны сердца с формированием подагрического порока сердца.
Тофусы - это депозиты (скопления) кристаллов моноурата натрия (солей мочевой кислоты), окруженные соединительной тканью и имеющие вид узелков (рис. 3-2).
Рис. 3-2. Тофусы
40
