
- •Предисловие
- •Химическая термодинамика, как теоретическая основа биоэнергетики Предмет, методы и основные понятия химической термодинамики
- •Термодинамические системы: изолированные, закрытые, открытые, гомогенные, гетерогенные
- •Термодинамические параметры
- •Внутренняя энергия системы
- •Форма обмена энергии с окружающей средой
- •Первое начало термодинамики. Тепловые эффекты химических реакций
- •1. В изолированной системе сумма всех видов энергии есть величина постоянная.
- •Изобарный и изохорный процессы. Энтальпия. Тепловые эффекты химических реакций
- •Термохимия. Закон Гесса
- •Влияние температуры и давления на тепловой эффект реакции
- •Использование закона Гесса в биохимических исследованиях
- •Энтропия. Второй закон термодинамики Энтропия
- •Второе начало термодинамики. Свободная энергия Гиббса
- •Принцип энергетического сопряжения
- •Химическое равновесие Обратимые и необратимые реакции. Константа равновесия
- •Смещение химического равновесия. Принцип Ле-Шателье
- •Учение о растворах Растворы
- •Физические свойства н2о и строение ее молекул
- •Механизм образования растворов
- •Растворимость веществ. Факторы, влияющие на растворимость
- •Влияние природы веществ на растворимость
- •Влияние давления на растворимость веществ
- •Влияние температуры на растворимость веществ
- •Влияние электролитов на растворимость веществ
- •Взаимная растворимость жидкостей
- •Способы выражения состава растворов
- •Термодинамические аспекты процесса растворения. Идеальные растворы
- •Коллигативные свойства разбавленных растворов
- •Диффузия и осмос в растворах
- •Роль осмоса в биологических процессах
- •Давление насыщенного пара растворителя над раствором. Закон Рауля
- •Следствия из закона Рауля
- •1) Растворы кипят при более высокой температуре, чем чистый растворитель;
- •2) Растворы замерзают при более низкой температуре, чем чистый растворитель.
- •Применение методов криоскопии и эбуллиоскопии
- •Коллигативные свойства растворов электролитов. Изотонический коэффициент Вант-Гоффа
- •Электролитическая диссоциация Электролиты и неэлектролиты. Теория электролитической диссоциации
- •Общая характеристика электролитов
- •Слабые электролиты
- •Сильные электролиты
- •Диссоциация воды. Водородный показатель
- •Теория кислот и оснований. Буферные растворы Теория кислот и оснований
- •Буферные растворы Определение буферных систем и их классификация
- •Механизм действия буферных систем
- •Вычисление рН и рОн буферных систем. Уравнение Гендерсона-Гассельбаха
- •Буферная емкость
- •Буферные системы человеческого организма
- •Нарушения кислотно-оснóвного равновесия крови. Ацидоз. Алкалоз
- •Химическая кинетика и катализ Кинетика химических реакций
- •Понятие о скорости химической реакции. Закон действующих масс
- •Кинетическая классификация химических реакций. Понятие о молекулярности и порядке химической реакции Порядок и молекулярность простых химических реакций
- •Понятие о сложных химических реакциях
- •Классификация сложных реакций
- •Измерение скорости химической реакции
- •Влияние температуры на скорость химической реакции
- •Катализ Общие положения и закономерности катализа
- •Механизм гомогенного и гетерогенного катализа
- •Особенности каталитической активности ферментов
- •2. Другим важным отличием ферментов от катализаторов небелковой природы является их высокая специфичность, т.Е. Избирательность действия.
- •Физическая химия дисперсных систем Определение дисперсных систем
- •Классификация дисперсных систем и их общая характеристика
- •Классификация дисперсных систем по агрегатному состоянию вещества дисперсной фазы и дисперсионной среды
- •Классификация по взаимодействию между частицами дисперсной фазы или степени структурированности системы
- •Классификация по характеру взаимодействия дисперсной фазы с дисперсионной средой
- •Методы получения дисперсных систем
- •Диспергирование жидкостей
- •Диспергирование газов
- •Конденсационные методы
- •Методы физической конденсации
- •Методы химической конденсации
- •Очистка золей
- •Компенсационный диализ и вивидиализ
- •Молекулярно-кинетические свойства золей
- •Броуновское движение
- •Диффузия
- •Седиментация в золях
- •Осмотическое давление в золях
- •Оптические свойства золей
- •Рассеяние света (опалесценция)
- •Оптические методы исследования коллоидных систем Ультрамикроскоп
- •Механизм образования и строение коллоидной частицы – мицеллы
- •1. Получение золя берлинской лазури:
- •2. Получение с помощью гидролиза FeCl3 золя гидроксида железа (III).
- •3. Получение золя As2s3:
- •Электрокинетические свойства золей
- •Устойчивость гидрофобных коллоидных систем. Коагуляция золей Виды устойчивости золей
- •Теория коагуляции Дерягина-Ландау-Фервея-Овербека
- •Влияние электролитов на устойчивость золей. Порог коагуляции. Правило Шульца-Гарди
- •Чередование зон коагуляции
- •Коагуляции золей смесями электролитов
- •Скорость коагуляции
- •Коллоидная защита
- •Роль процессов коагуляции в промышленности, медицине, биологии
- •Растворы высокомолекулярных соединений
- •1) Своеобразное тепловое движение частиц растворенного вещества, схожее с броуновским движением мицелл в золях;
- •Общая характеристика высокомолекулярных соединений
- •Классификация полимеров
- •Набухание и растворение вмс
- •Термодинамические аспекты процесса набухания
- •Давление набухания
- •Свойства растворов высокомолекулярных соединений
- •Осмотическое давление растворов вмс
- •Онкотическое давление крови
- •Вязкость растворов полимеров
- •Свободная и связанная вода в растворах
- •Полиэлектролиты
- •Факторы, влияющие на устойчивость растворов полимеров. Высаливание
- •Электрохимия растворы электролитов как проводники второго рода. Электропроводность растворов электролитов
- •Эквивалентная электропроводность растворов
- •Практическое применение электропроводности
- •Равновесные электродные процессы
- •Металлический электрод
- •Измерение электродных потенциалов
- •Окислительно-восстановительные электроды
- •1. Переход окисленной формы в восстановленную и наоборот заключается только в обмене между ними электронами:
- •Диффузионный и мембранный потенциалы
- •Химические источники электрического тока. Гальванические элементы
- •Потенциометрия
- •Содержание
Влияние электролитов на устойчивость золей. Порог коагуляции. Правило Шульца-Гарди
Фактором, вызывающим коагуляцию, может быть любое внешнее воздействие, нарушающее агрегативную устойчивость системы. Кроме изменения температуры в его роли может выступать механическое воздействие (интенсивное встряхивание, перемешивание, перекачивание по трубам), действие света и различного рода других излучений, действие электрических разрядов. Однако наиболее эффективным способом является добавление в золь электролитов. Они быстро и резко влияют на толщину ДЭС и величину ζ-потенциала частицы.
Многочисленные исследования показали, что добавление в золь практически любого электролита вызывает уменьшение его устойчивости. Однако с заметной скоростью коагуляция золя будет происходить, если концентрация добавляемого электролита в растворе достигает строго определенной величины.
Та минимальная концентрация электролита в коллоидном растворе, которая вызывает протекание в нем явной коагуляции, называется порогом коагуляции данного электролита. Она измеряется в ммоль/дм3 или в моль/м3 и обозначается СП или γ.
Величину,
обратную порогу коагуляции, называют
коагулирующей способностью
и обозначают VK:
VK
=
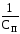 .
.
Порог коагуляции обычно определяют визуально и опытным путем, поэтому его величина может зависеть от ряда субъективных факторов. Например, от момента его фиксирования после внесения электролита, от метода наблюдения, от концентрации исследуемого золя и др. Поэтому все это необходимо учитывать, особенно, если проводится сравнительный анализ воздействия одного и того же электролита на разные золи или разных электролитов на один и тот же золь.
Опытным путем было установлено, что коагулирующее воздействие на коллоидный раствор оказывают не весь электролит, а только те его ионы, знак заряда которых противоположен заряду гранулы (или совпадает со знаком заряда потенциалопределяющих ионов) мицеллы.
Так, коагуляцию золя с отрицательно заряженными гранулами вызывают катионами электролита, а золя с положительно заряженными гранулами – его анионами.
Очень часто порог коагуляции и коагулирующую способность определяют не по концентрации всего электролита в растворе, а только его коагулирующего иона.
В 1882 г. Г. Шульц, а несколько позже и М. Гарди показали, что коагулирующая способность ионов электролита напрямую зависит от величины их заряда. Причем, с увеличением величины заряда иона на единицу его коагулирующая способность возрастает в 10 и более раз. Такая закономерность получила название правило Шульца-Гарди и носит приближенный характер. Это связано с тем, что, кроме величины заряда, на коагулирующую способность иона оказывает влияние и ряд других факторов: природа иона, его радиус и способность к сольватации (гидратации для водных растворов).
У ионов с одинаковой величиной заряда коагулирующая способность возрастает с увеличением их радиуса и уменьшением степени сольватации. По данному признаку ионы располагают в так называемые лиотропные ряды Гофмейстера:
Li+, Na+, K+, Rb+, Cs+;
Mg2+, Ca2+, Sr2+, Ba2+;
F–,Cl–,Br–,I–

увеличение коагулирующей способности ионов электролита
Таким образом, коагулирующая способность ионов электролита в растворе напрямую связана с их способностью к адсорбции на твердой поверхности.
В зависимости от механизма действия различают 2 вида коагуляции золей электролита: концентрационнуюинейтрализационную.
Концентрационная коагуляциянаблюдается при увеличении содержания в золе электролита, не вступающего в химическое взаимодействие с компонентами двойного электрического слоя мицеллы. Такие электролиты называютсяиндифферентными. Их ионы не способны достраивать кристаллическую решетку агрегата и не могут реагировать с потенциалопределяющими ионами, образуя нерастворимые соединения. При увеличении концентрации такого электролита в растворе диффузный слой мицеллы сжимается из-за перехода ее противоионов и коагулирующих ионов электролита в адсорбционный слой. Одновременно с этим процессом уменьшается и электрокинетический потенциал гранулы (но не поверхностный потенциал).
Наблюдения показали, что для большинства коллоидных систем явная коагуляция наступает, если значение ζ-потенциала достигает одного и того же критического значения: ≈ 0,029-0,03 В.
В идеале при добавлении электролита ζ-потенциал гранулы может уменьшаться до нуля. Такое состояние коллоидной системы называется изоэлектрическим. В этом случае у коллоидных частиц отсутствует и диффузный слой. Такие системы являются максимально неустойчивыми.
При нейтрализационной коагуляцииионы прибавляемого электролита способны взаимодействовать с потенциалопределяющими ионами агрегата, образуя на его поверхности нерастворимые соединения. В этом случае наряду с ζ-потенциалом уменьшается и общий (поверхностный или электротермодинамический) потенциал частицы.
Если электролит в коллоидный раствор вводят не сразу, а небольшими порциями через определенные промежутки времени, может наблюдаться явление привыкания.Привыканиемназывается повышение устойчивости золя к коагулирующему действию электролита в случае уменьшения скорости его поступления. Этот факт учитывают в медицине при внутривенных инъекциях больших объемов растворов лекарственных веществ.
При смешивании двух устойчивых коллоидных растворов с разноименно заряженными гранулами нередко происходит образование осадка, называемое взаимной коагуляциейзолей.
