
- •Предисловие
- •Химическая термодинамика, как теоретическая основа биоэнергетики Предмет, методы и основные понятия химической термодинамики
- •Термодинамические системы: изолированные, закрытые, открытые, гомогенные, гетерогенные
- •Термодинамические параметры
- •Внутренняя энергия системы
- •Форма обмена энергии с окружающей средой
- •Первое начало термодинамики. Тепловые эффекты химических реакций
- •1. В изолированной системе сумма всех видов энергии есть величина постоянная.
- •Изобарный и изохорный процессы. Энтальпия. Тепловые эффекты химических реакций
- •Термохимия. Закон Гесса
- •Влияние температуры и давления на тепловой эффект реакции
- •Использование закона Гесса в биохимических исследованиях
- •Энтропия. Второй закон термодинамики Энтропия
- •Второе начало термодинамики. Свободная энергия Гиббса
- •Принцип энергетического сопряжения
- •Химическое равновесие Обратимые и необратимые реакции. Константа равновесия
- •Смещение химического равновесия. Принцип Ле-Шателье
- •Учение о растворах Растворы
- •Физические свойства н2о и строение ее молекул
- •Механизм образования растворов
- •Растворимость веществ. Факторы, влияющие на растворимость
- •Влияние природы веществ на растворимость
- •Влияние давления на растворимость веществ
- •Влияние температуры на растворимость веществ
- •Влияние электролитов на растворимость веществ
- •Взаимная растворимость жидкостей
- •Способы выражения состава растворов
- •Термодинамические аспекты процесса растворения. Идеальные растворы
- •Коллигативные свойства разбавленных растворов
- •Диффузия и осмос в растворах
- •Роль осмоса в биологических процессах
- •Давление насыщенного пара растворителя над раствором. Закон Рауля
- •Следствия из закона Рауля
- •1) Растворы кипят при более высокой температуре, чем чистый растворитель;
- •2) Растворы замерзают при более низкой температуре, чем чистый растворитель.
- •Применение методов криоскопии и эбуллиоскопии
- •Коллигативные свойства растворов электролитов. Изотонический коэффициент Вант-Гоффа
- •Электролитическая диссоциация Электролиты и неэлектролиты. Теория электролитической диссоциации
- •Общая характеристика электролитов
- •Слабые электролиты
- •Сильные электролиты
- •Диссоциация воды. Водородный показатель
- •Теория кислот и оснований. Буферные растворы Теория кислот и оснований
- •Буферные растворы Определение буферных систем и их классификация
- •Механизм действия буферных систем
- •Вычисление рН и рОн буферных систем. Уравнение Гендерсона-Гассельбаха
- •Буферная емкость
- •Буферные системы человеческого организма
- •Нарушения кислотно-оснóвного равновесия крови. Ацидоз. Алкалоз
- •Химическая кинетика и катализ Кинетика химических реакций
- •Понятие о скорости химической реакции. Закон действующих масс
- •Кинетическая классификация химических реакций. Понятие о молекулярности и порядке химической реакции Порядок и молекулярность простых химических реакций
- •Понятие о сложных химических реакциях
- •Классификация сложных реакций
- •Измерение скорости химической реакции
- •Влияние температуры на скорость химической реакции
- •Катализ Общие положения и закономерности катализа
- •Механизм гомогенного и гетерогенного катализа
- •Особенности каталитической активности ферментов
- •2. Другим важным отличием ферментов от катализаторов небелковой природы является их высокая специфичность, т.Е. Избирательность действия.
- •Физическая химия дисперсных систем Определение дисперсных систем
- •Классификация дисперсных систем и их общая характеристика
- •Классификация дисперсных систем по агрегатному состоянию вещества дисперсной фазы и дисперсионной среды
- •Классификация по взаимодействию между частицами дисперсной фазы или степени структурированности системы
- •Классификация по характеру взаимодействия дисперсной фазы с дисперсионной средой
- •Методы получения дисперсных систем
- •Диспергирование жидкостей
- •Диспергирование газов
- •Конденсационные методы
- •Методы физической конденсации
- •Методы химической конденсации
- •Очистка золей
- •Компенсационный диализ и вивидиализ
- •Молекулярно-кинетические свойства золей
- •Броуновское движение
- •Диффузия
- •Седиментация в золях
- •Осмотическое давление в золях
- •Оптические свойства золей
- •Рассеяние света (опалесценция)
- •Оптические методы исследования коллоидных систем Ультрамикроскоп
- •Механизм образования и строение коллоидной частицы – мицеллы
- •1. Получение золя берлинской лазури:
- •2. Получение с помощью гидролиза FeCl3 золя гидроксида железа (III).
- •3. Получение золя As2s3:
- •Электрокинетические свойства золей
- •Устойчивость гидрофобных коллоидных систем. Коагуляция золей Виды устойчивости золей
- •Теория коагуляции Дерягина-Ландау-Фервея-Овербека
- •Влияние электролитов на устойчивость золей. Порог коагуляции. Правило Шульца-Гарди
- •Чередование зон коагуляции
- •Коагуляции золей смесями электролитов
- •Скорость коагуляции
- •Коллоидная защита
- •Роль процессов коагуляции в промышленности, медицине, биологии
- •Растворы высокомолекулярных соединений
- •1) Своеобразное тепловое движение частиц растворенного вещества, схожее с броуновским движением мицелл в золях;
- •Общая характеристика высокомолекулярных соединений
- •Классификация полимеров
- •Набухание и растворение вмс
- •Термодинамические аспекты процесса набухания
- •Давление набухания
- •Свойства растворов высокомолекулярных соединений
- •Осмотическое давление растворов вмс
- •Онкотическое давление крови
- •Вязкость растворов полимеров
- •Свободная и связанная вода в растворах
- •Полиэлектролиты
- •Факторы, влияющие на устойчивость растворов полимеров. Высаливание
- •Электрохимия растворы электролитов как проводники второго рода. Электропроводность растворов электролитов
- •Эквивалентная электропроводность растворов
- •Практическое применение электропроводности
- •Равновесные электродные процессы
- •Металлический электрод
- •Измерение электродных потенциалов
- •Окислительно-восстановительные электроды
- •1. Переход окисленной формы в восстановленную и наоборот заключается только в обмене между ними электронами:
- •Диффузионный и мембранный потенциалы
- •Химические источники электрического тока. Гальванические элементы
- •Потенциометрия
- •Содержание
Общая характеристика электролитов
Одни электролиты в растворах полностью распадаются на ионы. Они называются сильными.
Другие электролиты только частично распадаются на ионы, т.е. большая часть их молекул остаётся в растворе в недиссоциированном виде. Такие электролиты называются слабыми.
Данное свойство вещества не абсолютно, и зависит не только от его природы, но и от природы растворителя. Чем больше диэлектрическая постоянная растворителя, тем сильнее его ионизирующая слабость. Так, в водных растворах (ε(Н2О) = 80).LiClиNaClведут себя как сильные электролиты. Но если их растворить в уксусной кислоте (ε = 6) или ацетоне (ε = 21), то они начинают проявлять свойства слабых электролитов.
В водных растворах сильными электролитами являются соли, растворимые основания (образованные, как правило, щелочными и щелочноземельными металлами), некоторые неорганические или минеральные кислоты (HCl, HBr, HI, H2SO4, HNO3 и др.).
В то же время многие органические кислоты, некоторые неорганические кислоты (HNO2, HF, H2S, H2SiO3, H3PO4 и т.д.), нерастворимые в Н2О основания ведут себя как слабые электролиты.
Вещества, в которых частицы связаны различными видами химической связи, распадаются на ионы сперва по ионным связям
KНSO4K++ НSO4–,
а затем – по наиболее полярным ковалентным связям
НSO4–Н++SO42–.
Гетеролитический разрыв малополярных или неполярных ковалентных связей в процессах диссоциации таких веществ, как правило, не происходит.
Количественно процесс распада молекул электролита на ионы оценивается с помощьюстепени электролитической диссоциации α.
Степень диссоциации – это отношение числа распавшихся на ионы молекул вещества к общему числу его молекул в растворе (распавшихся и нераспавшихся):
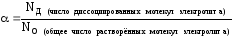
NО=NД+NH (число непродиссоциированных молекул электролита в растворе)
Так как число частиц вещества (N) и их химическое количество (n) связаны между собой соотношениемN=n∙NA, то степень диссоциации можно ещё рассчитать и другим способом:

Для сильных электролитов α близка к единице. Практически все их молекулы в растворе находятся в диссоциированном виде, процесс ассоциации протекает крайне незначительно.
В связи с этим
в уравнениях диссоциации данных веществ
вместо знака обратимости « »
ставят знак «»
(т.е. используют стрелку только в
направлении распада), например:
»
ставят знак «»
(т.е. используют стрелку только в
направлении распада), например:
HCl H+ + Cl–
KOН K+ + OH–
K2SO42K++SO42–
Слабые электролиты
Для слабых электролитов степень диссоциации очень мала (α<<1). Так, для воды при 20оС α ≈ 1 ∙ 10–9. Это означает, что только одна молекула из миллиарда распадается на ионы. В растворах слабых электролитов, наряду с диссоциацией, непрерывно протекает и обратный процесс – ассоциация. С течением времени между ними устанавливается химическое равновесие, которое может быть смещено в ту или иную сторону.
В результате диссоциации электролита происходит увеличение числа его частиц в растворе. Это позволяет экспериментально определить степень диссоциации по измерению тех свойств раствора, которые зависят только от количества содержащихся в нём частиц растворённого вещества, но не от их природы, размеров, массы. К таким свойствам относятся температура кипения и замерзания раствора, осмотическое давление и некоторые другие.
Для растворов слабых электролитов значения α, определённые различными способами, как правило, совпадают и всегда значительно меньше единицы, что хорошо согласуется с теорией Аррениуса.
Как показали экспериментальные исследования, степень диссоциации слабых электролитов зависит от температуры раствора и его концентрации.
Таблица 8.Изменение степени диссоциации уксусной кислоты в зависимости от ее молярной концентрации в растворе
|
Ссн3соон, моль/дм3 |
0,2 |
0,1 |
0,05 |
0,01 |
0,005 |
0,001 |
|
α, % |
0,95 |
1,4 |
1,9 |
4,2 |
6,0 |
12,4 |
При повышении температуры раствора степень диссоциации увеличивается, т.к. при этом лучше обеспечивается поляризация и облегчается последующий разрыв ковалентной полярной связи в молекулах электролита. При понижении температуры α уменьшается.
Возрастает α и при уменьшении концентрации растворов, т.е. при их разбавлении (табл. 8), т.к. при этом толщина разделяющей ионы водной прослойки становится больше, поэтому электростатическое взаимодействие между ними, приводящее к ассоциации ионов в молекулы, наблюдается реже.
При бесконечно большом разведении степень диссоциации электролита стремится к своему максимальному значению, т.е. к единице (рис. 30).
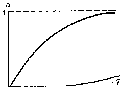
Рис. 30. Изменение степени электролитической диссоциации α с разбавлением V(схема)
Таким образом, для слабых электролитов α не является постоянной величиной. Поэтому их способность к распаду на ионы удобнее сравнивать по константе диссоциации, которая представляет собой константу равновесия обратимой реакции электролитического разложения молекул электролита.
Например:
HNO2
 H+ +
NO2–
H+ +
NO2–
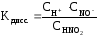
где СН+, СNO2–, CHNO2 – равновесные молярные концентрации ионов H+, NO2– и непродиссоциированных молекул HNO2.
Константа диссоциации слабых электролитов не зависит от их концентрации в растворе даже при значительном разбавлениии и при данной температуре остается постоянной величиной (табл. 9). С увеличением температуры раствора константа диссоциации слабых электролитов во многих случаях изменяется сложным образом (рис. 31).
Таблица 9.Зависимость величиныKдисс.уксусной кислоты в растворе от ее молярной концентрации при Т = 298K
|
Ссн3соон, моль/дм3 |
0,1 |
0,05 |
0,0012 |
0,0003 |
|
Kдисс. |
1,845·10–5 |
1,845·10–5 |
1,850·10–5 |
1,855·10–5 |
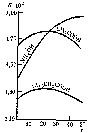
Рис. 31. Зависимость константы диссоциации K некоторых слабых электролитов в водных растворах от температурыt (°С)
Чем меньше Kдисс., тем более слабым является данный электролит. Например, уксусная кислота (Kдисс.= 1,85·10–5) почти в 220 000 раз сильнее циановодороднойHCN(Kдисс.= 4,8·10–10) и примерно в 10 раз слабее муравьиной кислоты (Kдисс.= 1,8·10–4).
Существуют слабые электролиты (многоосновные кислоты, многокислотные основания) процесс распада которых на ионы протекает ступенчато, т.е. в несколько стадий. При этом каждая стадия характеризуется своей величиной константы диссоциации.
Например, в 2 стадии осуществляется диссоциация сероводородной кислоты:
1) H2S
 H+ +
HS–
H+ +
HS–
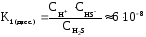
2) HS–
 H+ +
S2–
H+ +
S2–
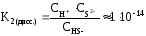
Суммарное уравнение реакции диссоциации H2Sвыглядит следующим образом:
H2S 2H++S2–
2H++S2–

Величина константы диссоциации для суммарного уравнения и значения констант диссоциации отдельных стадий связаны между собой соотношением:
Kсумм.=K1·K2·K3…
При ступенчатой диссоциации распад слабого электролита на каждой последующей стадии происходит в меньшей степени, чем на предыдущей, т.е. K1 > K2 > K3 и т.д. Это объясняется тем, что отрыв иона происходит уже не от нейтральной молекулы (как на первой стадии), а от частицы со все более возрастающим зарядом и требует поэтому больших затрат энергии.
Часто для оценки силы слабого электролита вместо величины константы диссоциации используют ее десятичный логарифм, взятый с обратным знаком (pK)
pK= -lgKдисс.
В этом случае чем больше величина pK, тем более слабым является электролит.
Степень диссоциации слабого электролита уменьшается, если внести в его раствор даже в небольшом количестве сильный электролит, содержащий в своем составе одноименные ионы.
Например, если в раствор СН3СООН добавить ацетат натрияCH3COONa, то за счет диссоциации соли концентрация ацетат-ионов СН3СОО–резко увеличится. В соответствии с принципом Ле Шателье это приведет к смещению равновесия реакции
СН3СООН СН3СОО–+ Н+
СН3СОО–+ Н+
в левую сторону. Аналогичный эффект наблюдается, если в раствор СН3СООН добавить небольшое количество сильной кислоты.
Таким образом, диссоциация слабой кислоты подавляется в присутствии собственной соли или сильной кислоты. То же можно сказать и о слабом основании, диссоциация которого будет подавляться в сильнощелочной среде или в присутствии соли, содержащей одноименный катион.
При добавлении большого количества соответствующего сильного электролита слабый электролит практически не будет диссоциировать.
Существует количественная связь между степенью диссоциации слабого электролита и его концентрацией в растворе, называемая законом разбавления Оствальда.
Для бинарного электролита, молекулы которого распадаются только на 2 иона, можно показать, что
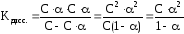
где С – исходная молярная концентрация электролита в растворе; α – степень диссоциации электролита; С ∙ α – концентрация распавшихся молекул электролита и образовавшихся при этом ионов.
Вильгельм
Фридрих Оствальд (1853 – 1932).
Родился в Риге. Учился в Дерптском университете, здесь же в 1878 г. получил степень доктора. С 1882 г. был профессором Рижского университета. С 1887 г. перешел на кафедру физической химии в Лейпциге, где работал до 1928 г.
В. Оствальд изучал электрическую проводимость органических кислот. Познакомившись с работами С. Аррениуса, он стал его сторонником. В. Оствальд внес существенный вклад в теорию электролитической диссоциации. В частности, он предложил свой известный закон разбавления, показал, что аналитические реакции в растворах следует рассматривать как ионные, и объяснил цвет растворов многих веществ специфической окраской ионов. В. Освальду принадлежат также исследования по катализу.
Так как степень
диссоциации слабых электролитов мала,
то можно пренебречь этой величиной в
знаменателе. Тогда K=C·α2,
откуда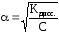 или учитывая, что
или учитывая, что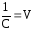 (разведение
или разбавление раствора), то
(разведение
или разбавление раствора), то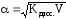 .
.
Для электролитов, молекулы или формульные единицы которых распадаются на большее число ионов, закон разбавления Оствальда носит более сложный характер.
