
- •Предисловие
- •Химическая термодинамика, как теоретическая основа биоэнергетики Предмет, методы и основные понятия химической термодинамики
- •Термодинамические системы: изолированные, закрытые, открытые, гомогенные, гетерогенные
- •Термодинамические параметры
- •Внутренняя энергия системы
- •Форма обмена энергии с окружающей средой
- •Первое начало термодинамики. Тепловые эффекты химических реакций
- •1. В изолированной системе сумма всех видов энергии есть величина постоянная.
- •Изобарный и изохорный процессы. Энтальпия. Тепловые эффекты химических реакций
- •Термохимия. Закон Гесса
- •Влияние температуры и давления на тепловой эффект реакции
- •Использование закона Гесса в биохимических исследованиях
- •Энтропия. Второй закон термодинамики Энтропия
- •Второе начало термодинамики. Свободная энергия Гиббса
- •Принцип энергетического сопряжения
- •Химическое равновесие Обратимые и необратимые реакции. Константа равновесия
- •Смещение химического равновесия. Принцип Ле-Шателье
- •Учение о растворах Растворы
- •Физические свойства н2о и строение ее молекул
- •Механизм образования растворов
- •Растворимость веществ. Факторы, влияющие на растворимость
- •Влияние природы веществ на растворимость
- •Влияние давления на растворимость веществ
- •Влияние температуры на растворимость веществ
- •Влияние электролитов на растворимость веществ
- •Взаимная растворимость жидкостей
- •Способы выражения состава растворов
- •Термодинамические аспекты процесса растворения. Идеальные растворы
- •Коллигативные свойства разбавленных растворов
- •Диффузия и осмос в растворах
- •Роль осмоса в биологических процессах
- •Давление насыщенного пара растворителя над раствором. Закон Рауля
- •Следствия из закона Рауля
- •1) Растворы кипят при более высокой температуре, чем чистый растворитель;
- •2) Растворы замерзают при более низкой температуре, чем чистый растворитель.
- •Применение методов криоскопии и эбуллиоскопии
- •Коллигативные свойства растворов электролитов. Изотонический коэффициент Вант-Гоффа
- •Электролитическая диссоциация Электролиты и неэлектролиты. Теория электролитической диссоциации
- •Общая характеристика электролитов
- •Слабые электролиты
- •Сильные электролиты
- •Диссоциация воды. Водородный показатель
- •Теория кислот и оснований. Буферные растворы Теория кислот и оснований
- •Буферные растворы Определение буферных систем и их классификация
- •Механизм действия буферных систем
- •Вычисление рН и рОн буферных систем. Уравнение Гендерсона-Гассельбаха
- •Буферная емкость
- •Буферные системы человеческого организма
- •Нарушения кислотно-оснóвного равновесия крови. Ацидоз. Алкалоз
- •Химическая кинетика и катализ Кинетика химических реакций
- •Понятие о скорости химической реакции. Закон действующих масс
- •Кинетическая классификация химических реакций. Понятие о молекулярности и порядке химической реакции Порядок и молекулярность простых химических реакций
- •Понятие о сложных химических реакциях
- •Классификация сложных реакций
- •Измерение скорости химической реакции
- •Влияние температуры на скорость химической реакции
- •Катализ Общие положения и закономерности катализа
- •Механизм гомогенного и гетерогенного катализа
- •Особенности каталитической активности ферментов
- •2. Другим важным отличием ферментов от катализаторов небелковой природы является их высокая специфичность, т.Е. Избирательность действия.
- •Физическая химия дисперсных систем Определение дисперсных систем
- •Классификация дисперсных систем и их общая характеристика
- •Классификация дисперсных систем по агрегатному состоянию вещества дисперсной фазы и дисперсионной среды
- •Классификация по взаимодействию между частицами дисперсной фазы или степени структурированности системы
- •Классификация по характеру взаимодействия дисперсной фазы с дисперсионной средой
- •Методы получения дисперсных систем
- •Диспергирование жидкостей
- •Диспергирование газов
- •Конденсационные методы
- •Методы физической конденсации
- •Методы химической конденсации
- •Очистка золей
- •Компенсационный диализ и вивидиализ
- •Молекулярно-кинетические свойства золей
- •Броуновское движение
- •Диффузия
- •Седиментация в золях
- •Осмотическое давление в золях
- •Оптические свойства золей
- •Рассеяние света (опалесценция)
- •Оптические методы исследования коллоидных систем Ультрамикроскоп
- •Механизм образования и строение коллоидной частицы – мицеллы
- •1. Получение золя берлинской лазури:
- •2. Получение с помощью гидролиза FeCl3 золя гидроксида железа (III).
- •3. Получение золя As2s3:
- •Электрокинетические свойства золей
- •Устойчивость гидрофобных коллоидных систем. Коагуляция золей Виды устойчивости золей
- •Теория коагуляции Дерягина-Ландау-Фервея-Овербека
- •Влияние электролитов на устойчивость золей. Порог коагуляции. Правило Шульца-Гарди
- •Чередование зон коагуляции
- •Коагуляции золей смесями электролитов
- •Скорость коагуляции
- •Коллоидная защита
- •Роль процессов коагуляции в промышленности, медицине, биологии
- •Растворы высокомолекулярных соединений
- •1) Своеобразное тепловое движение частиц растворенного вещества, схожее с броуновским движением мицелл в золях;
- •Общая характеристика высокомолекулярных соединений
- •Классификация полимеров
- •Набухание и растворение вмс
- •Термодинамические аспекты процесса набухания
- •Давление набухания
- •Свойства растворов высокомолекулярных соединений
- •Осмотическое давление растворов вмс
- •Онкотическое давление крови
- •Вязкость растворов полимеров
- •Свободная и связанная вода в растворах
- •Полиэлектролиты
- •Факторы, влияющие на устойчивость растворов полимеров. Высаливание
- •Электрохимия растворы электролитов как проводники второго рода. Электропроводность растворов электролитов
- •Эквивалентная электропроводность растворов
- •Практическое применение электропроводности
- •Равновесные электродные процессы
- •Металлический электрод
- •Измерение электродных потенциалов
- •Окислительно-восстановительные электроды
- •1. Переход окисленной формы в восстановленную и наоборот заключается только в обмене между ними электронами:
- •Диффузионный и мембранный потенциалы
- •Химические источники электрического тока. Гальванические элементы
- •Потенциометрия
- •Содержание
Влияние температуры на скорость химической реакции
Скорость химических реакций зависит от многих факторов, главными из которых являются концентрация и природа исходных веществ, температура реакционной системы и присутствие в ней катализатора.
Кроме того, скорость гетерогенных реакций зависит еще и от величины поверхности раздела фаз(чем ее площадь больше, тем скорость реакции выше). Если в реакции участвуют твердые вещества, то можно сравнительно легко увеличить площадь поверхности раздела за счет их измельчения (диспергирования).
Влияние концентрации исходных веществ на скорость химической реакции математически описывается с помощью её основного кинетического уравнения. Для образования продуктов реакции необходимо, в первую очередь, чтобы молекулы исходных веществ столкнулись между собой. Чем больше таких соударений (или единичных актов реакции) происходит в единицу времени, тем скорость реакции будет выше. Частота столкновений между молекулами реагентов напрямую зависит от их числа в единице объема реакционной системы, т.е. от концентрации.
Кроме концентрации реагирующих веществ, важнейшим фактором, влияющим на скорость реакции, является температура реакционной смеси.Причем для большинства химических реакций наблюдается возрастание их скорости с повышением температуры (рис. 41а). Такой тип температурной зависимости скорости реакции называетсянормальным. Он характерен для всех простых реакций. Более сложная зависимость от температуры наблюдается для ферментативных реакций, протекающихinvivoилиinvitro(рис. 41б). Более подробно о ее причине будет сказано нами позже.
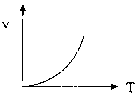
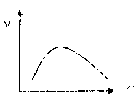
а б
Рис. 41. Зависимость скорости различных типов реакций от температуры: а – нормальная, б – для ферментативных реакций
Увеличение скорости химической реакции с ростом температуры, на первый взгляд, можно объяснить возрастанием скорости теплового движения молекул исходных веществ. Это должно приводить к увеличению числа соударений между ними, несмотря на то, что общее количество молекул осталось неизменным.
Однако, как показали расчёты, число соударений между частицами, находящимися в газовых и жидких средах за единицу времени, всегда достаточно велико. Так, в 1 см3газа (при н.у.) за одну секунду происходит ~ 1 · 1028столкновений между молекулами. Если бы каждое из них приводило к образованию конечных продуктов, то подавляющее большинство химических реакций протекали бы практически мгновенно, т.е. со взрывом.
На практике этого не наблюдается, т.к. не все соударения между молекулами исходных веществ являются «успешными». Установлено, что для многих реакций число таких «успешных» соударений ~ в 1015–1020раз меньше, чем общее число соударений.
Протекание реакции становится возможным только в том случае, если столкнувшиеся молекулы обладают достаточным запасом внутренней энергии. Если её значение равно какой-то определённой величине или больше её, то реакция осуществится (в противном случае – нет). Такие молекулы называются активными, а соударения между ними –эффективными.
Обычно доля активных молекул реагентов, по сравнению с их общим числом, для большинства реакций невелика.
При повышении температуры увеличивается запас внутренней энергии молекул. Всё большее их число становятся активными. Как следствие этого, возрастает доля эффективных соударений между молекулами за единицу времени, а значит и скорость химической реакции.
При повышении температуры концентрации исходных веществ в реакционной смеси практически не изменяются. Значит, увеличение скорости реакции в соответствии с главным кинетическим уравнением должно быть связано с возрастанием её константы скорости.
Голландский учёный Вант-Гофф опытным путём определил, что для химических реакций (имеющих нормальный тип зависимости скорости от температуры) при повышении температуры на каждые 10 градусов величина константы скорости возрастает в 2-4 раза.Причём для каждой химической реакции это число является постоянным и может принимать из указанного интервала как целочисленные (2, 3, 4) значения, так и дробные. Оно определяется экспериментально, называетсятемпературным коэффициентом скорости химической реакции или коэффициентом Вант-Гоффа и обозначается греческой буквой γ:
γ =
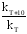
где kТ – константа скорости химической реакции при температуре, равной Т; kT+10 – константа скорости химической реакции при температуре, повышенной, по сравнению с исходной, на 10 градусов.
Согласно правилу Вант-Гоффа, температурный коэффициент γ для химической реакции должен оставаться постоянным в любом температурном диапазоне. Однако в действительности для многих реакций при высоких температурах наблюдается постепенное уменьшение его значения с ростом Т (рис. 42), вплоть до единицы. Поэтому правило Вант-Гоффа справедливо лишь в сравнительно узком интервале температур: от 0°С до 300°С.
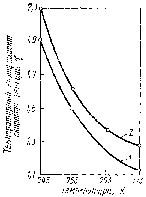
Рис. 42. Зависимость температурного коэффициента скорости реакции от температуры для реакции образования (1) и разложения (2) HI(I2+H22HI)
Более точная зависимость константы скорости химической реакции от температуры была найдена Аррениусом:
k=A·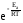
где А – предэкспоненциальный множитель; Еа – энергия активации химической реакции.
Множитель А отражает долю эффективных соударений между молекулами исходных веществ в общем их числе.
Очевидно, что его значения должны находиться в интервале от 0 до 1. При А = 1 все соударения оказываются эффективными. При А = 0 химическая реакция не протекает, несмотря на столкновение между молекулами реагентов.
Истинное значение множителя А для реакции обычно значительно меньше единицы, поскольку не всякое соударение молекул (даже обладающих энергией, равной или большей, чем Еа) обязательно приведёт к образованию продуктов. Столкнувшиеся активные молекулы могут не прореагировать по той причине, что не были должным образом сориентированы в пространстве друг относительно друга. Особенно сильно данный стерический фактор проявляется в превращениях биомолекул, где изменению (трансформации) подвергается лишь сравнительно небольшой их участок.
Соударение может быть неэффективным и из-за того, что перераспределение энергии внутри столкнувшихся молекул осуществляется без их химического изменения, т.е. без разрушения химических связей внутри них.
Энергию активации химической реакции (Еа) по физическому смыслу можно определить как тот избыток энергии, по сравнению со средней энергией неактивных молекул исходных веществ в реакционной системе при данной температуре, который им нужно сообщить, чтобы столкновения между ними привели к химической реакции.
Минимальный запас энергии, которым должны обладать молекулы для вступления в ту или иную реакцию, можно рассматривать как своеобразный энергетический барьер этой реакции.
Причём, чем он выше, тем меньшее число молекул способно его преодолеть. Зная общее число молекул в системе и величину энергии активации для данной реакции, количество таких активных молекул можно рассчитать по закону Максвелла-Больцмана
Na=No
∙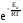
где Na – число активных молекул, No – общее число молекул.
При протекании химической реакции число активных молекул вследствие их расходования уменьшается. Но при этом в результате столкновений между неактивными молекулами исходных веществ происходит перераспределение энергии, в результате чего доля активных молекул Na/No непрерывно восстанавливается и реакция не прекращается.
Величина энергии активации зависит от типа и прочности связей между атомами в молекулах исходных веществ и от характера взаимодействия, в которое они вступают. Таким образом, каждая химическая реакция характеризуется определённой величиной энергии активации. Её значение может быть меньше энергии разрыва связей в молекуле реагента, т.к. для того, чтобы молекула смогла провзаимодействовать, во многих случаях и не требуется полного разрыва связей, а достаточно лишь их ослабления.
Для большинства химических реакций величина Еаизменяется в пределах от 20 до 300 кДж/моль. Низкие значения энергии активации соответствуют высоким скоростям протекания реакции и наоборот.
Опытным путём было установлено, что если величина Еа< 40 кДж/моль, то реакция протекает мгновенно; если величина Еаизменяется в пределах 40-120 кДж/моль, реакция идёт с измеримой скоростью; при Еа>120 кДж/моль скорость реакции становится очень малой.
Влияние величины энергии активации на скорость химической реакции рассматривается в рамках теории переходного состояния или активированного комплекса.
Она основана на предположении, что в ходе взаимодействия начальная конфигурация частиц реагентов переходит в конечную в результате непрерывного изменения межатомных расстояний.
Продукты реакции могут получиться лишь при условии образования промежуточной конфигурации, называемой активированным комплексом. Эта конфигурация состоит из атомов реагентов, но в ней старые связи еще не целиком разрушились, а новые не успели полностью образоваться.
Покажем схематически механизм данного процесса на примере бимолекулярной реакции, протекающей между двухатомными молекулами по схеме:
АВ + CD→AC+BD
В результате столкновения молекул реагентов связи между атомами в них значительно ослабляются, и происходит образование промежуточного неустойчивого соединения, состоящего из четырех атомов, которое затем распадается с образованием двух новых молекул.
A−BA∙∙∙∙BAB
+ → ::→ | + |
C–DC∙∙∙∙DCD
Активированный
комплекс
На образование активированного комплекса необходимо затратить энергию. Величина ее и равняется энергии активации. Конфигурация активированного комплекса и его свойства для большинства химических реакций неизвестны. Несмотря на это, с помощью приближенных квантовомеханических расчетов можно получить качественные результаты, помогающие понять закономерности протекания многих химических явлений.
На рис. 43 представлены
энергетические диаграммы эндотермической
(а) и экзотермической (б) реакций,
поясняющие вышесказанные представления.
Здесь по горизонтали отложен ход
процесса, а по вертикали – энергия
рассматриваемой совокупности веществ;
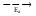 и
и – энергии активации, соответственно,
прямой и обратной реакций. Из рис. 43
следует, что тепловой эффект химической
реакции определяется не только
энергетическим состоянием исходных и
конечных веществ, но и разностью энергий
активации прямой и обратной реакций.
– энергии активации, соответственно,
прямой и обратной реакций. Из рис. 43
следует, что тепловой эффект химической
реакции определяется не только
энергетическим состоянием исходных и
конечных веществ, но и разностью энергий
активации прямой и обратной реакций.
Кроме того, независимо от направления процесса при переходе из начального состояния в конечное система должна преодолеть энергетический барьер, равный энергии активации.
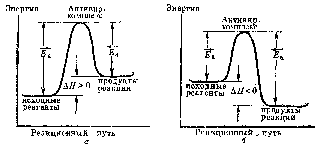
Рис. 43. Изменение энергии реагирующей системы (схема): а – эндотермическая реакция, б – экзотермическая реакция
Энергию активации химической реакции можно определить экспериментально на основании уравнения Аррениуса для константы скорости, записанного в логарифмической форме:
lgk= -∙ +lgA
+lgA
Оно представляет
собой уравнение прямой в координатах
lgkи 1/Т
(рис. 44). Для ее построения необходимо
опытным путем определить несколько
значенийkпри разных
температурах Т. Тангенс угла наклона
прямой равен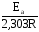 и дает возможность найти величину Еа.
и дает возможность найти величину Еа.

Рис. 44. Графическое определение энергии активации
Величину Еаможно рассчитать и теоретически, зная значения констант скоростей химической реакцииk1иk2при двух разных температурах Т1и Т2, с помощью уравнения
lg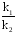 = -
= - ∙
(
∙
(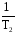 –
– )
)
Оно получено из уравнений Аррениуса для константы скорости химической реакции (в логарифмической форме), записанных для двух разных температур Т1и Т2, путем их вычитания.
Как уже было показано ранее (рис. 41б), влияние температуры на скорость биохимических реакций носит более сложный характер. Сперва, с повышением температуры, их скорость увеличивается, но до определенного температурного предела (~315 К), при превышении которого происходит резкое уменьшение скорости.
Как правило, многие биохимические процессы протекают с участием ферментов, имеющих белковую природу. Если проследить зависимость активности любого фермента от температуры (рис. 45), то можно заметить аналогичную закономерность, как и со скоростью биохимической реакции. Наибольшей активностью ферменты обладают при температуре 312-315К. Дальнейшее повышение температуры приводит к резкому снижению их активности. Очевидно, это связано с процессом денатурации белковых молекул, протекающим при Т > 315К. При этом происходит нарушение третичной и четвертичной (для сложных белков) структур, вследствие чего ферменты теряют свою активность, и скорость биохимических процессов замедляется. Наиболее оптимальные условия в организме человека для протекания биохимических процессов лежат в достаточно узком температурном интервале 308-311К. При этих условиях большинство ферментов обладают высокой активностью, а вероятность протекания процессов денатурации их молекул мала.
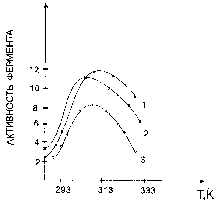
Рис. 45. Активность фермента трипсина в различных организмах от температуры: 1 – собака, 2 – окунь, 3 – треска
В животном мире наблюдаются отступления от этого правила. Так, температура тела некоторых певчих птиц равна 318K. В горячих источниках острова Цейлон при температуре 323Kживут и размножаются некоторые виды рыб. Самые жизнестойкие организмы можно найти в мире бактерий. Некоторые из них способны вести нормальную жизнь даже при температуре выше 373K(100оС).
