
- •Міністерство освіти і науки україни
- •1. Техніка безпеки і перша допомога в хімічній лабораторії
- •Запам'ятайте!
- •2. Оптичні методи аналізу
- •2.1. Абсорбційна фотометрія
- •Правила проведення фотометрії та розрахунок результатів досліджень
- •Лабораторна робота № 1 Фотоколориметричний аналіз
- •Правила роботи з колориметром фэк – 56м
- •Методика виконання роботи
- •Результати визначення концентрацій барвника за калібрувальним графіком та стандартним розчином
- •Питання та вправи для самоконтролю
- •Лабораторна робота № 2 Фотоколориметричний аналіз суміші барвників
- •Методика виконання роботи
- •Залежність оптичної густини стандартних розчинів барвників від довжини хвилі
- •Оптична густина стандартних розчинів барвників а і в
- •Оптична густина суміші барвників а і в
- •Результати сумісного визначення барвників
- •Питання та вправи для самоконтролю
- •2.2. Нефелометрія і турбідиметрія
- •Лабораторна робота № 3 Нефелометричний аналіз
- •Готування розчинів
- •Виконання роботи
- •Робота з фотометром лмф-72
- •Результати визначення йонів so42–
- •Питання та вправи для самоконтролю
- •2.3. Емісійна фотометрія Люмінесцентні методи аналізу
- •Лабораторна робота № 4 Люмінесцентний метод визначення замаслювачів у тканинах
- •Методика виконання роботи
- •Готування стандартної шкали
- •Приклад розрахунку
- •Питання та вправи для самоконтролю
- •2.4. Поляриметричний метод аналізу
- •Вміст вуглеводів в плодах
- •Вміст вуглеводів в овочах і баштанних
- •Лабораторна робота № 5 Визначення вуглеводів поляриметричним методом
- •Хід визначення
- •Результати поляриметричних вимірювань
- •Питання та вправи для самоконтролю
- •2.5. Рефрактометричний метод аналізу
- •Лабораторна робота № 6 Рефрактометричний метод визначення вуглеводів
- •Рефрактометр ирф–22
- •Результати рефрактометричних вимірювань
- •Питання та вправи для самоконтролю
- •3. Електрохімічні методи аналізу
- •3.1. Кондуктометрія
- •3) Кондуктометричне титрування суміші сильної та слабкої кислот.
- •Лабораторна робота 7 Кондуктометричний аналіз
- •Методика виконання роботи
- •Дані кондуктометричного кислотно-основного титрування сильної кислоти
- •Дані кондуктометричного кислотно-основного титрування
- •Дані кондуктометричного кислотно-основного титрування
- •Дані кондуктометричного кислотно-основного титрування
- •Дані кондуктометричного кислотно-основного титрування
- •Дані кондуктометричного кислотно-основного титрування
- •Результати кондуктометричного кислотно-основного титрування
- •Питання та вправи для самоконтролю
- •3.2. Потенціометричні методи аналізу
- •Лабораторна робота № 8 Потенціометричне титрування кислот
- •Робота з приладом
- •Методика виконання роботи
- •Дані потенціометричного титрування хлоридної кислоти лугом
- •Дані потенціометричного титрування хлоридної кислоти лугом
- •Дані потенціометричного титрування оцтової кислоти лугом
- •Дані потенціометричного титрування оцтової кислоти лугом
- •Дані потенціометричного титрування ________________кислоти лугом (контрольна задача)
- •Дані потенціометричного титрування _____________кислоти лугом
- •Результати потенціометричного кислотно-основного титрування
- •Питання та вправи для самоконтролю
- •Лабораторна робота №9 Потенціометричне визначення концентрації йонів натрію у водяних розчинах
- •Методика виконання роботи
- •Питання та вправи для самоконтролю
- •3.3. Кулонометричне титрування
- •Основні електрохімічні процеси:
- •Лабораторна работа № 10 Кулонометричне визначення відновників. Визначення в розчині кількості тіосульфату натрію
- •Результати кулонометричного титрування натрій тіосульфату
- •Питання та вправи для самоконтролю
- •4. Радіометричний метод аналізу
- •Лабораторна робота № 11 Визначення калій хлориду у суміші хлоридів. Роздільне визначення b– і g–випромінювань
- •Методика виконання роботи
- •Результати радіометричного визначення калій хлориду у суміші з натрій хлоридом
- •Питання та вправи для самоконтролю
- •Відповіді до розрахункових задач
- •73008, М. Херсон, Бериславське шосе, 24
3.2. Потенціометричні методи аналізу
Потенціометричний метод заснований на залежності потенціалу індикаторного електроду від концентрації йонів, що визначаються.
Потенціал
розраховується за формулою Нернста:
![]() ,
де
,
де![]() -
електродний потенціал в умовах досліду,
В;
-
електродний потенціал в умовах досліду,
В;
![]() -
стандартний електродний потенціал, В;
R -
універсальна газова стала, Дж/(моль·К);
F -
стала Фарадея Кл/моль; Т -
абсолютна температура, К; z -
число електронів, що беруть участь у
елементарному акті електрохімічної
реакції;
-
стандартний електродний потенціал, В;
R -
універсальна газова стала, Дж/(моль·К);
F -
стала Фарадея Кл/моль; Т -
абсолютна температура, К; z -
число електронів, що беруть участь у
елементарному акті електрохімічної
реакції;
![]() -
активність.
-
активність.
Існують методи визначення аніонів, катіонів і активних нейтральних молекул. При цьому використовуються різноманітні типи електродів.
Електрод,
який чутливий до даного виду йонів, чи
речовини називається індикаторним. Він
завжди використовується в парі з
електродом порівняння (каломельним або
хлоридсрібним). Можливо безпосереднє
визначення концентрації електрохімічно-активної
речовини по електродному потенціалу.
Для цього будують калібрувальний графік
залежності
![]() відlgс,
що частіше усього має лінійний характер.
За допомогою графіка по визначеному
значенню
відlgс,
що частіше усього має лінійний характер.
За допомогою графіка по визначеному
значенню
![]() знаходять концентрацію невідомого
розчину.
знаходять концентрацію невідомого
розчину.
 Інший
спосіб- потенціометричне
титрування: відновлена форма (титрат)
титрується окислювачем - титрантом.
У цьому випадку, наприклад, в ацидометрії,
криві потенціометричного титрування
мають вигляд, приведений на рис.20. Точка
еквівалентності буде знаходитися в
тому місці кривої, де є максимум, тобто
в області найбільшої швидкості зміни
функції. Якщо хвиля на графіку полога,
то більшу точність має диференціальний
графік (рис. 21). Для його побудови
використовується графічне диференціювання.
Особливе місце серед потенціометричних
методів займають методи, які засновані
на вимірюванні рН. Для цього використовують
рН-метри
та йономіри.
Інший
спосіб- потенціометричне
титрування: відновлена форма (титрат)
титрується окислювачем - титрантом.
У цьому випадку, наприклад, в ацидометрії,
криві потенціометричного титрування
мають вигляд, приведений на рис.20. Точка
еквівалентності буде знаходитися в
тому місці кривої, де є максимум, тобто
в області найбільшої швидкості зміни
функції. Якщо хвиля на графіку полога,
то більшу точність має диференціальний
графік (рис. 21). Для його побудови
використовується графічне диференціювання.
Особливе місце серед потенціометричних
методів займають методи, які засновані
на вимірюванні рН. Для цього використовують
рН-метри
та йономіри.
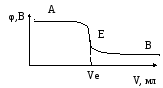
Рис. 20. Інтегральний графік Рис. 21. Диференціальний графік
потенціометричного титрування потенціометричного титрування.
Лабораторна робота № 8 Потенціометричне титрування кислот
Мета роботи: визначити кількість кислоти в розчині потенціометричним титруванням.
Прилади та реактиви: рН–метр мілівольтметр типу ЛПУ – 01; розчин з молярною концентрацією еквівалентів хлоридної кислоти (HCl) 0,01 моль/л, розчин з молярною концентрацією еквівалентів оцтової кислоти (CH3COOH) 0,01 моль/л, розчин з молярною концентрацією еквівалентів натрій гідроксиду (NaOH) 0,05 моль/л, бюретки.
Робота з приладом
рН–метр мілівольтметр типу ЛПУ – 01 призначений для вимірів концентрацій йонів Гідрогену (Н+). Діапазон вимірювання рН від "0" до"14". Границі температурної компенсації приладу від 0 до 1000С. Прилад складається з перетворювача і системи електродів. На передній панелі перетворювача розташовані органи оперативного управління і пристрій, що показує. Електродна система, яка складається з вимірювального (скляного) та допоміжного хлоридсрібного електродів, занурена у розчин (рис. 22).
Виміри виконують таким чином:
1. Вмикають прилад у мережу і прогрівають протягом 15 хвилин (тумблер "Включено").
2. Перемикач "Виды работ" – у положення "рН".
3. Перемикач "Пределы измерений" – у положення "–2 – 14".
4. Перемикачем "Температура раствора" встановлюють кімнатну температуру.
5. Виконують калібрування приладу за допомогою стандартних буферних розчинів.
5.1. Електродну систему занурюють у стандартний буферний розчин 1,68 рН. Перемикач "Пределы измерений" встановлюють у положення "–2–2". По верхній шкалі приладу реєструють показання. Якщо на приладі не встановлюється показання 1,68, то перемикачем "Настройка по буф. раствору" встановлюють це значення.
5.2. Промивають електродну систему дистильованою водою.
5.3. Занурюють електроди в наступний стандартний буферний розчин 9,18 рН. Перемикач "Пределы измерений" встановлюють у положення "6–10" і обертанням перемикача "Крутизна" домагаються положення стрілки приладу на рН 9,18.
5.4. Промивають електродну систему дистильованою водою.
5.5. Цю процедуру (пп. 5.1–5.4) повторюють, поки на приладі самовільно не встановляться певні значення рН.
6. Занурюють електроди в досліджуваний розчин. Встановлюють межу вимірювань "–2–14". По нижній шкалі приладу визначають приблизне значення рН. Потім вибирають межу вимірювань відповідно до попередньо отриманого значення рН і реєструють точне значення рН розчину по верхній шкалі.


14 15 13 10 12 9 11 5 8 2 4 3 6 7 1
Рис. 22. рН–метр мілівольтметр типу ЛПУ – 01
1 – тумблер "Включено"; 2 – перемикач "Виды работ"; 3 – перемикач "Температура раствора"; 4 – перемикач "Пределы измерений"; 5 – регулятор "Настройка по буф. раствору"; 6 – регулятор "Крутизна"; 7 – шкала приладу; 8 – світловий індикатор; 9 – "Датчик" – місце підключення скляного електроду (10); 11 – місце підключення хлоридсрібного електроду (12); 13 – термометр; 14 – штатив з рухомим столиком (15) для ємності з досліджуваним розчином.
