
- •Міністерство освіти і науки україни
- •1. Техніка безпеки і перша допомога в хімічній лабораторії
- •Запам'ятайте!
- •2. Оптичні методи аналізу
- •2.1. Абсорбційна фотометрія
- •Правила проведення фотометрії та розрахунок результатів досліджень
- •Лабораторна робота № 1 Фотоколориметричний аналіз
- •Правила роботи з колориметром фэк – 56м
- •Методика виконання роботи
- •Результати визначення концентрацій барвника за калібрувальним графіком та стандартним розчином
- •Питання та вправи для самоконтролю
- •Лабораторна робота № 2 Фотоколориметричний аналіз суміші барвників
- •Методика виконання роботи
- •Залежність оптичної густини стандартних розчинів барвників від довжини хвилі
- •Оптична густина стандартних розчинів барвників а і в
- •Оптична густина суміші барвників а і в
- •Результати сумісного визначення барвників
- •Питання та вправи для самоконтролю
- •2.2. Нефелометрія і турбідиметрія
- •Лабораторна робота № 3 Нефелометричний аналіз
- •Готування розчинів
- •Виконання роботи
- •Робота з фотометром лмф-72
- •Результати визначення йонів so42–
- •Питання та вправи для самоконтролю
- •2.3. Емісійна фотометрія Люмінесцентні методи аналізу
- •Лабораторна робота № 4 Люмінесцентний метод визначення замаслювачів у тканинах
- •Методика виконання роботи
- •Готування стандартної шкали
- •Приклад розрахунку
- •Питання та вправи для самоконтролю
- •2.4. Поляриметричний метод аналізу
- •Вміст вуглеводів в плодах
- •Вміст вуглеводів в овочах і баштанних
- •Лабораторна робота № 5 Визначення вуглеводів поляриметричним методом
- •Хід визначення
- •Результати поляриметричних вимірювань
- •Питання та вправи для самоконтролю
- •2.5. Рефрактометричний метод аналізу
- •Лабораторна робота № 6 Рефрактометричний метод визначення вуглеводів
- •Рефрактометр ирф–22
- •Результати рефрактометричних вимірювань
- •Питання та вправи для самоконтролю
- •3. Електрохімічні методи аналізу
- •3.1. Кондуктометрія
- •3) Кондуктометричне титрування суміші сильної та слабкої кислот.
- •Лабораторна робота 7 Кондуктометричний аналіз
- •Методика виконання роботи
- •Дані кондуктометричного кислотно-основного титрування сильної кислоти
- •Дані кондуктометричного кислотно-основного титрування
- •Дані кондуктометричного кислотно-основного титрування
- •Дані кондуктометричного кислотно-основного титрування
- •Дані кондуктометричного кислотно-основного титрування
- •Дані кондуктометричного кислотно-основного титрування
- •Результати кондуктометричного кислотно-основного титрування
- •Питання та вправи для самоконтролю
- •3.2. Потенціометричні методи аналізу
- •Лабораторна робота № 8 Потенціометричне титрування кислот
- •Робота з приладом
- •Методика виконання роботи
- •Дані потенціометричного титрування хлоридної кислоти лугом
- •Дані потенціометричного титрування хлоридної кислоти лугом
- •Дані потенціометричного титрування оцтової кислоти лугом
- •Дані потенціометричного титрування оцтової кислоти лугом
- •Дані потенціометричного титрування ________________кислоти лугом (контрольна задача)
- •Дані потенціометричного титрування _____________кислоти лугом
- •Результати потенціометричного кислотно-основного титрування
- •Питання та вправи для самоконтролю
- •Лабораторна робота №9 Потенціометричне визначення концентрації йонів натрію у водяних розчинах
- •Методика виконання роботи
- •Питання та вправи для самоконтролю
- •3.3. Кулонометричне титрування
- •Основні електрохімічні процеси:
- •Лабораторна работа № 10 Кулонометричне визначення відновників. Визначення в розчині кількості тіосульфату натрію
- •Результати кулонометричного титрування натрій тіосульфату
- •Питання та вправи для самоконтролю
- •4. Радіометричний метод аналізу
- •Лабораторна робота № 11 Визначення калій хлориду у суміші хлоридів. Роздільне визначення b– і g–випромінювань
- •Методика виконання роботи
- •Результати радіометричного визначення калій хлориду у суміші з натрій хлоридом
- •Питання та вправи для самоконтролю
- •Відповіді до розрахункових задач
- •73008, М. Херсон, Бериславське шосе, 24
Результати визначення йонів so42–
|
№ з/п |
Кількість йонів SO42–, мг |
Похибка, % | ||
|
Взято |
Знайдено | |||
|
Випробування методики | ||||
|
1 |
|
|
| |
|
2 |
|
|
| |
|
3 |
|
|
| |
|
Контрольні задачі | ||||
|
1 |
|
|
| |
|
2 |
|
|
| |
За результатами роботи зробити висновок. _______________________________
________________________________________________________________________________________________________________________
Питання та вправи для самоконтролю
1. Наведіть основний закон світлорозсіяння (рівняння Релея) і охарактеризуйте величини, які входять до нього.
2. Які умови треба дотримувати для забезпечення достатньої точності нефелометричних вимірювань?
3. Як пов’язана інтенсивність світла, яке пройшло через суспензію, з концентрацією речовини, що аналізується, в турбідиметричному методі?
4. Назвіть переваги та недоліки методів нефелометрії та турбідиметрії?
5. Чим відрізняються між собою нефелометрія і турбідиметрія.
6. Які прилади використовують при нефелометричних вимірюваннях? Наведіть оптичну схему нефелометра.
7. При визначенні натрій хлориду у розчині натрій гідроксиду приготували серію стандартних розчинів. Для цього V мл розчину NaCl (T = 0,100 мг/мл) перенесли у мірні колби місткістю 25,0 мл, додали реактиви, які необхідні для одержання суспензії AgCl, виміряли удавані оптичні густини за допомогою нефелометра і одержали значення: V, мл 0,30 0,50 0,80 1,50
Dудавана 0,670 0,550 0,390 1,150.
Наважку розчину, що аналізується, масою 21,74 г нейтралізували нітратною кислотою, перенесли у мірну колбу і приготували 50,0 мл розчину, 2,0 мл якого використали для приготування 25,0 мл суспензії AgCl. Визначити масову частку NaCl, якщо удавана оптична густина суспензії AgCl має значення 0,480.
2.3. Емісійна фотометрія Люмінесцентні методи аналізу
Емісійна фотометрія базується на вимірі енергії, що випромінюється речовиною внаслідок енергетично збудженого стана. До методів емісійної фотометрії відносять люмінесценцією, яка заснована на ефекті енергетичного збудження молекул і атомів досліджуваної речовини, як наслідок впливу жорсткого ультрафіолетового випромінювання, і полум'яну фотометрію, яка заснована на ефекті енергетичного збудження полум'ям структурних складових досліджуваної речовини.
Люмінесцентні методи аналізу засновані на спроможності деяких речовин виділяти променисту енергію під впливом електромагнітного випромінювання з більш короткою довжиною хвилі. Це явище називається фотолюмінесценцією. Якщо розташувати по лінії хвиль спектральну характеристику збудливої системи і смугу люмінесценції, то одержимо графік, зображений на рис.11.
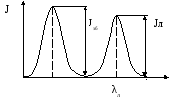
Р
λзб λ,
нм
g - квантовий
вихід люмінесценції: g = ![]() .
Чим більшеg,
тим інтенсивніше люмінесценція. Як
правило g
< 1. Проста модифікація кількісного
люмінесцентного аналізу -
метод стандартних серій.
.
Чим більшеg,
тим інтенсивніше люмінесценція. Як
правило g
< 1. Проста модифікація кількісного
люмінесцентного аналізу -
метод стандартних серій.
Флуориметрія
заснована на вимірі інтенсивності
флуоресценції речовин. Інтенсивність
флуоресценції залежить від концентрації
речовини. Звичайно для флуориметричних
вимірів застосовують концентрації
речовин 10–4-10–6 г/мл;
в цих межах залежність інтенсивності
від концентрації прямолінійна. Кількісні
виміри у флуориметрії засновані на
використанні стандартних розчинів
речовин (спосіб порівняння або
калібрувального графіку). Якщо в якості
розчину порівняння застосовується
стандартний розчин речовини, то
концентрацію досліджуваного розчину
(Сх)
розраховують за формулою:
![]() ,
де
,
де![]() ,
,![]() ,
,![]() –відповідно
показання флуориметру для досліджуваного
розчину, стандартного розчину, контрольного
розчину;
–відповідно
показання флуориметру для досліджуваного
розчину, стандартного розчину, контрольного
розчину;![]() – концентрація
стандартного розчину.
– концентрація
стандартного розчину.
