
- •Государственное бюджетное образовательное учреждение высшего профессионального образования
- •Содержание
- •Список сокращений
- •Введение
- •І. Тема: белки
- •1. Строение и биологическая роль аминокислот, пептидов, белков
- •Аспарагиновая кислота (асп)
- •Лизин (лиз)
- •Серин (сер)
- •1.1. Первичная структура белка
- •1.2. Варианты вторичной структуры белка
- •1.3. Третичная структура белка
- •1.4. Четвертичная структура белка – высший уровень организации
- •Свойства протеинов
- •2.1. Физико - химические свойства биополимеров
- •2.2. Особенности биологических свойств белков
- •3. Методы очистки и выделения белков
- •4. Классификация белков
- •4.1. Простые белки
- •4.1.1. Глобулярные белки
- •4.1. 2. Фибриллярные белки
- •4.2. Сложные белки
- •Отличительные особенности строения углеводсодержащих белков
- •Характеристика липопротеиновых частиц
- •5. Биологическая роль протеинов
- •Вопросы для самоконтроля
- •Тестовые задания для оценки уровня знаний
- •Ситуационные задачи
- •II. Тема: ферменты
- •1. Особенности строения ферментов
- •1.1. Энзим – сложный белок
- •1.1.1. Природа и роль кофермента
- •Витамины – компоненты коферментов
- •1.1.2. Апофермент и его значение
- •1.2. Функциональные центры фермента
- •2. Энзимы как биокатализаторы
- •2.1. Теории, объясняющие механизм действия ферментов
- •I стадия. Образование es-комплекса
- •II стадия. Активация es-комплекса
- •III стадия. Образование eр-комплекса
- •IV стадия. Распад eр-комплекса
- •2.2. Специфичность действия энзимов
- •2.3. Кинетика ферментативных реакций
- •2.3.1. Зависимость скорости реакции от содержания субстрата
- •2.3.2. Влияние концентрации фермента на скорость реакции
- •2.3.3. Эффект колебаний температуры
- •2.3.4. Связь интенсивности процесса с величинами рН среды
- •3. Классификация, номенклатура ферментов
- •3.1. Классификация
- •2.1.1. Характеристика отдельных классов ферментов
- •4. Положительная и отрицательная регуляции работы ферментов
- •4.1. Механизмы аллостерической регуляции
- •4.2. Последствия белок - белкового взаимодействия
- •4.3. Регуляция путём ковалентной модификации
- •4.4. Частичный протеолиз как способ активации зимогена
- •Особенности конкурентного ингибирования
- •5. Использование ферментов в медицине
- •5.1. Энзимопатии
- •Энзимодиагностика
- •Энзимотерапия
- •Вопросы для самоконтроля
- •Тестовые задания для оценки уровня знаний:
- •Ситуационные задачи
- •Приложение № 1
- •Варианты правильных ответов на контрольные тесты
- •Список литературы
Вопросы для самоконтроля
1. Что такое фермент?
2. Чем он выгодно отличается от минеральных катализаторов?
3. Как построена молекула фермента?
4. Какую природу имеют коферменты? С какой целью используются в ферментативных реакциях?
5. Какова роль апофермента?
6. Как называются функциональные центры энзимов?
7. Как обычно строится название фермента? А если он относится к классу лигаз?
8. В чём сходство и отличия различных классов энзимов?
9. Что является главным условием успешной работы фермента?
10. Чем предпочтительней теория Кошланда?
11. Почему при повышении температуры организма даже на 1-30 резко меняется (как?) активность энзимов?
12. Как влияют колебания рН среды на активность ферментов?
13. Почему липазы и протеазы ЖКТ секретируются в виде зимогенов? Как происходит их активация?
14. Какой вид ингибирования наиболее распространён в живых клетках? Почему?
15. Что такое энзимопатии? Приведите примеры.
16. Как врачи-лаборанты могут использовать ферменты с целью диагностики?
17. Почему трипсин, который в физиологических условиях работает как протеаза в ЖКТ, можно применять при болезнях дыхательной системы?
Тестовые задания для оценки уровня знаний:
(Выберите один правильный вариант)
1. ПРИ НЕОГРАНИЧЕННОМ УВЕЛИЧЕНИИ КОНЦЕНТРАЦИИ СУБСТРАТА СКОРОСТЬ ФЕРМЕНТАТИВНОЙ РЕАКЦИИ ИЗМЕНЯЕТСЯ
1) сначала возрастает, затем сохраняется на достигнутом уровне
2) непрерывно возрастает
3) сначала снижается, затем возрастает
2. КЛАССИФИКАЦИЯ ФЕРМЕНТОВ ОСНОВАНА НА
1) кинетической характеристике
2) органной принадлежности
3) типе катализируемой реакции
3. ПЕПСИН ОБЛАДАЕТ СПЕЦИФИЧНОСТЬЮ
1) абсолютной
2) относительной
3) стереохимической
4. ФУНКЦИЕЙ АЛЛОСТЕРИЧЕСКОГО ЦЕНТРА ФЕРМЕНТА ЯВЛЯЕТСЯ
1) связывание регуляторов
2) связывание субстрата
3) связывание кофермента
5. ФУНКЦИЕЙ КАТАЛИТИЧЕСКОГО УЧАСТКА АКТИВНОГО ЦЕНТРА ФЕРМЕНТА ЯВЛЯЕТСЯ
1) связывание субстрата
2) временное связывание регулятора
3) преобразование субстрата
6. КАРДИОМИОЦИТЫ В НАИБОЛЬШЕМ КОЛИЧЕСТВЕ СОДЕРЖАТ ИЗОФЕРМЕНТ
1) ЛДГ-3
2) ЛДГ-1
3) ЛДГ-5
7. К МУЛЬТИЭНЗИМНЫМ КОМПЛЕКСАМ ОТНОСЯТ
1) -кетоглутаратдегидрогеназу
2) изоферменты ЛДГ
3) пируваткарбоксилазу
8. НЕСПЕЦИФИЧЕСКИЕ ИНГИБИТОРЫ СНИЖАЮТ АКТИВНОСТЬ ФЕРМЕНТА, ВЫЗЫВАЯ
1) связывание субстрата
2) связывание кофермента
3) изменение конформации фермента
9. КОФЕРМЕНТНАЯ ФОРМА ВИТАМИНА В2
1) ФМН
2) НАД+
3) ТДФ
10. АКТИВАЦИЯ ФЕРМЕНТОВ МОЖЕТ ОСУЩЕСТВЛЯТЬСЯ ПУТЁМ
1) удаления кофермента
2) ограниченного протеолиза
3) блокирования активного центра
11. КОФЕРМЕНТНАЯ ФОРМА ВИТАМИНА В3
1) пиридоксальфосфат
2) ретиналь
3) никотинамидадениндинуклеотид
12. ИЗОФЕРМЕНТЫ ОТЛИЧАЮТСЯ ДРУГ ОТ ДРУГА
1) числом субъединиц
2) тканевой локализацией
3) типом катализируемой реакции
Ситуационные задачи
Как может измениться активность энзима, если на контактную площадку активного центра ляжет аналог субстрата?
Назовите фермент, катализирующий следующую реакцию:
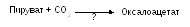
Объясните, почему протеолитические ферменты используются в медицине для очищения раневых поверхностей.
Дайте название ферменту, катализирующему данную реакцию. Укажите к какому классу он принадлежит.
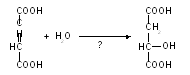
5. Почему операции на головном мозге проводят после предварительной гипотермии?
6. Почему сульфаниламидные препараты подавляют рост бактериальных клеток?
7. На чём основано действие нервно-паралитических ядов?
