
- •Государственное бюджетное образовательное учреждение высшего профессионального образования
- •Содержание
- •Список сокращений
- •Введение
- •І. Тема: белки
- •1. Строение и биологическая роль аминокислот, пептидов, белков
- •Аспарагиновая кислота (асп)
- •Лизин (лиз)
- •Серин (сер)
- •1.1. Первичная структура белка
- •1.2. Варианты вторичной структуры белка
- •1.3. Третичная структура белка
- •1.4. Четвертичная структура белка – высший уровень организации
- •Свойства протеинов
- •2.1. Физико - химические свойства биополимеров
- •2.2. Особенности биологических свойств белков
- •3. Методы очистки и выделения белков
- •4. Классификация белков
- •4.1. Простые белки
- •4.1.1. Глобулярные белки
- •4.1. 2. Фибриллярные белки
- •4.2. Сложные белки
- •Отличительные особенности строения углеводсодержащих белков
- •Характеристика липопротеиновых частиц
- •5. Биологическая роль протеинов
- •Вопросы для самоконтроля
- •Тестовые задания для оценки уровня знаний
- •Ситуационные задачи
- •II. Тема: ферменты
- •1. Особенности строения ферментов
- •1.1. Энзим – сложный белок
- •1.1.1. Природа и роль кофермента
- •Витамины – компоненты коферментов
- •1.1.2. Апофермент и его значение
- •1.2. Функциональные центры фермента
- •2. Энзимы как биокатализаторы
- •2.1. Теории, объясняющие механизм действия ферментов
- •I стадия. Образование es-комплекса
- •II стадия. Активация es-комплекса
- •III стадия. Образование eр-комплекса
- •IV стадия. Распад eр-комплекса
- •2.2. Специфичность действия энзимов
- •2.3. Кинетика ферментативных реакций
- •2.3.1. Зависимость скорости реакции от содержания субстрата
- •2.3.2. Влияние концентрации фермента на скорость реакции
- •2.3.3. Эффект колебаний температуры
- •2.3.4. Связь интенсивности процесса с величинами рН среды
- •3. Классификация, номенклатура ферментов
- •3.1. Классификация
- •2.1.1. Характеристика отдельных классов ферментов
- •4. Положительная и отрицательная регуляции работы ферментов
- •4.1. Механизмы аллостерической регуляции
- •4.2. Последствия белок - белкового взаимодействия
- •4.3. Регуляция путём ковалентной модификации
- •4.4. Частичный протеолиз как способ активации зимогена
- •Особенности конкурентного ингибирования
- •5. Использование ферментов в медицине
- •5.1. Энзимопатии
- •Энзимодиагностика
- •Энзимотерапия
- •Вопросы для самоконтроля
- •Тестовые задания для оценки уровня знаний:
- •Ситуационные задачи
- •Приложение № 1
- •Варианты правильных ответов на контрольные тесты
- •Список литературы
1.1. Энзим – сложный белок
В природе существуют как простые (реже), так в основном и сложные ферменты:
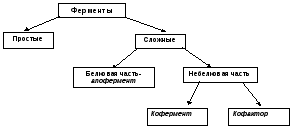
Первые представлены полипептидными цепями и при гидролизе распадаются исключительно на аминокислоты. Это в основном гидролитические ферменты, в частности пепсин, трипсин, липаза, уреаза, лизоцим, рибонуклеаза, фосфатаза и др.
Большинство энзимов относится к классу сложных, содержащих помимо полипептидного компонента (апофермента), какой-либо небелковый фрагмент (кофермент или кофактор), присутствие которого является абсолютно необходимым для каталитической активности. Он может иметь различную химическую природу и отличаться по прочности связи с апоферментом. Исходя из особенности строения, коферментами бывают органические соединения (активные формы витаминов РР, группы В), а кофактор – неорганические частицы (ионы металлов и другие электролиты).
Если апофермент связан прочной ковалентной связью с небелковым компонентом и этот комплекс не разделяется при выделении и очистке, то такой энзим получает название холофермент (холоэнзим), а кофермент – простетическая группа (например, ФАД, ФМН, биотин, липоевая кислота). Когда же между частями мицеллы связь непрочная (нековалентная) и они легко отделяются при диализе, то тогда небелковый фрагмент принято называеть коферментом (например, НАД+, НАД+Ф) или кофактором (ионы металлов: Mg2+, Мn2+, Са2+ и др.).
1.1.1. Природа и роль кофермента
Все коферменты термодинамически стабильные органические соединения, имеющие различное строение. Часто это вещества - производные витаминов (табл. 3)
Таблица 3
Витамины – компоненты коферментов
|
Витамин |
Название кофермента |
Роль |
|
Нуклеотидной природы | ||
|
Никотинамид (витамин РР, или В3) |
Никатинамидадениндинуклеотид (фосфат) (NAD+, NAD+F) |
Перенос протонов и электронов |
|
Рибофлавин, (витамин В2)
|
Флавинмононуклеотид, флавинадениндинуклеотид (FMN, FAD) |
Перенос протонов и электронов
|
|
Пантотеновая кислота (витамин В5) |
Коэнзим А (СоА) |
Перенос ацильных или ацетильных групп |
|
Фолиевая кислота (витамин ВС) |
Тетрагидрофолиевая кислота (ТHF) |
Перенос метильных, метиленовых, формильных групп или формиминогрупп (одноуглеродных остатков) |
|
Биотин (витамин Н) |
Биоцитин |
Перенос активной формы диоксида углерода |
|
Кобаламин (витамин В12)
|
Дезоксиаденозил- и (метил)-кобаламин (В12- коферменты) |
Меж- или внутримолекулярный перенос атомов |
|
Продукты реакций фосфорилирования с участием АТФ | ||
|
Тиамин (витамин В1) |
Тиаминдифосфат (TDP) |
Перенос карбонильных групп и некоторых молекул |
|
Пиридоксин (витамин В6)
|
Пиридоксамин-5-фосфат (фосфопиридоксаль, FP) |
Взаимоперенос амино- и карбоксильной групп |
Кроме того в качестве коэнзимов регистрируются соединения невитаминной природы: глутатион, АТФ, липоевая кислота, производные нуклеозидов (уридинфосфат, цитидинфосфат, фосфоаденозинфосфосульфат), вещества тетрапиррольной природы типа гема и др.
Более 25% всех ферментов для проявления полной каталитической активности нуждается в кофакторах (ионах металлов), механизм влияния которых на скорость реакций разнообразен.
Кофермент необходим для выполнения следующих задач:
Служит фрагментом активного центра холоэнзима, необходимого для связывания субстрата.
Принимает непосредственное участие в химической реакции.
