
- •Оглавление
- •СПИСОК СОКРАЩЕНИЙ
- •ПОДРОБНОЕ СОДЕРЖАНИЕ
- •ГЛАВА 02. ДЕМОГРАФИЧЕСКАЯ СИТУАЦИЯ В РОССИЙСКОЙ ФЕДЕРАЦИИ. ОБЩИЕ И ЧАСТНЫЕ АСПЕКТЫ
- •ГЛАВА 03.МАТЕРИНСКАЯ И ПЕРИНАТАЛЬНАЯ ЗАБОЛЕВАЕМОСТЬ И СМЕРТНОСТЬ. СТРАТЕГИЯ РИСКА В АКУШЕРСТВЕ И ПЕРИНАТОЛОГИИ
- •ГЛАВА 04.ПОСЛЕДИПЛОМНАЯ ПОДГОТОВКА ВРАЧЕЙ АКУШЕРОВГИНЕКОЛОГОВ В КОНТЕКСТЕ БОЛОНСКОЙ ДЕКЛАРАЦИИ
- •ГЛАВА 05.ДЕОНТОЛОГИЯ В АКУШЕРСТВЕ
- •ГЛАВА 07. ИЗМЕНЕНИЯ В ОРГАНИЗМЕ ЖЕНЩИНЫ ВО ВРЕМЯ БЕРЕМЕННОСТИ
- •ГЛАВА 08. РАЦИОНАЛЬНОЕ ПОВЕДЕНИЕ ЗДОРОВОЙ ЖЕНЩИНЫ В ПЕРИОД БЕРЕМЕННОСТИ
- •ГЛАВА 09. КЛИНИЧЕСКИЕ МЕТОДЫ ОБСЛЕДОВАНИЯ БЕРЕМЕННЫХ
- •ГЛАВА 10. ЛАБОРАТОРНЫЕ МЕТОДЫ ДИАГНОСТИКИ.
- •ГЛАВА 11. ИНСТРУМЕНТАЛЬНЫЕ НЕИНВАЗИВНЫЕ МЕТОДЫ ДИАГНОСТИКИ.
- •ГЛАВА 12.ИНСТРУМЕНТАЛЬНЫЕ ИНВАЗИВНЫЕ МЕТОДЫ ДИАГНОСТИКИ
- •ГЛАВА 13. ПРИНЦИПЫ АНЕСТЕЗИОЛОГИЧЕСКОГО ОБЕСПЕЧЕНИЯ В АКУШЕРСТВЕ
- •ГЛАВА 14. ХИРУРГИЧЕСКИЕ МЕТОДЫ ЛЕЧЕНИЯ
- •ГЛАВА 15. ФАРМАКОТЕРАПИЯ В АКУШЕРСКОЙ ПРАКТИКЕ
- •ГЛАВА 16.ВЕДЕНИЕ ФИЗИОЛОГИЧЕСКОЙ БЕРЕМЕННОСТИ
- •ГЛАВА 17. ФИЗИОЛОГИЧЕСКИЕ РОДЫ
- •ГЛАВА 18.ФИЗИОЛОГИЧЕСКОЕ ТЕЧЕНИЕ ПОСЛЕРОДОВОГО ПЕРИОДА И ПЕРИОДА НОВОРОЖДЁННОСТИ
- •ГЛАВА 19.БЕРЕМЕННОСТЬ У НЕСОВЕРШЕННОЛЕТНИХ
- •ГЛАВА 20.ТАКТИКА ВЕДЕНИЯ БЕРЕМЕННОСТИ ПОСЛЕ ЭКСТРАКОРПОРАЛЬНОГО ОПЛОДОТВОРЕНИЯ
- •ГЛАВА 21. МНОГОПЛОДНАЯ БЕРЕМЕННОСТЬ
- •ГЛАВА 22. САМОПРОИЗВОЛЬНЫЙ АБОРТ (ВЫКИДЫШ)
- •ГЛАВА 23. ПРИВЫЧНОЕ НЕВЫНАШИВАНИЕ БЕРЕМЕННОСТИ
- •ГЛАВА 24. НЕРАЗВИВАЮЩАЯСЯ БЕРЕМЕННОСТЬ
- •ГЛАВА 25. ПРЕЖДЕВРЕМЕННЫЕ РОДЫ
- •ГЛАВА 26. ПЕРЕНАШИВАНИЕ БЕРЕМЕННОСТИ
- •ГЛАВА 27. ПЛАЦЕНТАРНАЯ НЕДОСТАТОЧНОСТЬ
- •ГЛАВА 28. ЗАДЕРЖКА РОСТА ПЛОДА
- •ГЛАВА 29. ПАТОЛОГИЯ ОКОЛОПЛОДНЫХ ВОД
- •ГЛАВА 30. АНОМАЛИИ ПУПОВИНЫ, ОСЛОЖНЯЮЩИЕ ТЕЧЕНИЕ РОДОВ И УХУДШАЮЩИЕ ПЕРИНАТАЛЬНЫЙ ИСХОД
- •ГЛАВА 31. ТОКСИКОЗЫ БЕРЕМЕННЫХ И ГЕСТОЗ
- •ГЛАВА 32. НАСЛЕДСТВЕННЫЕ ДЕФЕКТЫ СИСТЕМЫ ГЕМОСТАЗА
- •ГЛАВА 33. АНТИФОСФОЛИПИДНЫЙ СИНДРОМ
- •ГЛАВА 34. HELLP-СИНДРОМ
- •ГЛАВА 35. СИНДРОМ ДИССЕМИНИРОВАННОГО ВНУТРИСОСУДИСТОГО СВЁРТЫВАНИЯ КРОВИ
- •ГЛАВА 36. ЭМБОЛИЯ ОКОЛОПЛОДНЫМИ ВОДАМИ
- •ГЛАВА 37. БЕРЕМЕННОСТЬ И ЗАБОЛЕВАНИЯ ВЕН
- •ГЛАВА 38. ИЗОСЕРОЛОГИЧЕСКАЯ НЕСОВМЕСТИМОСТЬ КРОВИ МАТЕРИ И ПЛОДА. ГЕМОЛИТИЧЕСКАЯ БОЛЕЗНЬ ПЛОДА И НОВОРОЖДЁННОГО
- •ГЛАВА 40. БЕРЕМЕННОСТЬ И ЗАБОЛЕВАНИЯ КРОВИ
- •ГЛАВА 41. БЕРЕМЕННОСТЬ И ЗАБОЛЕВАНИЯ ОРГАНОВ ДЫХАНИЯ
- •ГЛАВА 42. БЕРЕМЕННОСТЬ И ЗАБОЛЕВАНИЯ ОРГАНОВ ПИЩЕВАРЕНИЯ
- •ГЛАВА 43. БЕРЕМЕННОСТЬ И ЗАБОЛЕВАНИЯ ПОЧЕК И МОЧЕВЫВОДЯЩИХ ПУТЕЙ
- •ГЛАВА 44. БЕРЕМЕННОСТЬ И ОФТАЛЬМОЛОГИЧЕСКИЕ ОСЛОЖНЕНИЯ
- •ГЛАВА 45. БЕРЕМЕННОСТЬ И ЭНДОКРИННАЯ ПАТОЛОГИЯ. БЕРЕМЕННОСТЬ И БОЛЕЗНИ ЩИТОВИДНОЙ ЖЕЛЕЗЫ
- •ГЛАВА 46. БЕРЕМЕННОСТЬ И ДЕПРЕССИВНЫЕ СОСТОЯНИЯ
- •ГЛАВА 47. БЕРЕМЕННОСТЬ И ПСИХОАКТИВНЫЕ ВЕЩЕСТВА
- •ГЛАВА 48. ИНФЕКЦИОННЫЕ ЗАБОЛЕВАНИЯ ВО ВРЕМЯ БЕРЕМЕННОСТИ
- •ГЛАВА 49 БЕРЕМЕННОСТЬ И ДОБРОКАЧЕСТВЕННЫЕ ЗАБОЛЕВАНИЯ МАЛОГО ТАЗА
- •ГЛАВА 50. БЕРЕМЕННОСТЬ И ОНКОЛОГИЧЕСКИЕ ЗАБОЛЕВАНИЯ
- •ГЛАВА 51. БЕРЕМЕННОСТЬ И ХИРУРГИЧЕСКАЯ ПАТОЛОГИЯ
- •ГЛАВА 52. ПАТОЛОГИЧЕСКИЕ РОДЫ
- •ГЛАВА 53. КРОВОТЕЧЕНИЯ В АКУШЕРСКОЙ ПРАКТИКЕ
- •ГЛАВА 54 .ПАТОЛОГИЯ ПОСЛЕРОДОВОГО ПЕРИОДА
- •ГЛАВА 55. РОДОВОЙ ТРАВМАТИЗМ
- •ГЛАВА 56. ВНУТРИУТРОБНАЯ ИНФЕКЦИЯ
- •ГЛАВА 57. ВРОЖДЁННЫЕ ПОРОКИ РАЗВИТИЯ
- •ГЛАВА 58 .АСФИКСИЯ НОВОРОЖДЁННОГО
- •ГЛАВА 59. РЕСПИРАТОРНЫЙ ДИСТРЕСС-СИНДРОМ НОВОРОЖДЁННЫХ
- •ГЛАВА 60. ИНФЕКЦИИ НОВОРОЖДЁННЫХ
- •ГЛАВА 61. РОДОВЫЕ ТРАВМЫ ПЛОДА И НОВОРОЖДЁННОГО
- •ПРИЛОЖЕНИЕ. БЕЗОПАСНОСТЬ ИСПОЛЬЗОВАНИЯ ЛЕКАРСТВЕННЫХ СРЕДСТВ ВО ВРЕМЯ БЕРЕМЕННОСТИ
- •ПРАВА БЕРЕМЕННЫХ ЖЕНЩИН И КОРМЯЩИХ МАТЕРЕЙ
ГЛАВА 33. АНТИФОСФОЛИПИДНЫЙ СИНДРОМ
Антифосфолипидный синдром — термин, объединяющий патогенетические основы нарушения репродуктивной функции (в первую очередь, невынашивание беременности) и наличие антифосфолипидных АТ.
ЭПИДЕМИОЛОГИЯ
АФС обнаруживают в 12–15% случаев, причём у женщин в 2–5 раз чаще, чем у мужчин. Во время беременности антифосфолипидные АТ выявляют у 2–4% женщин. Среди пациенток с привычным невынашиванием беременности АФС диагностируют в 27–42% случаев.
КЛАССИФИКАЦИЯ
Выделяют следующие формы АФС:
•первичный АФС;
•вторичный АФС;
•АФС у больных с волчаночно-подобными проявлениями;
•катастрофический АФС;
•другие микроангиопатические синдромы (тромбоцитопеническая пурпура, ДВС-синдром, HELLP-синдром, гипопротромбический синдром);
•серонегативный АФС.
ЭТИОЛОГИЯ
Причины АФС до конца не изучены. Повышение концентрации антифосфолипидных АТ в крови, как правило, бывает транзиторным, и его отмечают на фоне многих инфекционных заболеваний бактериальной и особенно вирусной этиологии. Наличие латент-ной инфекции может способствовать развитию тромботических осложнений при АФС, несмотря на различия в иммунологических свойствах антифосфолипидных АТ, при истинных аутоиммунных процессах и воспалительных заболеваниях.
Проявления АФС могут быть генетически детермированными. Например, у больных с АФС чаще, чем в популяции, регистрируют Аг системы HLA DR4, DR7, DRw53, что свидетельствует о генетической предрасположенности к данному заболеванию.
ПАТОГЕНЕЗ
При взаимодействии антифосфолипидных АТ с фосфолипидами на мембранах эпителиальных клеток развивается системная эндотелиальная дисфункция и дисрегуляция в системе гемостаза. Проявлениями эндотелиальной дисфункции считают усиленную адгезию и агрегацию тромбоцитов, нарушение баланса между синтезом простациклина и тромбоксана и внутрисосудистый тромбоз в фетоплацентарном комплексе, который становится интегральным этиопатогенетическим фактором невынашивания беременности, тяжёлого гестоза, ЗРП и антенатальной гибели плода, ПОНРП.
Влияние антифосфолипидных АТ на систему гемостаза может проявляться также снижением активности естественных антикоагулянтов (протеина C, S и АТ III) и развитием тромботической и иммунной тромбоцитопении. Изза этих нарушений возникают вазоконстрикция, усиленная агрегация тромбоцитов и внутрисосудистый тромбоз. Возможны и другие коагуляционные нарушения, однако их конечным результатом при беременности бывает сосудистая недостаточность в плаценте.
Ранние преэмбрионические выкидыши при АФС обусловлены нарушением процесса имплантации. Под воздействием антифосфолипидных АТ изменяются предимплантационные характеристики морулы (заряд, конфигурация), нарушается слияние синцития, происходит подавление продукция ХГЧ, что приводит к снижению глубины инвазии трофобласта и прерыванию беременности.
Патологические состояния, в развитии которых играет роль АФС:
•привычное невынашивание беременности (включая НБ);
•ЗРП;
•плацентарная недостаточность;
•гестоз;
•HELLP-синдром;
•антенатальная гибель плода;
•ПОНРП.
ДИАГНОСТИКА
АНАМНЕЗ
При АФС в анамнезе у пациентки отмечают следующие нарушения:
•Один или более самопроизвольных выкидышей на сроке 10 нед и более (включая НБ).
•Три и более самопроизвольных выкидыша на преэмбрионической или ранней эмбрионической стадии (при исключении других причин невынашивания).
•Мертворождения.
•Неонатальная гибель плода как осложнение преждевременных родов, тяжёлого гестоза или плацентарной недостаточности.
•Случаи артериального или венозного тромбоза в возрасте до 45 лет (преходящие нарушения мозгового
кровообращения, тромбоз сосудов сетчатки, инфаркт, инсульт и др.).
•Патология ЦНС, сердечно-сосудистой системы, ЖКТ, эндокринных органов (болезни клапанов сердца, кардиомиопатия, лёгочная гипертензия, почечная и надпочечниковая недостаточность, гипопитуитаризм и др.).
ЛАБОРАТОРНЫЕ ИССЛЕДОВАНИЯ
•Определяют наличие волчаночного антикоагулянта в крови с помощью скрининговых тестов (АЧТВ, протромбинового времени, времени свертывания с использованием яда гадюки Рассела), коррекционной пробы, подтверждающих тестов.
•Выявляют высокие титры антикардиолипиновых АТ класса IgМ.
• Исследуют наличие АТ класса IgМ к подгруппе фосфолипидов (фосфадитилсерин, фосфадитилхолин, фосфадитилэтаноламин, фосфатидиловая кислота) и к кофакторам (β9-GPI, протромбин, аннексин V, протеин C, протеин S, тромбомодулин).
Предварительным диагностическим критерием АФС считают обнаружение антикардиолипиновых АТ и/или волчаночного антикоагулянта два и более раза при проведении исследований с интервалом 6–8 нед. При подозрении на АФС (в случае наличия тромботических нарушений, тромбоцитопении, акушерской патологии, а также при удлинении АЧТВ) лабораторные исследования следует проводить перед планируемой беременностью, во время беременности — на любом сроке и в послеродовом периоде.
Течение АФС, тяжесть и распространённость тромботических осложнений, как правило, не коррелируют с изменением титров антифосфолипидных АТ и активностью аутоиммунного процесса.
СКРИНИНГ
Показания к лабораторному и генетическому скринингу АФС:
•случаи тромбоза в семейном анамнезе или в раннем возрасте;
•самопроизвольное прерывание беременности;
•НБ;
•осложнённое течение беременности (гестоз, плацентарная недостаточность, преждевременная отслойка плаценты);
•длительный приём гормональных или цитостатических лекарственных средств.
ДИФФЕРЕНЦИАЛЬНАЯ ДИАГНОСТИКА
Дифференциальная диагностика АФС включает следующие нозологии:
•аутоиммунные заболевания соединительной ткани, прежде всего системные васкулиты;
•наследственные тромбофилии (мутации фактора V Лейден, гена протромбина G20210А, метилентетрагидрофолат
редуктазы C 6777 Т, полиморфизм гена активатора плазминогена, тромбоцитарных рецпторов);
• аутоиммунная тромбоцитопеническая пурпура.
ПОКАЗАНИЯ К КОНСУЛЬТАЦИИ ДРУГИХ СПЕЦИАЛИСТОВ
Наблюдать и вести пациенток с АФС следует совместно с врачами других специальностей (кардиолог, гематолог, сосудистый хирург и терапевт).
ПРИМЕР ФОРМУЛИРОВКИ ДИАГНОЗА
АФС (высокий титр АТ к кардиолипину) или АФС, серонегативная форма (АТ к β2-GPI).
ЛЕЧЕНИЕ
Общие принципы терапии АФС:
•По возможности следует устранить причину АФС.
•Лечение рекомендовано начинать до наступления беременности или в ранние сроки гестации на фоне тщательного мониторинга содержания антифосфолипидных АТ в крови.
•Проводят индивидуально подобранную противотромботическую терапию.
•Лечение АФС должно быть длительным и его необходимо проводить под контролем показателей гемостазиограммы.
ЦЕЛИ ЛЕЧЕНИЯ
Цель лечения АФС заключается в уменьшении количества циркулирующих аутоантител, активности аутоиммунного процесса, в предотвращении развития гемостазиологических нарушений и обеспечении пролонгирования беременности и рождения здорового ребенка.
ПОКАЗАНИЯ К ГОСПИТАЛИЗАЦИИ
Выделяют следующие показания к госпитализации в специализированный родильный дом:
•обследование и подбор противотромботической терапии;
•нарастание гемостазиологических нарушений на фоне проводимой терапии;
•осложнённое течение беременности (гестоз средней и тяжёлой степени тяжести, субкомпенсированная форма ПН);
•подозрение на катастрофическую форму АФС.
МЕДИКАМЕНТОЗНОЕ ЛЕЧЕНИЕ
•Показанием для назначения глюкокортикоидной терапии считают наличие в анамнезе аутоиммунных заболеваний. Лечение начинают во 2-й фазе предполагаемого фертильного цикла (со 2-го дня овуляции) и продолжают на протяжении всей беременности вплоть до 10–15 сут послеродового периода с последующей постепенной отменой препарата. Используют преднизолон в дозе 5 мг/сут (максимальная суточная доза составляет 10–15 мг) или метилпреднизолон в дозе 4 мг/сут.
•Иммуностимуляторы необходимы для профилактики реактивации вирусной инфекции на фоне иммуносупрессивной терапии: иммуноглобулин человеческий нормальный в дозе 25 мл через день (три дозы) в I триместре беременности, на сроке 24 недели и перед родами, вагинально (ректально) интерферон альфа-2 в дозе 1000 МЕ/сут.
•Антиагреганты показаны для коррекции гемостазиологических нарушений (гиперактивация тромбоцитов):
дипиридамол по 75–150 мг/сут за 1 ч до еды, пентоксифиллин по 10–20 мг/сут во время еды, ацетисалициловая кислота по 80–100 мг/сут (до 34 недель).
• Антикоагулянты назначают при выявлении гиперкоагуляции, обусловленной нарушениями плазменного звена гемостаза, при появлении в крови продуктов деградации фибрина, мономеров фибрина. Дозу препарата подбирают индивидуально, и её можно изменять.
G Нефракционированный гепарин по 15 000 ЕД/сут подкожно или по 10 000 ЕД/сут внутривенно капельно в 400 мл раствора декстрана с молекулярной массой 30 000–40 000.
G Надропарин кальций подкожно в лечебной дозе 0,01 мл (95 МЕ)/кг массы тела 2 раза в сутки. G Далтепарин натрий 1–2 раза в сутки подкожно в дозе 100–200 анти-Ха/кг массы тела.
G Эноксапарин натрия по 4000–10 000 МЕ/сут (40–100 мг/сут) подкожно.
• Для профилактики осложнённого течения беременности при АФС можно назначать также следующие лекарственные средства: препараты железа, фолиевую кислоту в дозе до 1–6 мг/сут, полинасыщенные жирные кислоты, поливитамины для беременных.
СРОКИ И МЕТОДЫ РОДОРАЗРЕШЕНИЯ
При нормальном течении беременности родоразрешение проводят на сроке 40 недель гестации. Роды ведут через естественные родовые пути, при наличии соответствующих показаний со стороны матери или плода — путём КС.
ПРИМЕРНЫЕ СРОКИ НЕТРУДОСПОСОБНОСТИ
Выдачу листка нетрудоспособности производят со срока беременности 30 недель единовременно. Его продолжительность должна составлять 140 календарных дней. В случае осложнённых родов листок нетрудоспособности продлевают на 16 календарных дней. Перечень заболеваний и состояний, при которых роды считают осложнёнными, определён «Инструкцией о порядке предоставления послеродового отпуска при осложённных родах» Минздрава России от 14 мая 1997 г. № 2510/2926-97-32, зарегистрированной Минюстом России 14 мая 1997 г. № 1305.
ОЦЕНКА ЭФФЕКТИВНОСТИ ЛЕЧЕНИЯ
Оценку эффективности лечения проводят на основании лабораторных методов исследования, а также по выраженности клинических симптомов заболевания. В течение первых четырёх недель еженедельно определяют количество и агрегационную способность тромбоцитов, содержание D-димера, молекулярных маркёров тромбофилии в крови. На основании результатов этих исследований можно выбрать препараты и определить их необходимую дозу для проведения противотромботической терапии в каждом конкретном случае. Далее исследования делают ежемесячно. При нарастании выраженности гемостазиологических нарушений увеличивают дозу назначенных препаратов или производят их замену.
Благодаря ультразвуковой допплерометрии, которую осуществляют со срока гестации 24 недели ежемесячно вплоть до родоразрешения, можно своевременно диагностировать снижение фетоплацентарного и маточноплацентарного кровотока и начать патогенетическую терапию ПН, а также оценить эффективность этого лечения. На основании результатов КТГ, проводимой со срока беременности 34 недели, оценивают состояние плода и выбрают оптимальный срок и метод родоразрешения.
ПРОФИЛАКТИКА
•Необходимо назначать адекватную антибактериальную терапию при лечении любого инфекционного заболевания.
•Не следует длительно применять гормональные препараты (контрацептивы, заместительную гормональную терапию).
ИНФОРМАЦИЯ ДЛЯ ПАЦИЕНТКИ
•Пациенткам с АФС рекомендовано проходить скрининг на волчаночный антикоагулянт и антикардиолипиновые АТ по крайней мере 2 раза перед каждой планируемой беременностью.
•На основании полученных результатов обследования следует обсудить с врачом прогноз беременности и возможное лечение с учётом его влияния на плод, которые могут и не быть напрямую связаны с клинической стадией заболевания у матери. Пациентки должны быть осведомлены о риске, сопряженном с назначением
иммуносупрессивной терапии, а также о высоком риске развития тромботических осложнений у матери.
• При наличии АФС показана длительная антиагрегантная и антикоагулянтная терапия на протяжении всей беременности и в послеродовом периоде.
ПРОГНОЗ
Прогноз АФС неблагоприятный. Без проведения лечения гибель эмбриона или плода при наличии АФС отмечают в 95–98% случаев. Частота рождения живого ребенка у матерей, имевших активность волчаночного антикоагулянта или высокую концентрацию АТ класса IgG в крови к кардиолипину, не превышает 10%. Летальность пациенток при катастрофической форме АФС достигает 60%.
СПИСОК РЕКОМЕНДУЕМОЙ ЛИТЕРАТУРЫ
Макацария А.Д., Бицадзе В.О. Антифосфолипидный синдром, генетические тромбофилии в патогенезе основных форм акушерской патологии / А.Д. Макацария, В.О. Бицадзе // Русский медицинский журнал. — 2006. — Специальный выпуск. — С. 2–10.
Макацария А.Д., Бицадзе В.О. Тромбофилии и противотромботическая терапия в акушерской практике / А.Д. Макацария, В.О. Бицадзе. — М.: Триада-Х, 2003. — 904 с.
Матвеева Т.Е. Вопросы патогенеза и профилактики синдрома потери плода у беременных с тромбофилией / Т.Е. Матвеева // Автореферат диссертации на соискание ученой степени канд. мед. наук. — М., 2002. — 25 с.
Насонов Е.Л. Современные подходы к профилактике и лечению антифосфолипидного синдрома / Е.Л. Насонов // Тер. Архив. — 2003. — № 5. — С. 83–87.
Руководство Дьюхерста по акушерству и гинекологии для постдипломного обучения / Под ред. Ч.Р. Уитфилда. — М.: Медицина, 2003. — 795 с.
Brenner B. Inherited thrombophilia and pregnancy loss / B. Brenner // Thrombosis and Haemostasis J. — 1999. — Vol. 82, N 2. — P. 634–641.
Loscalzo J. Oxidative stress in endothelial cell dysfunction and thrombosis / J. Loscalzo // Pathophysiologi of Haemostasis and Thrombosis J. — 2002. — Vol. 32, N 5–6. — P. 359–360.
ГЛАВА 34. HELLP-СИНДРОМ
HELLP-синдром — редкая и опасная патология в акушерстве. Первые буквы сокращённого названия синдрома обозначают следующее: Н — hemolysis (гемолиз); ЕL — еlеvated liver enzymes (повышение активности ферментов печени); LP — 1оw рlаtelet соunt (тромбоцитопения). Впервые этот синдром был описан в 1954 году Дж.А. Притчардом, а Р.С. Гудлин и соавт. (1978) связали проявление этого синдрома с преэклампсией. В 1982 году Л. Вейнштейн впервые объединил триаду симптомов c особой патологией — HELLP-синдромом.
ЭПИДЕМИОЛОГИЯ
При тяжёлом течении гестоза HELLP-синдром, при котором отмечают высокую материнскую (до 75%) и перинатальную (79 случаев на 1000 детей) смертность, диагностируют в 4–12% случаев.
КЛАССИФИКАЦИЯ
На основании лабораторных признаков некоторые авторы создали классификацию HELLP-синдрома.
•П.А Ван Дам и соавт. разделяют больных по лабораторным показателям на 3 группы: с явными, подозреваемыми и скрытыми признаками внутрисосудистой коагуляции.
•По сходному принципу построена классификация Дж.Н. Мартина, в которой пациенток с HELLP-синдромом подразделяют на два класса.
G Первый класс — содержание тромбоцитов в крови составляет менее 50×109/л. G Второй класс — концентрация тромбоцитов в крови равна 50–100×109/л.
ЭТИОЛОГИЯ
До настоящего времени истинную причину развития HELLP-синдрома выявить не удалось, однако были уточнены некоторые аспекты развития данной патологии.
Отмечают возможные причины развития HELLP-синдрома.
•Иммуносупрессия (депрессия T-лимфоцитов и B-лимфоцитов).
•Аутоиммунная агрессия (антитромбоцитарные, антиэндотелиальные АТ).
•Уменьшение отношения простациклин/тромбоксан (снижение продукции простациклинстимулирующего фактора).
•Изменения в системе гемостаза (тромбоз сосудов печени).
•АФС.
•Генетические дефекты ферментов печени.
•Применение лекарственных препаратов (тетрациклин, хлорамфеникол).
Выделяют следующие факторы риска развития HELLP-синдрома.
•Светлая кожа.
•Возраст беременной старше 25 лет.
•Многорожавшие женщины.
•Многоплодная беременность.
•Наличие выраженной соматической патологии.
ПАТОГЕНЕЗ
Патогенез HELLP-синдрома в настоящее время изучен не полностью (рис. 34-1).
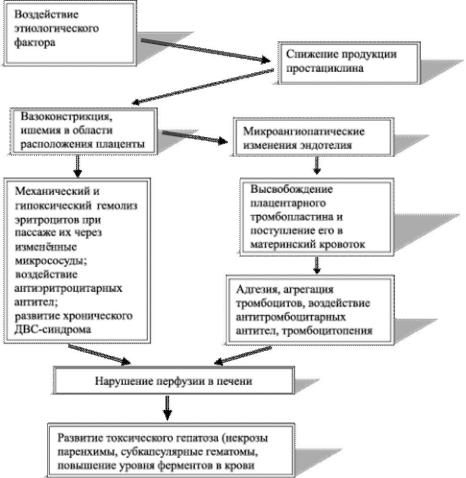
Рис. 34-1. Патогенез HELLP-синдрома.
Основными этапами развития HELLP-синдрома при тяжёлой форме гестоза считают аутоиммунное повреждение эндотелия, гиповолемию со сгущением крови и образование микротромбов с последующим фибринолизом. При повреждении эндотелия увеличивается агрегация тромбоцитов, что, в свою очередь, способствует вовлечению в патологический процесс фибрина, коллагеновых волокон, системы комплемента, IgG и IgM. Аутоиммунные комплексы обнаруживают в синусоидах печени и в эндокарде. В связи с этим целесообразно использовать при HELLP-синдроме глюкокортикоиды и иммунодепрессанты. Разрушение тромбоцитов приводит к высвобождению тромбоксанов и нарушению равновесия в тромбоксан-простациклиновой системе, генерализованному артериолоспазму с усугублением АГ, отёку мозга и судорогам. Развивается порочный круг, разорвать который в настоящее время возможно только путём экстренного родоразрешения.
Гестоз считают синдромом ПОН, а HELLP-синдром — её крайней степенью, бывающей следствием дезадаптации материнского организма при попытке обеспечения нормальной жизнедеятельности плода.
Макроскопически при HELLP-синдроме отмечают увеличение размеров печени, уплотнение её консистенции, субкапсулярные кровоизлияния. Окраска печени становится светло-коричневой. При микроскопическом исследовании обнаруживают перипортальные геморрагии, отложения фибрина, IgM, IgG в синусоидах печени, мультилобулярный некроз гепатоцитов.
КЛИНИЧЕСКАЯ КАРТИНА
HELLP-синдром обычно возникает в III триместре беременности, чаще на сроке 35 нед и более. Для заболевания характерно быстрое нарастание симптомов. Первоначальные проявления неспецифичны: тошнота и рвота (в 86% случаев), боли в эпигастральной области и, особенно, в области правого подреберья (в 86% случаев), выраженные отёки (в 67% случаев), головная боль, утомляемость, недомогание, моторное беспокойство, гиперрефлексия.
Характерными признаками заболевания являются желтуха, рвота с кровью, кровоизлияния в местах инъекций, нарастающая печёночная недостаточность, судороги и выраженная кома.
Наиболее распространённые клинические признаки HELLP-синдрома представлены в табл. 34-1.
ДИАГНОСТИКА
ЛАБОРАТОРНЫЕ ИССЛЕДОВАНИЯ
Довольно часто лабораторные изменения возникают гораздо раньше клинических проявлений.
• Одним из основных лабораторных симптомов HELLP-синдрома служит гемолиз, который проявляется наличием в мазке крови сморщенных и деформированных эритроцитов, полихромазией. Разрушение эритроцитов ведёт к освобождению фосфолипидов и к внутрисосудистому свёртыванию, т.е. хроническому ДВС-синдрому, который бывает причиной смертельных акушерских кровотечений.
• При подозрении на HELLP-синдром необходимо немедленно провести лабораторные исследования, включающие определение активности АЛТ, АСТ, лактатдегидрогензы, концентрации билирубина, гаптоглобина, мочевой кислоты, количества тромбоцитов в крови и оценку состояния свёртывающей системы крови.
Основополагающими критериями диагностики HELLP-синдрома служат лабораторные показатели (табл. 34-2).
Таблица 34-1. Клиническая картина HELLP-синдрома |
|
|
|
|
Признаки |
|
|
HELLP-синдром |
|
|
|
|
|
|
Боль в эпигастральной области и/или в правом подреберье |
|
+++ |
|
|
|
|
|
|
|
Головная боль |
|
|
++ |
|
|
|
|
|
|
Желтуха |
|
|
+++ |
|
|
|
|
|
|
АГ |
|
|
+++/– |
|
|
|
|
|
|
Протеинурия (более 5 г/сут) |
|
|
+++/– |
|
|
|
|
|
|
Периферические отёки |
|
|
++/– |
|
|
|
|
|
|
Рвота |
|
|
+++ |
|
|
|
|
|
|
Тошнота |
|
|
+++ |
|
|
|
|
|
|
Мозговые или зрительные нарушения |
|
|
++/– |
|
|
|
|
|
|
Олигурия (менее 400 мл/сут) |
|
|
++ |
|
|
|
|
|
|
Острый тубулярный некроз |
|
|
++ |
|
|
|
|
|
|
Корковый некроз |
|
|
++ |
|
|
|
|
|
|
Гематурия |
|
|
++ |
|
|
|
|
|
|
Пангипопитуитаризм |
|
|
++ |
|
|
|
|
|
|
Отёк лёгких или цианоз |
|
|
+/– |
|
|
|
|
|
|
Слабость, утомляемость |
|
|
+/– |
|
|
|
|
|
|
Желудочное кровотечение |
|
|
+/– |
|
|
|
|
|
|
Кровоизлияния в местах инъекций |
|
|
+ |
|
|
|
|
|
|
Нарастающая печёночная недостаточность |
|
+ |
|
|
|
|
|
|
|
Печёночная кома |
|
|
+/– |
|
|
|
|
|
|
Судороги |
|
|
+/– |
|
|
|
|
|
|
Асцит |
|
|
+/– |
|
|
|
|
|
|
Лихорадка |
|
|
++/– |
|
|
|
|
|
|
Кожный зуд |
|
|
+/– |
|
|
|
|
|
|
Снижение массы тела |
|
|
+ |
|
|
|
|
|
|
Примечание: +++, ++, +/– — выраженность проявлений. |
|
|
|
|
Таблица 34-2. Данные лабораторного исследования |
|
|
|
|
Лабораторные показатели |
|
|
Изменения при HELLP-синдроме |
|
|
|
|
|
|
Содержание лейкоцитов в крови |
В пределах нормы |
|
|
|
|
|
|||
Активность аминотрансфераз в крови |
Повышено до 500 ЕД (норма до 35 ЕД) |
|||
(АЛТ, АСТ) |
|
|
|
|
|
|
|||
Активность ЩФ в крови |
Выраженное повышение (в 3 раза и более) |
|||
|
|
|
|
|
Концентрация билирубина в крови |
20 мкмоль/л и более |
|
|
|
|
|
|
СОЭ |
|
Снижена |
|
|
|
Количество лимфоцитов в крови |
|
Норма или незначительное снижение |
|
|
|
Концентрация белка в крови |
|
Снижена |
|
|
|
Количество тромбоцитов в крови |
|
Тромбоцитопения (менее 100×109/л) |
|
|
|
Характер эритроцитов в крови |
|
Изменённые эритроциты с клетками Барра, полихромазия |
|
|
|
Количество эритроцитов в крови |
|
Гемолитическая анемия |
|
|
|
Протромбиновое время |
|
Увеличено |
|
|
|
Концентрация глюкозы в крови |
|
Снижена |
|
|
|
Факторы свертывания крови |
|
Коагулопатия потребления: снижение содержания факторов, для синтеза |
|
|
которых в печени необходим витамин K, снижение концентрации антитромбина |
|
|
III в крови |
|
|
|
Концентрация азотистых веществ |
в |
Повышена |
крови (креатинин, мочевина) |
|
|
|
|
|
Содержание гаптоглобина в крови |
|
Снижено |
|
|
|
ИНСТРУМЕНТАЛЬНЫЕ ИССЛЕДОВАНИЯ
• Для раннего обнаружения субкапсульной гематомы печени показано УЗИ верхней части живота. При УЗИ печени у беременных с тяжёлым гестозом, осложнённым HELLP-синдромом, также обнаруживают множественные гипоэхогенные участки, которые расценивают как признаки перипортальных некрозов и кровоизлияний (геморрагического инфаркта печени).
• Для дифференциальной диагностики HELLP-синдрома используют КТ и МРТ.
ДИФФЕРЕНЦИАЛЬНАЯ ДИАГНОСТИКА
Несмотря на трудности диагностики HELLP-синдрома, выделяют ряд характерных для данной нозологии признаков: тромбоцитопения и нарушение функций печени. Выраженность этих нарушений достигает максимума спустя 24–48 ч после родов, в то время как при тяжёлом гестозе, наоборот, наблюдают регресс этих показателей в течение первых суток послеродового периода.
Признаки HELLP-синдрома могут быть и при других патологических состояниях помимо гестоза. Необходима дифференциальная диагностика данного состояния с гемолизом эритроцитов, повышением активности печёночных ферментов в крови и тромбоцитопенией, развившихся при следующих заболеваниях.
•Кокаиновая наркомания.
•Системная красная волчанка.
•Тромбоцитопеническая пурпура.
•Гемолитический уремический синдром.
•Острый жировой гепатоз беременных.
•Вирусные гепатиты A, B, C, E.
•ЦМВИ и инфекционный мононуклеоз.
Клиническая картина поражения печени при беременности часто бывает стёртой и вышеописанные симптомы врачи иногда рассматривают в качестве проявления иной патологии.
ПОКАЗАНИЯ К КОНСУЛЬТАЦИИ ДРУГИХ СПЕЦИАЛИСТОВ
Показаны консультации реаниматолога, гепатолога, гематолога.
ПРИМЕР ФОРМУЛИРОВКИ ДИАГНОЗА
Беременность 36 недель, головное предлежание. Гестоз в тяжёлой форме. HELLP-синдром.
ЛЕЧЕНИЕ
ЦЕЛИ ЛЕЧЕНИЯ
Восстановление нарушенного гомеостаза.
ПОКАЗАНИЯ К ГОСПИТАЛИЗАЦИИ
HELLP-синдром как проявление тяжёлого гестоза во всех случаях служит показанием для госпитализации.
НЕМЕДИКАМЕНТОЗНОЕ ЛЕЧЕНИЕ
Экстренное родоразрешение проводят на фоне инфузионно-трансфузионной терапии под наркозом.
МЕДИКАМЕНТОЗНОЕ ЛЕЧЕНИЕ
Наряду с инфузионно-трансфузионной терапией назначают ингибиторы протеаз (апротинин), гепатопротекторы (витамин C, фолиевая кислота), липоевую кислоту по 0,025 г 3–4 раза в сутки, свежезамороженную плазму в дозе не менее 20 мл/кг массы тела в сутки, переливание тромбоконцентрата (не менее 2 доз при содержании тромбоцитов менее 50×109/л), глюкокортикоиды (преднизолон в дозе не менее 500 мг/сут внутривенно). В послеоперационном периоде под контролем клинико-лабораторных показателей продолжают введение свежезамороженной плазмы в дозе 12–15 мл/кг массы тела с целью восполнения содержания плазменных факторов свертывания крови, а также рекомендуют проводить плазмаферез в сочетании с заместительным переливанием свежезамороженной плазмы,
ликвидацию гиповолемии, антигипертензивную и иммунодепрессивную терапию. Майенн и соавт. (1994) считают, что введение глюкокортикоидов способствует улучшению исхода для матери у женщин с преэклампсией и HELLPсиндромом.
СРОКИ И МЕТОДЫ РОДОРАЗРЕШЕНИЯ
При HELLP-синдроме показано экстренное родоразрешение путём КС на фоне коррекции метаболических нарушений, заместительной и гепатопротекторной терапии и проведения профилактики осложнений (табл. 34-3).
Таблица 34-3. Возможные осложнения у беременных с тяжёлым гестозом, осложнившимся HELLP-синдромом
Осложнения |
|
Частота развития при HELLP-синдроме |
|
|
|
ОПН |
|
8% |
|
|
|
Отёк лёгких |
|
6% |
|
|
|
Кровоизлияния в головной мозг |
|
5% |
|
|
|
Разрыв гематомы печени |
|
1,8% |
|
|
|
Субкапсулярная печёночная гематома |
|
2% |
|
|
|
ПОНРП |
|
22% |
|
|
|
Летальный исход |
|
24,2% |
|
|
|
При КС следует применять наиболее щадящие методы защиты матери и плода от акушерской агрессии. Останавливая свой выбор на перидуральной или спинномозговой анестезии, нельзя забывать о высоком риске экстрадуральных и субдуральных кровотечений при тромбоцитопении. Содержание тромбоцитов менее 100×109/л считают критической величиной для проведения регионарной анестезии при тяжёлом гестозе с HELLP-синдромом. Субдуральные гематомы могут возникать при регионарной анестезии также у беременных с тяжёлым гестозом, длительно принимавших ацетилсалициловую кислоту.
При родоразрешении особое внимание обращают на состояние детей. Установлено, что у новорождённых в 36% случаев возникает тромбоцитопения, что приводит к развитию у них кровоизлияний и поражений нервной системы. В состоянии асфиксии рождаются 5,6% детей, а у большинства новорождённых диагностируют РДС. В 39% случаев отмечают ЗРП, в 21% случаев — лейкопению, в 33% случаев — нейтропению, в 12,5% случаев — внутричерепные кровоизлияния, в 6,2% случаев — некроз кишечника.
ОЦЕНКА ЭФФЕКТИВНОСТИ ЛЕЧЕНИЯ
Успех интенсивной терапии HELLP-синдрома во многом зависит от своевременной диагностики, как до родов, так и в послеродовом периоде. Несмотря на крайнюю тяжесть течения HELLP-синдрома, его присоединение не должно служить оправданием летального исхода тяжёлого гестоза, а скорее свидетельствует о несвоевременной диагностике и поздней или неадекватной интенсивной терапии.
ПРОФИЛАКТИКА
Своевременная диагностика и адекватное лечение гестоза.
ИНФОРМАЦИЯ ДЛЯ ПАЦИЕНТКИ
HELLP-синдром — тяжёлое осложнение гестоза, требующее профессионального лечения в стационаре. В большинстве случаев через неделю после родоразрешения проявления заболевания проходят.
ПРОГНОЗ
При благоприятном течении в послеродовом периоде наблюдают быструю регрессию всех симптомов. По окончании беременности спустя 3–7 сут нормализуются лабораторные показатели крови, за исключением случаев выраженной тромбоцитопении (ниже 50×109/л), когда при использовании соответствующей корригирующей терапии, содержание тромбоцитов возвращается к норме на 11-е сутки, а активность ЛДГ — через 8–10 сут. Риск развития рецидивов при последующей беременности невелик и составляет 4%, но женщин следует отнести в группу повышенного риска по развитию данной патологии.
СПИСОК РЕКОМЕНДУЕМОЙ ЛИТЕРАТУРЫ
Акушерство: Справочник Калифорнийского университета / Под ред. К. Нисвандера, А. Эванса. — М.: Практика, 1999. — С. 132–134.
Валленберг Х.С.С. Новые достижения в тактике ведения ранней преэклампсии и HELLP-синдрома / Х.С.С. Валленберг // Акушерство и гинекология. — 1998. — № 5. — С. 29–32.
Интенсивная терапия в акушерстве и гинекологии / В.И. Кулаков и др. — М.: Медицинское информационное агентство, 1998. — С. 44–61.
Достижение с помощью терапии дексаметазоном лучших результатов лечения матерей с послеродовым HELLPсиндромом / Мартин Дж. и др. // АГ-инфо. — 2000. — № 1. — С. 20–21.
Макацария А.Д., Бицадзе В.О. Тромбофилии и противотромботическая терапия в акушерской практике / А.Д. Макацария, В.О. Бицадзе. – М.: Триада-Х, 2003. – 904 с.
Николаева Е.И., Бобкова М.В. HELLP-синдром или острый жировой гепатоз беременных / Е.И. Николаева, М.В. Бобкова // Медицинская помощь. — Медицина, 1994. —№ 2. — С. 23–25.
Сидорова И.С. Гестоз / И.С. Сидорова. — М., 1997. — С. 130–136.
Суров А.В. Hellp-синдром в акушерстве / А.В. Суров // Акушерство и гинекология. — 1997. — № 6. — С. 7–9.
Савельева Г.М., Шалина Р.И., Белякова Г.И. HELLP-синдром: этиология, патогенез, диагностика, лечение / Г.М. Савельева, Р.И. Шалина, Г.И. Белякова // Вестник российской ассоциации акушеров-гинекологов. — 1997. — № 2. — С. 33–37.
Хадасевич Л.С., Харева О.В., Абрамов А.А. Преэклампсия беременных, осложнённая HELLP-синдромом / Л.С. Хадасевич, О.В. Харева, А.А. Абрамов // Архив патологии. — 1999. — Т. 61, № 6. — С. 41–43.
