- •Федеральное агентство морского и речного транспорта
- •Предисловие
- •Лекция 1. Предмет физики.
- •1. Кинематика. Движение тел.
- •2. Движение материальной точки.
- •3. Скорость.
- •4. Ускорение.
- •5. Вращательное движение. Угловая скорость и угловое ускорение.
- •6. Качение тела.
- •Лекция 2. Динамика материальной точки.
- •1. Первый закон Ньютона.
- •2. Второй закон Ньютона.
- •3. Третий закон Ньютона.
- •4. Закон всемирного тяготения. Сила тяжести. Вес.
- •Силы упругости.
- •Силы трения.
- •Лекция 3. Закон сохранения импульса.
- •Введение.
- •Закон сохранения импульса.
- •Закон движения центра масс.
- •Движение тел с переменной массой. Реактивное движение.
- •Лекция 4. Закон сохранения энергии в механике.
- •Энергия, работа, мощность.
- •Потенциальная энергия.
- •Кинетическая энергия
- •Закон сохранения энергии.
- •Удар абсолютно упругих и абсолютно неупругих тел.
- •Лекция 5. Динамика вращательного движения твердого тела.
- •Вращение твердого тела вокруг неподвижной оси. Кинетическая энергия.
- •2. Момент инерции твердого тела.
- •3. Моменты инерции тел различной формы.
- •4. Момент силы относительно неподвижной точки.
- •5. Момент силы относительно неподвижной оси.
- •6. Момент импульса относительно неподвижной точки.
- •7. Момент импульса относительно неподвижной осиz.
- •Лекция 6. Уравнения динамики вращательного движения.
- •1. Закон сохранения момента импульса.
- •2. Гироскоп.
- •Лекция 7 Колебания и волны.
- •Свободные гармонические колебания. Гармонический осциллятор.
- •Задача о колебании груза на пружине.
- •Задача о физическом маятнике.
- •Задача о математическом маятнике.
- •Скорость и ускорение при гармоническом колебании.
- •Энергия гармонического осциллятора.
- •Лекция 8. Сложение колебаний.
- •Сложение гармонических колебаний одного направления и одной частоты.
- •Биения.
- •Формула для сложения колебаний в общем случае для плоских волн.
- •Вынужденные колебания.
- •Затухающие колебания.
- •Механические волны (упругие волны)
- •Лекция 9 Уравнение плоской гармонической волны.
- •Фронт волны
- •Фазовая скорость.
- •Волновое уравнение.
- •Стоячие волны.
- •Звуковые волны.
- •Лекция 10 Механика жидкости
- •Линии и трубки тока. Неразрывность струи.
- •Уравнение Бернулли.
- •Ламинарное и турбулентное течение.
- •Силы сопротивления при движении тел в жидкостях. Закон Стокса. Число Рейнольдса.
- •Лекция 11 Физические основы молекулярно-кинетической теории газов.
- •1. История.
- •2. Идеальный газ. Параметры состояния газа. Уравнение состояния идеального газа.
- •3. Атомная единица массы (а.Е.М.).
- •4. Свойства идеального газа.
- •5. Уравнение Менделеева-Клапейрона.
- •6. Основное уравнение кинетической теории газов (уравнение Клаузиуса).
- •Лекция 12 Первый закон термодинамики.
- •1. Термодинамические системы (тдс).
- •2. Внутренняя энергия систем.
- •3. Первый закон термодинамики. Термодинамические процессы.
- •4. Работа газа при изменении его объема.
- •5. Теплоемкость.
- •Лекция 13 Термодинамические процессы.
- •1. Изохорный процесс
- •2. Изобарный процесс.
- •3. Изотермический процесс.
- •Лекция 14
- •4. Адиабатический процесс.
- •5. Политропический процесс.
- •Лекция 15 Второе начало термодинамики. Сущность второго начала термодинамики.
- •1. Введение
- •2. Обратимые и необратимые процессы.
- •3. Круговые процессы (циклы).
- •4. Прямой цикл (тепловая машина).
- •5. Обратный цикл (холодильник).
- •6. Цикл Карно. Произвольный обратимый цикл.
- •Лекция 16 Энтропия.
Лекция 14
4. Адиабатический процесс.
Адиабатический процесс осуществляется без теплообмена рабочего тела со средой.
1. Условием процесса является отсутствие теплообмена
![]() (1)
(1)
Для получения уравнения адиабаты используем две формы записи первого закона термодинамики
![]() (2)
(2)
![]()
![]()
![]() (3)
(3)
Из условия (1), (2) и (3) имеем
![]()
![]() .
.
Поделив первое уравнение на второе, получим
![]() .
.
Теперь
![]() или
или![]() .
(4)
.
(4)
Выражение (4) является дифференциалом
![]() .
.
Тогда имеем
![]()
или
![]() (5)
(5)
- уравнение Пуассона или уравнение
адиабаты,
![]() - показатель адиабаты.
- показатель адиабаты.
|
|
2. На рисунке изображены графики
изотермы и адиабаты. Адиабата ( 3. Связь между параметрами найдем из уравнения адиабаты (5)
|
|
Рис.1. |
|
Связь между параметрами
![]() и
и![]() найдем, используя уравнения состояния
найдем, используя уравнения состояния
![]()
![]() .
.
Деля первое на второе, получим
![]() .
.
Подставив это выражение в (6), получаем
![]() ,
,
или
![]() ,
,
или
![]() .
(7)
.
(7)
Сравнивая (6) и (7), получим
![]() ,
,
или
![]() .
(8)
.
(8)
4. Изменение внутренней энергии определяется выражением
![]() .
.
Так как
![]() ,
то
,
то
![]() .
(9)
.
(9)
Учтем, что
![]() и
и![]() ,
тогда
,
тогда
![]() .
(10)
.
(10)
Преобразуем (10), учитывая (7)
![]() .
(11)
.
(11)
В адиабатическом расширении газа вся совершаемая газом работа осуществляется за счет уменьшения внутренней энергии газа.
5. Политропический процесс.
До сих пор рассматривались процессы, у которых имелись вполне определенные признаки: изохорный – постоянный объем; изобарный – постоянное давление; изотермический – постоянная температура; адиабатный – при отсутствии теплообмена между рабочим телом и внешней средой. Наряду с этими процессами можно представить еще бесконечное множество процессов, у которых имеются другие постоянные признаки.
Условились всякий процесс идеального газа, в котором теплоемкость является постоянной величиной, называть политропным процессом.
Из определения политропного процесса следует, что основные термодинамические процессы – изохорный, изобарный, изотермический и адиабатный, если они протекают при постоянной теплоемкости, являются частными случаями политропного процесса.
Теплоемкость политропного процесса
![]() может принимать самые разнообразные
положительные и отрицательные значения
от
может принимать самые разнообразные
положительные и отрицательные значения
от![]() до
до![]() .
Количество теплоты, участвующее в
политропном процессе, может быть выражено
произведением теплоемкости процесса
.
Количество теплоты, участвующее в
политропном процессе, может быть выражено
произведением теплоемкости процесса![]() на разность температур.
на разность температур.
![]() ,
,
или
![]()
1. Уравнение политропического процесса выводится на основании первого закона термодинамики:
![]() =
=![]()
![]() =
=![]() .
.
Преобразуем эти выражения
![]()
![]() .
.
Разделим первое на второе
![]() (1)
(1)
Введем обозначение
![]() (2)
(2)
Тогда уравнение (1) примет вид
![]() или
или![]() (3)
(3)
Выражение (3) является дифференциалом
выражения
![]() .
Тогда
.
Тогда
![]() .
(4)
.
(4)
После потенцирования выражения (4) получим
![]() .
(5)
.
(5)
Уравнение (5) является уравнением
политропического процесса,
![]() - показатель политропы.
- показатель политропы.
Теплоемкость политропного процесса определяется из формулы (2)
![]()
![]()
![]() ,
так как
,
так как![]() .
Теперь
.
Теперь
![]() (6)
(6)
Из уравнений (6) и (2) можно получить значения теплоемкостей термодинамических процессов и показатели политропы. Все они занесены в таблицу.
|
№ |
Процесс |
|
|
Уравнение состояния. |
|
1.
2.
3.
4. |
Изохорический
Изобарический
Изотермический
Адиабатический |
0
1
|
|
|
2. Поскольку уравнение политропы
отличается от уравнения адиабаты только
величиной показателя
![]() ,
то все соотношения между основными
параметрами могут быть представлены
формулами, аналогичными адиабатному
процессу.
,
то все соотношения между основными
параметрами могут быть представлены
формулами, аналогичными адиабатному
процессу.
![]() ,
,![]() ,
,![]() .
.
3. Изменение внутренней энергии газа и теплота в политропном процессе определяется по формулам
![]() ,
,
![]() .
.
Уравнение работы изменения объема, совершаемой телом при политропном процессе имеет аналогичный вид с уравнением работы в адиабатном процессе
![]() ,
,
![]() .
.
Значение
![]() в любом политропном процессе может быть
определено по параметрам двух состояний
процесса.
в любом политропном процессе может быть
определено по параметрам двух состояний
процесса.
|
|
|
|
Рис.2. |
|
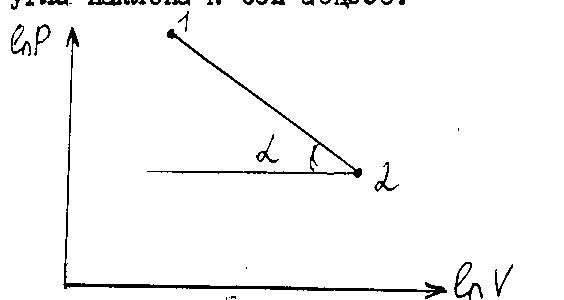
Изображая политропный процесс в
логарифмических координатах можно
очень просто определить
![]() (рис.2).
(рис.2).
![]() ,
,
![]() - это уравнение прямой в координатах
- это уравнение прямой в координатах![]() и
и![]() ,
а показатель политропы
,
а показатель политропы![]() - тангенс угла наклона к оси абсцисс.
- тангенс угла наклона к оси абсцисс.
Все реальные процессы, протекающие в тепловых машинах, можно аппроксимировать политропными процессами с соответствующими показателями политропы , которые могут быть найдены по экспериментальным данным ( по замерам давлений и удельных объемов в начальном и конечном состояниях газа).
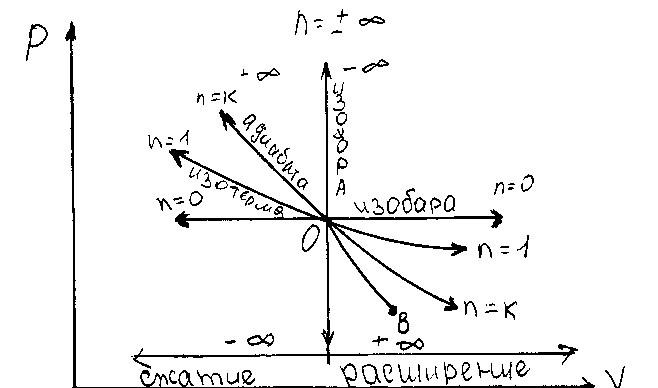
4. Особенности распределения энергии в различных политропных процессах.
Рассмотрим расположение политропных
процессов на
![]() -
диаграмме.(см. рис. 3),
-
диаграмме.(см. рис. 3),
|
|
выходящие из одной и той же точки, в зависимости от величины показателя. |
|
Рис.3. |
|
|
|
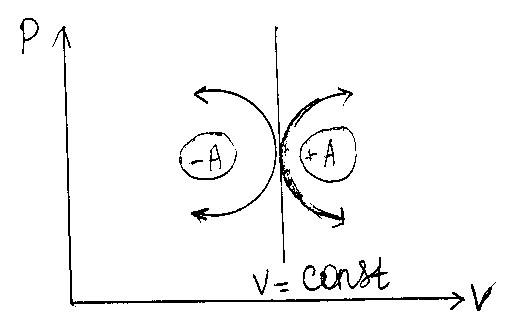
. В процессах расположенных справа от изохоры газ совершает работу (+А), а расположенных слева – внешние силы совершают работу над газом (-А) (см. рис. 4)
|
|
Рис. 4. |
|
|
|
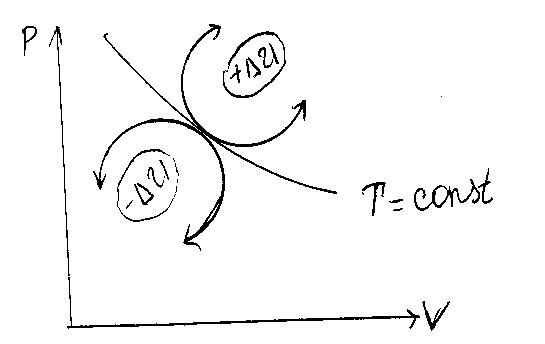
Процессы, расположенные выше изотермы, протекают с увеличением внутренней энергии, а процессы расположенные ниже изотермы – с уменьшением внутренней энергии (см. рис. 5.) |
|
Рис. 5. |
|
|
|
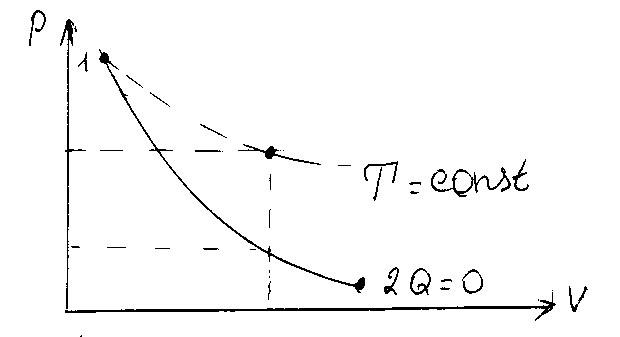
Процессы, расположенные выше адиабаты, протекают с подводом тепла, а расположенные ниже – с отводом тепла. (см. рис. 6). |
|
Рис. 6. |
|

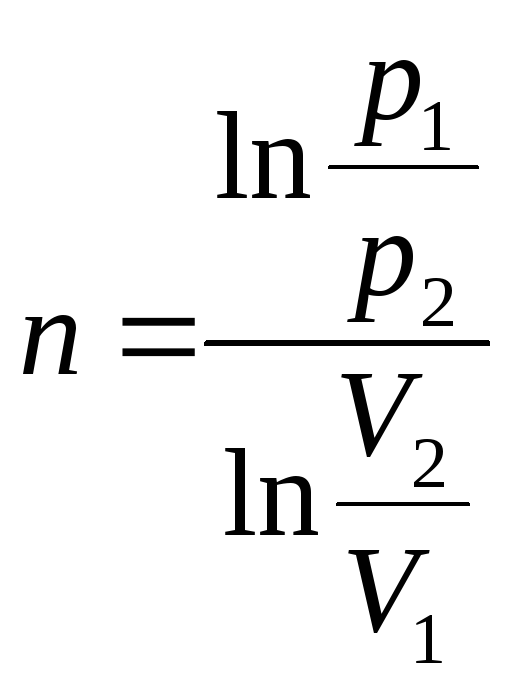 .
.