
- •И. В. Крепышева
- •Содержание
- •Тема 7. Химия металлов 125
- •1.2. Квантово-механическая модель атома водорода
- •1.3. Строение многоэлектронных атомов
- •1.4. Периодическая система элементов д.И. Менделеева
- •1.5. Периодические свойства элементов
- •1.6. Решение типовых задач
- •1.7. Задачи для самостоятельного решения
- •Тема 2. Химическая связь
- •2.1. Ковалентная связь
- •2.2. Гибридизация атомных орбиталей
- •2.3. Ионная химическая связь
- •2.4. Металлическая связь
- •2.5. Водородная связь
- •2.6. Строение твердого тела
- •Тема 3. Элементы химической термодинамики
- •3.1. Основные понятия термодинамики
- •3.2. Внутренняя энергия
- •3.3. Энтальпия
- •3.4. Термохимия. Закон Гесса
- •3.5. Энтропия
- •3.6. Самопроизвольные процессы. Энергия Гиббса
- •3.7. Решение типовых задач
- •3.8. Задачи для самостоятельного решения
- •Тема 4. Химическая кинетика и химическое равновесие
- •4.1. Скорость химической реакции
- •4.2. Зависимость скорости химической реакции от концентрации реагирующих веществ
- •4.3. Зависимость скорости реакции от температуры
- •4.4. Катализ
- •4.5. Химическое равновесие
- •4.6. Смещение химического равновесия. Принцип Ле Шателье
- •4.7. Решение типовых задач
- •4.8. Задачи для самостоятельного решения
- •Тема 5. Растворы. Дисперсные системы
- •5.1. Общие свойства растворов
- •5.2. Способы выражения состава растворов
- •5.3. Теория электролитической диссоциации
- •5.4. Теории кислот и оснований
- •5.5. Ионные реакции в растворах
- •5.6. Ионное произведение воды. Водородный показатель рН
- •5.7. Гидролиз солей
- •5.8. Дисперсные системы и их классификация
- •5.9. Решение типовых задач
- •28,57 Г соли растворены в 71,43 г воды
- •3% Массы раствора составляют 48,84 г
- •Соотношение между рН и рОн
- •5.10. Задачи для самостоятельного решения
- •Тема 6. Окислительно-восстановительные электрохимические процессы
- •6.1. Основные понятия
- •Правила определения степени окисления
- •6.2. Составление уравнений окислительно-восстановительных реакций
- •6.3. Влияние среды на характер протекания реакций
- •6.4. Важнейшие окислители и восстановители
- •6.5. Электрохимические процессы
- •96500 Кл (26,8 а∙ч) – 31,77 г Cu (масса моля эквивалентов)
- •96500 Кл – 1 г (11,2 л– объем моля эквивалентов)
- •6.6. Гальванический элемент Даниэля-Якоби
- •6.7. Окислительно-восстановительные потенциалы
- •6.8. Эдс окислительно-восстановительных реакций
- •6.9. Электролиз расплавов и растворов солей
- •6.10. Некоторые области применения электрохимии
- •6.11. Решение типовых задач
- •6.12. Задачи для самостоятельного решения
- •Тема 7. Химия металлов
- •7.1. Общая характеристика металлов
- •7.2. Химические свойства металлов
- •7.3. Взаимодействие металлов с кислотами
- •Взаимодействие металлов с соляной кислотой.
- •Взаимодействие металлов с азотной кислотой
- •Взаимодействие металлов с серной кислотой
- •7.4. Сплавы
- •7.5. Получение металлов
- •Тема 8. Коррозия и защита металлов
- •8.1. Определение и классификация коррозионных процессов
- •8.2. Химическая коррозия
- •8.3. Электрохимическая коррозия
- •8.4. Возможность коррозии с водородной и кислородной деполяризацией
- •8.5. Защита металлов от коррозии
- •8.6. Решение типовых задач
- •8.7. Задачи для самостоятельного решения
- •Тема 9. Органические полимерные материалы
- •9.1. Классификация полимерных (высокомолекулярных) материалов
- •9.2. Строение полимеров
- •9.3. Кристаллическое и аморфное состояние полимеров
- •9.4. Методы получения полимеров
- •9.5. Применение полимеров
- •Тема 10. Химическая идентификация и анализ вещества
- •10.1. Химическая идентификация вещества
- •Некоторые реагенты для идентификации катионов
- •Классификация анионов по окислительно-восстановительным свойствам
- •Некоторые реагенты для идентификации анионов
- •10.2. Количественный анализ. Химические методы анализа
- •10.3. Инструментальные методы анализа
- •Приложение
- •Важнейшие единицы си и их соотношение с единицами других систем
- •Приставки для дольных и кратных единиц си
- •Термодинамические характеристики некоторых веществ при 298 к
- •Стандартные потенциалы металлических
- •Энергия разрыва связи
- •Электроотрицательность элементов по Полингу
- •Стандартные окислительно-восстановительные потенциалы элементов
- •Растворимость соединений
- •Обозначения: р – растворимый, м – малорастворимый, н – нерастворимый,
- •Константы диссоциации Кд слабых электролитов
- •Распределение электронов в атоме
- •Список литературы
- •Крепышева Ирина Вадимовна
- •Учебное пособие для самостоятельной работы студентов
- •Нехимических специальностей и направлений
4.6. Смещение химического равновесия. Принцип Ле Шателье
Если система находится в состоянии равновесия, то она будит пребывать в нем до тех пор, пока внешние условия сохраняются постоянными.
Наибольшее значение имеют случаи нарушения равновесия вследствие изменения концентрации какого – либо из веществ, участвующих в равновесии, давления или температуры.
Рассмотрим каждый из этих случаев.
При увеличении концентрации какого-либо вещества, участвующего в равновесии, равновесие смещается в сторону расхода этого вещества; при уменьшении концентрации какого-либо вещества равновесие смещается в сторону образования этого вещества.
Например, для реакции
![]()
Введем в систему дополнительно некоторое количество водорода. Согласно закону действия масс, увеличение концентрации водорода повлечет за собой увеличение скорости прямой реакции – реакции синтеза HI, тогда как скорость обратной реакции не изменится. В прямом направлении реакция будет теперь протекать быстрее, чем в обратном, т.е. равновесие смещается вправо, т.е. в направлении течения прямой реакции. При обратном изменении концентраций говорят о смещении равновесия влево – в направлении обратной реакции.
2. При увеличении давления путем сжатия системы равновесие смещается в сторону уменьшения числа молекул газов, т.е. в сторону понижения давления; при уменьшении давления равновесие сдвигается в сторону возрастания числа молекул газов, т.е. в сторону увеличения давления.
Для реакции
![]()
увеличение давления должно смещать равновесие вправо (слева число моль газов равно 3, справа – 2).
В том случае, когда реакция протекает без изменения числа молекул газов, равновесие не нарушается при сжатии или при расширении системы. Например, в системе
![]()
равновесие не нарушается при изменении объема; выход HI не зависит от давления.
3. При повышении температуры равновесие смещается в направлении эндотермической, а при понижении – в направлении экзотермической реакции.
Так, синтез аммиака представляет собой экзотермическую реакцию (ΔН<0)
![]()
Поэтому при
повышении температуры равновесие в
системе
![]() сдвигается влево – в сторону разложения
аммиака, так как этот процесс идет с
поглощением теплоты.
сдвигается влево – в сторону разложения
аммиака, так как этот процесс идет с
поглощением теплоты.
Наоборот, синтез оксида азота (II) представляет собой эндотермическую реакцию (ΔН > 0)
![]()
Поэтому при
повышении температуры равновесие в
системе
![]() сдвигается вправо в сторону образования
NO.
сдвигается вправо в сторону образования
NO.
Закономерности, которые проявляются в рассмотренных примерах нарушения химического равновесия, представляют собой частные случаи общего принципа Ле Шателье:
Если на систему, находящуюся в равновесии, оказать какое-либо воздействие, то в результате протекающих в ней процессов равновесие сместится в таком направлении, что оказанное воздействие уменьшится.
Гетерогенное химическое равновесие также подчиняется принципу Ле Шателье, но твердые исходные вещества и продукты реакции не влияют на смещение гетерогенного химического равновесия.
4.7. Решение типовых задач
Пример 1. Вычислить равновесные концентрации водорода и йода, если известно, что их начальные концентрации составляли по 0,02 моль/л, а равновесная концентрация НI – 0,03 моль/л. Вычислить константу равновесия.
Решение. Из уравнения реакции
![]()
видно, что на образование 0,03 моля НI расходуется 0,015 моля водорода и столько же йода, следовательно, их равновесные концентрации равны и составляют 0,02 - 0,015 = 0,005 моль/л, а константа равновесия
![]() .
.
Пример 2.
В системе
![]() равновесные концентрации веществ
равновесные концентрации веществ![]() =0,3
моль/л,
=0,3
моль/л,![]() =0,2
моль/л и
=0,2
моль/л и![]() =1,2
моль/л. Вычислить константу равновесия
системы и начальные концентрации хлора
и окиси углерода.
=1,2
моль/л. Вычислить константу равновесия
системы и начальные концентрации хлора
и окиси углерода.
Решение. Из
уравнения реакции видно, что для
образования 1,2 моля
![]() расходуется по 1,2 моля
расходуется по 1,2 моля![]() и
и![]() .
Следовательно, исходная концентрация
хлора 0,3 + 1,2 = 1,5 моль/л, окиси углерода
0,2 + 1,2 = 1,4 моль/л. Константа равновесия
.
Следовательно, исходная концентрация
хлора 0,3 + 1,2 = 1,5 моль/л, окиси углерода
0,2 + 1,2 = 1,4 моль/л. Константа равновесия
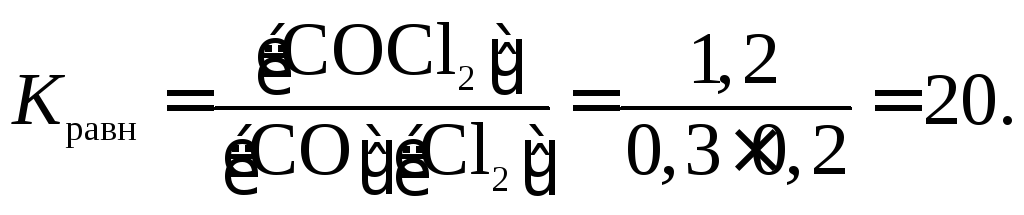
Пример 3. Во сколько раз возрастет скорость реакции взаимодействия оксида углерода (II) с кислородом, если концентрации исходных веществ увеличить в три раза?
Решение. 1) Записываем уравнение реакции:
![]()
Согласно закону действующих масс
![]()
2) Обозначим
![]() ,
тогда:
,
тогда:![]()
3) При повышении концентрации исходных веществ в 3 раза получим:
![]() ,
а
,
а
![]()
4) Рассчитываем
скорость реакции
![]() :
:
![]() ,
а
,
а
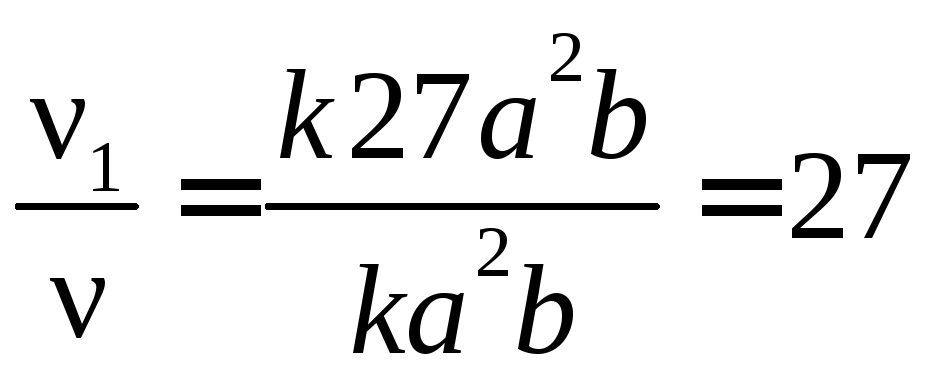 ,
т.е. скорость реакции возрастет в 27 раз.
,
т.е. скорость реакции возрастет в 27 раз.
Пример 4. Во сколько раз возрастет скорость химической реакции при повышении температуры на 40˚С, если температурный коэффициент скорости реакции равен 3?
Решение. Согласно правилу Вант – Гоффа:
![]()
![]() ,
т.е. скорость реакции возрастет в 81 раз.
,
т.е. скорость реакции возрастет в 81 раз.
Пример 5. Реакция при температуре 30˚С протекает за 2 минуты. За сколько времени закончится эта реакция при температуре 60˚С, если температурный коэффициент скорости равен 2?
Решение. 1) В соответствии с правилом Вант – Гоффа:
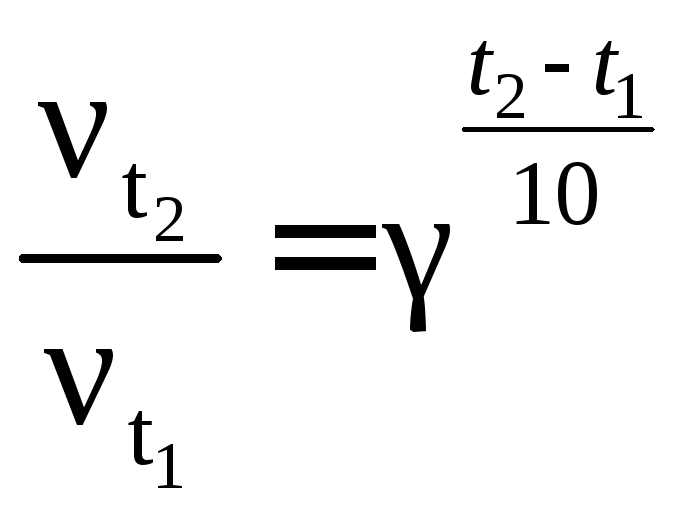
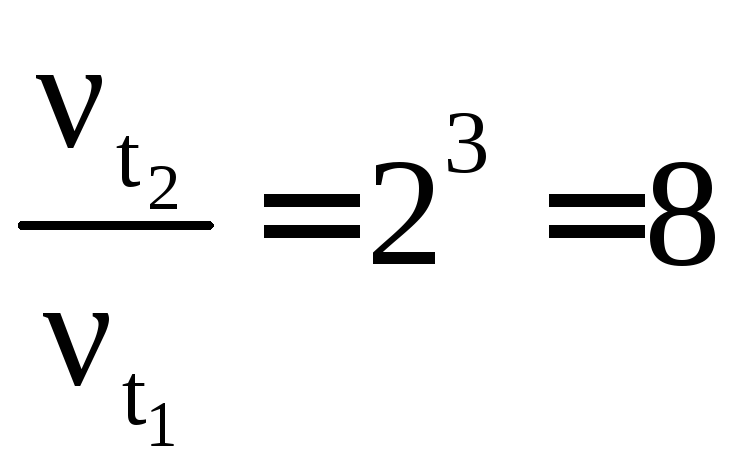
2) Скорость реакции обратно пропорциональна времени реакции, следовательно:
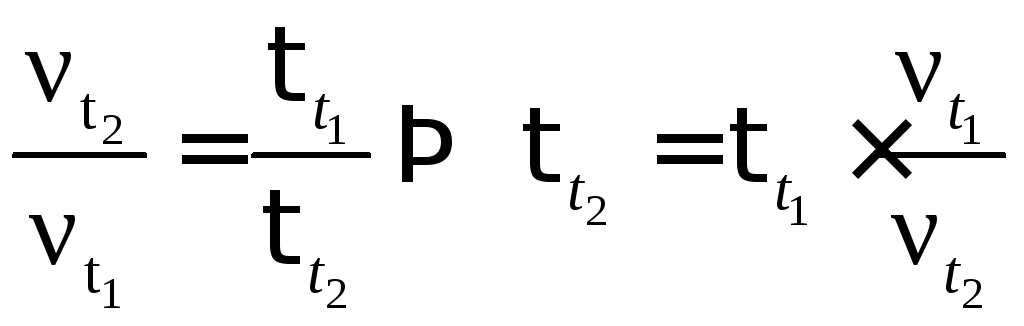
![]()
Пример 6. Реакция образования оксида азота (IV) выражается уравнением
![]() .
.
Как изменится скорость прямой и обратной реакций, если увеличить давление в 3 раза, а температуру оставить постоянной? Вызовет ли это изменение скорости смещение равновесия?
Решение. Пусть до увеличения давления равновесные концентрации оксида азота (II), кислорода и оксида азота (IV) были: [NO] = a, [O2] = b,
[NO2] = c, тогда скорость прямой реакции
![]() ,
,
скорость обратной реакции
![]() .
.
При увеличении давления в 3 раза во столько же раз увеличатся концентрации всех реагентов: [NO] = 3a, [O2] = 3b, [NO2] = 3c.
Скорость прямой реакции станет:
![]()
Скорость обратной реакции станет:
![]() .
.
Скорость прямой реакции возросла в 27 раз, а обратной – в 9 раз. Равновесие сместится в сторону прямой реакции, что согласуется с принципом Ле Шателье.
Пример 7. Как влияют на равновесие в системе
![]() ,
(ΔН<0)
,
(ΔН<0)
а) понижение давления;
б) повышение температуры;
в) увеличение концентрации исходных веществ?
Решение. Согласно принципу Ле Шателье понижение давления приведет к смещению равновесия в сторону реакции, приводящей к увеличению ее объема, т.е. в сторону обратной реакции. Повышение температуры приведет к смещению равновесия в сторону эндотермической реакции, т.е. в сторону обратной реакции. И, наконец, увеличение концентрации исходных веществ приведет к смещению равновесия в сторону образования продуктов реакции, т.е. в сторону прямой реакции.
Пример 8. Рассмотрим химическое равновесие
![]()
Определим равновесные концентрации NH3 для двух равновесных смесей:
1. [N2] = 0,1 M и [H2] = 0,1 M.
2. [N2] =1,0 M и [H2] = 0,1 M.
Константа равновесия К = 6,0 ∙ 10-2 при 525 ˚С
Решение. Составим выражение для константы химического равновесия, подставим в него известные величины и произведем вычисления.
Первый вариант химического равновесия:

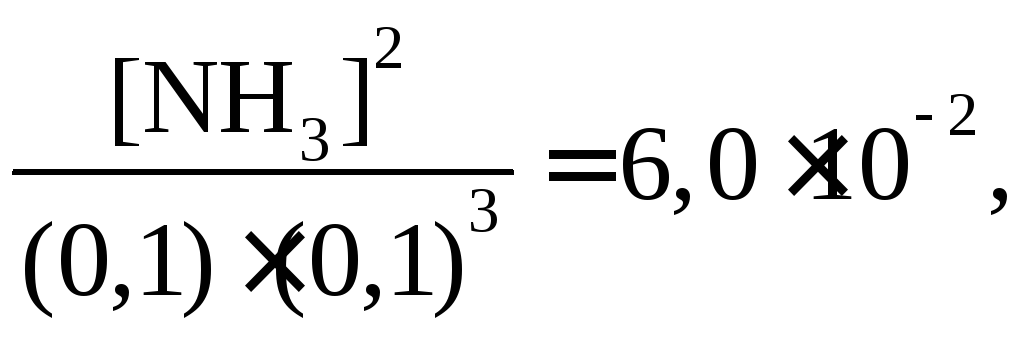 откуда
откуда
![]()
Второй вариант химического равновесия
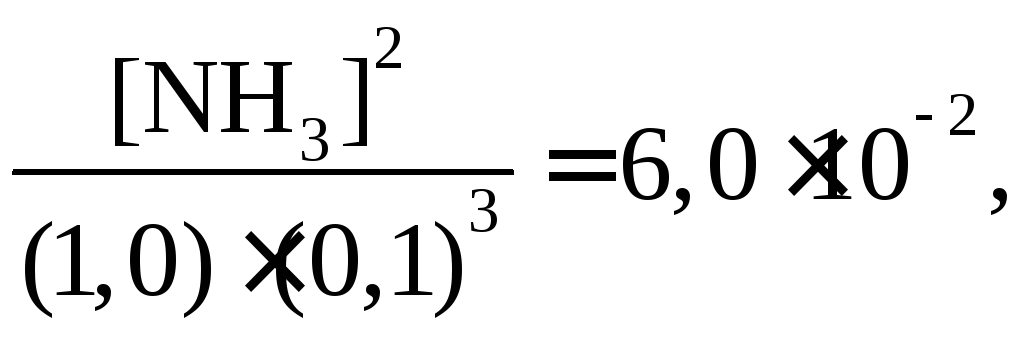 откуда
откуда
![]()
Вывод. При увеличении в равновесной смеси концентрации N2 (реагента) повышается концентрация NH3 (продукта реакции).
