
- •И. В. Крепышева
- •Содержание
- •Тема 7. Химия металлов 125
- •1.2. Квантово-механическая модель атома водорода
- •1.3. Строение многоэлектронных атомов
- •1.4. Периодическая система элементов д.И. Менделеева
- •1.5. Периодические свойства элементов
- •1.6. Решение типовых задач
- •1.7. Задачи для самостоятельного решения
- •Тема 2. Химическая связь
- •2.1. Ковалентная связь
- •2.2. Гибридизация атомных орбиталей
- •2.3. Ионная химическая связь
- •2.4. Металлическая связь
- •2.5. Водородная связь
- •2.6. Строение твердого тела
- •Тема 3. Элементы химической термодинамики
- •3.1. Основные понятия термодинамики
- •3.2. Внутренняя энергия
- •3.3. Энтальпия
- •3.4. Термохимия. Закон Гесса
- •3.5. Энтропия
- •3.6. Самопроизвольные процессы. Энергия Гиббса
- •3.7. Решение типовых задач
- •3.8. Задачи для самостоятельного решения
- •Тема 4. Химическая кинетика и химическое равновесие
- •4.1. Скорость химической реакции
- •4.2. Зависимость скорости химической реакции от концентрации реагирующих веществ
- •4.3. Зависимость скорости реакции от температуры
- •4.4. Катализ
- •4.5. Химическое равновесие
- •4.6. Смещение химического равновесия. Принцип Ле Шателье
- •4.7. Решение типовых задач
- •4.8. Задачи для самостоятельного решения
- •Тема 5. Растворы. Дисперсные системы
- •5.1. Общие свойства растворов
- •5.2. Способы выражения состава растворов
- •5.3. Теория электролитической диссоциации
- •5.4. Теории кислот и оснований
- •5.5. Ионные реакции в растворах
- •5.6. Ионное произведение воды. Водородный показатель рН
- •5.7. Гидролиз солей
- •5.8. Дисперсные системы и их классификация
- •5.9. Решение типовых задач
- •28,57 Г соли растворены в 71,43 г воды
- •3% Массы раствора составляют 48,84 г
- •Соотношение между рН и рОн
- •5.10. Задачи для самостоятельного решения
- •Тема 6. Окислительно-восстановительные электрохимические процессы
- •6.1. Основные понятия
- •Правила определения степени окисления
- •6.2. Составление уравнений окислительно-восстановительных реакций
- •6.3. Влияние среды на характер протекания реакций
- •6.4. Важнейшие окислители и восстановители
- •6.5. Электрохимические процессы
- •96500 Кл (26,8 а∙ч) – 31,77 г Cu (масса моля эквивалентов)
- •96500 Кл – 1 г (11,2 л– объем моля эквивалентов)
- •6.6. Гальванический элемент Даниэля-Якоби
- •6.7. Окислительно-восстановительные потенциалы
- •6.8. Эдс окислительно-восстановительных реакций
- •6.9. Электролиз расплавов и растворов солей
- •6.10. Некоторые области применения электрохимии
- •6.11. Решение типовых задач
- •6.12. Задачи для самостоятельного решения
- •Тема 7. Химия металлов
- •7.1. Общая характеристика металлов
- •7.2. Химические свойства металлов
- •7.3. Взаимодействие металлов с кислотами
- •Взаимодействие металлов с соляной кислотой.
- •Взаимодействие металлов с азотной кислотой
- •Взаимодействие металлов с серной кислотой
- •7.4. Сплавы
- •7.5. Получение металлов
- •Тема 8. Коррозия и защита металлов
- •8.1. Определение и классификация коррозионных процессов
- •8.2. Химическая коррозия
- •8.3. Электрохимическая коррозия
- •8.4. Возможность коррозии с водородной и кислородной деполяризацией
- •8.5. Защита металлов от коррозии
- •8.6. Решение типовых задач
- •8.7. Задачи для самостоятельного решения
- •Тема 9. Органические полимерные материалы
- •9.1. Классификация полимерных (высокомолекулярных) материалов
- •9.2. Строение полимеров
- •9.3. Кристаллическое и аморфное состояние полимеров
- •9.4. Методы получения полимеров
- •9.5. Применение полимеров
- •Тема 10. Химическая идентификация и анализ вещества
- •10.1. Химическая идентификация вещества
- •Некоторые реагенты для идентификации катионов
- •Классификация анионов по окислительно-восстановительным свойствам
- •Некоторые реагенты для идентификации анионов
- •10.2. Количественный анализ. Химические методы анализа
- •10.3. Инструментальные методы анализа
- •Приложение
- •Важнейшие единицы си и их соотношение с единицами других систем
- •Приставки для дольных и кратных единиц си
- •Термодинамические характеристики некоторых веществ при 298 к
- •Стандартные потенциалы металлических
- •Энергия разрыва связи
- •Электроотрицательность элементов по Полингу
- •Стандартные окислительно-восстановительные потенциалы элементов
- •Растворимость соединений
- •Обозначения: р – растворимый, м – малорастворимый, н – нерастворимый,
- •Константы диссоциации Кд слабых электролитов
- •Распределение электронов в атоме
- •Список литературы
- •Крепышева Ирина Вадимовна
- •Учебное пособие для самостоятельной работы студентов
- •Нехимических специальностей и направлений
3.6. Самопроизвольные процессы. Энергия Гиббса
Процессы, протекающие без подвода энергии от внешнего источника, называются самопроизвольными. Например, образование ржавчины, реакция натрия с водой, растворение соли в воде и др.
Выясним критерии самопроизвольных процессов.
Большинство экзотермических реакций (
 <0)
протекают самопроизвольно. Однако
существуют и эндотермические процессы,
которые протекают самопроизвольно
(растворение солей KCl
и NH4NO3
в воде), следовательно,
<0)
протекают самопроизвольно. Однако
существуют и эндотермические процессы,
которые протекают самопроизвольно
(растворение солей KCl
и NH4NO3
в воде), следовательно,
 <0
-
не критерий самопроизвольного процесса.
<0
-
не критерий самопроизвольного процесса.Кроме уменьшения
 имеется другая движущая сила
самопроизвольного процесса - это
стремление частиц (молекул, ионов,
атомов) к беспорядочному движению.
имеется другая движущая сила
самопроизвольного процесса - это
стремление частиц (молекул, ионов,
атомов) к беспорядочному движению.
Энтропийный и энтальпийный факторы, взятые по отдельности, не могут быть критериями самопроизвольного течения химических реакций.
Для изобарно – изотермических процессов их объединяет функция, называемая энергией Гиббса:
![]() ,
(1)
,
(1)
а в общем случае
![]() ,
(2)
,
(2)
Эти уравнения
позволяют вычислить
![]() любой химической реакции, если известны
любой химической реакции, если известны![]() и
и
![]() .
.
Стандартные энергии
Гиббса
![]() ,
энтальпии образования
,
энтальпии образования![]() и энтропии
и энтропии![]() приводятся в справочных таблицах, в
которых
приводятся в справочных таблицах, в
которых![]() и
и![]() элементарных веществ в стандартном
состоянии условно принимаются равными
нулю.
элементарных веществ в стандартном
состоянии условно принимаются равными
нулю.
Как уже было
упомянуто, движущая сила химической
реакции определяется ее энергией Гиббса
![]() .
.![]() представляет энтальпийный, а
представляет энтальпийный, а![]() - энтропийный фактор. Первый из них
отражает тенденцию системы к образованию
связей в результате взаимного притяжения
частиц – молекул или атомов, что приводит
к их усложнению, а второй – тенденцию
к усилению процессов диссоциации сложных
частиц на более простые и их менее
упорядоченному состоянию. Оба фактора
обычно действуют в противоположных
направлениях, и общее направление
реакции определяется влиянием
преобладающего фактора.
- энтропийный фактор. Первый из них
отражает тенденцию системы к образованию
связей в результате взаимного притяжения
частиц – молекул или атомов, что приводит
к их усложнению, а второй – тенденцию
к усилению процессов диссоциации сложных
частиц на более простые и их менее
упорядоченному состоянию. Оба фактора
обычно действуют в противоположных
направлениях, и общее направление
реакции определяется влиянием
преобладающего фактора.
Энергия Гиббса служит критерием самопроизвольного протекания химической реакции при изобарно – изотермических процессах.
Химическая
реакция принципиально возможна, если
энергия Гиббса уменьшается, т.е.
![]() <0.Чем
больше отрицательное значение энергии
Гиббса, тем полнее идет процесс. Уменьшение
энергии Гиббса является условием
возможности самопроизвольного течения
реакции в прямом направлении.
<0.Чем
больше отрицательное значение энергии
Гиббса, тем полнее идет процесс. Уменьшение
энергии Гиббса является условием
возможности самопроизвольного течения
реакции в прямом направлении.
Химическая
реакция не может протекать самопроизвольно,
если энергия Гиббса системы возрастает,
т.е.
![]() >0.
Увеличение энергии Гиббса является
условием невозможности самопроизвольного
течения реакции в прямом направлении,
а также служит термодинамическим
условием возможности самопроизвольного
протекания обратной реакции.
>0.
Увеличение энергии Гиббса является
условием невозможности самопроизвольного
течения реакции в прямом направлении,
а также служит термодинамическим
условием возможности самопроизвольного
протекания обратной реакции.
Наконец,
если
![]() =0,
то реакция может протекать как в прямом,
так и в обратном направлениях, т.е.
реакция обратима.
=0,
то реакция может протекать как в прямом,
так и в обратном направлениях, т.е.
реакция обратима.
Поскольку энергию Гиббса можно превратить в работу, то её также называют свободной энергией.
Если T → 0, то ΔG → ΔH. Таким образом, при низких температурах величина и знак ΔG определяются величиной и знаком ΔH. При низких температурах самопроизвольно протекают, как правило, экзотермические реакции.
Если T → , то ΔG → TΔS. При высоких температурах величина и знак ΔG определяются величиной и знаком ΔS. При высоких температурах самопроизвольно протекают, как правило, реакции, ведущие к увеличению энтропии.
Таким образом, процессы в закрытой системе идут самопроизвольно в сторону понижения энергии Гиббса (ΔG = 0), что дает возможность установить границу, позволяющую судить о начале развития реакции в нужном направлении.
Для этого в
уравнении:
![]() полагаем,
полагаем,![]() следовательно,
следовательно, ![]() и
и 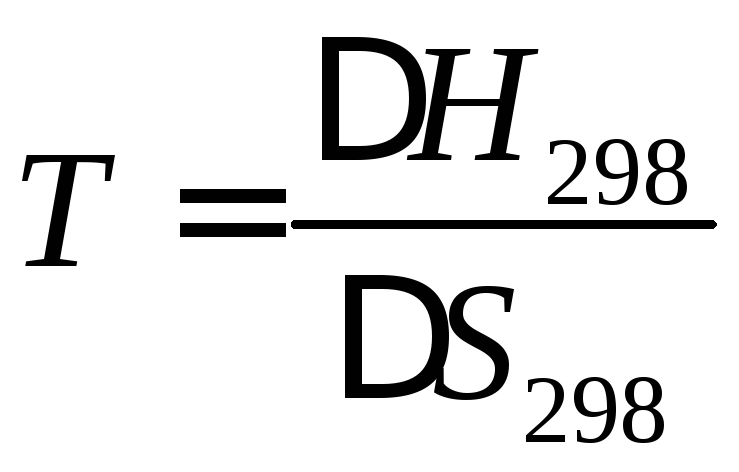 – температура при которой
– температура при которой ![]() .
.
Изменение энергии Гиббса системы при образовании 1 моль вещества из простых веществ, устойчивых при 298 К, называется энергией Гиббса образования вещества. Если исходные вещества и продукты реакции находятся в стандартных состояниях, то энергия Гиббса называется стандартной энергией Гиббса химической реакции ΔG0 и является критерием самопроизвольного протекания реакции.
Используя закон Гесса, энергию Гиббса можно рассчитать как сумму энергий Гиббса образования продуктов реакции за вычетом энергий Гиббса образования исходных веществ с учетом стехиометрических коэффициентов:
ΔG = ∑nkΔGобр - ∑nнΔGобр.
