
Ко 2 сессии / Малашонок Неорганическая химия
.pdf
КНF2 ¾¾®to КF + НF
Катод  2HF + 2e– = H2 + 2F– Анод Å 2F– – 2e – = F2
2HF + 2e– = H2 + 2F– Анод Å 2F– – 2e – = F2
Получение фтора и работа с ним осложняются из-за его высокой реакционной способности. Материалами, обладающими химической стойкостью по отношению к фтору, являются сталь, медь и сплавы никель-медь. Их устойчивость в атмосфере фтора объясняется тем, что под действием фтора их поверхность покрывается слоем нерастворимых фторидов.
В лаборатории F2 получают разложением фторидов:
CoF = CoF + ½F
3 2 2
В промышленности Cl2 получают электролизом концентрированных водных растворов хлорида натрия:
2NaCl + 2H2O  2NaOH + H2- + Cl2-
2NaOH + H2- + Cl2-
Катод  2Н2О + 2е– = Н2 + 2ОН– Анод Å 2Сl– – 2 е– = Сl2
2Н2О + 2е– = Н2 + 2ОН– Анод Å 2Сl– – 2 е– = Сl2
На угольном аноде выделяется хлор, а на стальном катоде – водород. Поскольку в катодном пространстве остаются ионы натрия, не восстанавливающиеся в условиях процесса, и присутствуют гидро- ксид-ионы, образующиеся в процессе восстановления воды, то происходит накопление водного раствора щелочи NaOH – третьего товарного продукта. При получении хлора катод может быть изготовлен из ртути. В этом случае в катодном пространстве образуется особенно чистый водный раствор гидроксида натрия, но поскольку при этом возможны потери ртути, то такой способ получения хлора является экологически небезопасным.
В лаборатории Cl2 получают действием концентрированной соляной кислоты на окислители (KMnO4, MnO2, PbO2 и др.), разложением некоторых хлоридов:
16HCl + 2KMnO4 ® 5Cl2 + 2MnCl2 + 2KCl + 8H2O
MnO 4− + 8Н+ + 5е– = Mn2+ + 4Н2О; ЕO |
− |
|
Mn |
2+ = 1,51 В |
||||
|
||||||||
|
|
|
|
MnO |
4 |
|
|
|
Cl2 |
+2е– = 2Сl– ; ЕO |
|
Cl |
− = 1,36 В |
|
|||
|
|
|||||||
|
Cl2 |
|
|
|
|
|
|
|
11

4HCl + MnO2 → Cl2 + MnCl2 + 2H2O
PbO2 + 4HCl → PbCl2 + Cl2 + 2H2O 2AuCl3 → 2Au + 3Cl2
Окислительная способность галогенов с увеличением заряда ядра уменьшается, о чем свидетельствует уменьшение значений стандартных электродных потенциалов процессов Э2 + 2е– = 2Э– (табл.1.2). Галогены, расположенные выше в подгруппе, вытесняют из галогенидов расположенные ниже галогены.
Бром и иод в промышленности получают из бромидов и иодидов вытеснением хлором:
2KBr + Cl2 → 2KCl + Br2
2KI + Cl2 → 2KCl + I2
путем электролиза водных растворов бромидов и иодидов:
2NaI + 2H2O  2NaOH + H2− + I2
2NaOH + H2− + I2
Иод встречается в природе также в виде иодатов, из иодатов I2 получают восстановлением:
5NaHSO3 + 2NaIO3 = 2Na2SO4 + 3NaHSO4 + I2 + H2O
Br2 и I2 могут быть получены в лаборатории при окислении га- логенид-ионов неорганическими окилителями:
K2Cr2O7 + 6KBr + 7H2SO4 = 2Cr2(SO4)3 + 4K2SO4 + 3Br2 + 7H2O 8NaI + 5H2SO4 (конц. ) = Na2SO4 + 4I2 + H2S + 4H2O
4КI + 2СuSO4 = 2СuI + I2 + 2К2SO4
Химические свойства галогенов
Галогены обладают большим сродством к электрону и являются сильными окислителями. Окислительные свойства их возрастают от йода к фтору. Они активно взаимодействуют почти со всеми элементами периодической системы.
Фтор реагирует со всеми металлами и неметаллами, кроме He, Ne, Ar. Реакции протекают очень бурно, часто сопровождаются взрывом, образуются соединения, в которых элементы, как правило, находятся в высшей степени окисления, например:
2Na + F2 = 2NaF (на холоду)
2Au + 3F2 = 2AuF3
12
5P + 5F2 = 2PF5
3F2 + S → SF6
F2 + Xe → XeF6
Фтор при обычной температуре не взаимодействует с некоторыми металлами (Fe, Cu, Ni, A1, Zn), на поверхности этих металлов образуется защитная фторидная пленка.
В виде порошка железо горит в хлоре без предварительного нагревания, компактное железо реагирует при нагревании:
2Fe + 3Cl2 ¾t ® 2FeCl3
Однако в отсутствие воды на поверхности металлов может образоваться плотная солевая пленка, предохраняющая металл от разрушения, поэтому сжиженный сухой хлор перевозят в стальных баллонах. С помощью сухого хлора извлекают олово из отходов белой жести, используемой главным образом для приготовления консервных банок. Сухой хлор не реагирует с железом, но взаимодействует с оловом, образуя жидкий SnС14.
С неметаллами:
2P + 3Cl2(недост.) ¾t ® 2PCl3 2P + 5Cl2(изб.) ¾t ® 2PCl5 2Cl2 + S → SCl4
Активность брома и йода значительно ниже, но и они со многими металлами и неметаллами могут реагировать при обычных условиях:
2А1 + 3I2 = 2А1I3 (Н2О – катализатор)
2P + 3Br2 = 2PBr3
2P + 3I2 = 2PI3 (при нагревании)
Галогены вступают в реакцию с водородом, образуя соединения НГ: Н2 + Г2 = 2НГ
Фтор взаимодействует с водородом с взрывом, выделяя при этом большое количество энергии. Хлор при обычных условиях очень медленно взаимодействует с водородом, но на прямом солнечном свету или при нагревании реакция идет также с взрывом. Реакция водорода и хлора протекает по цепному механизму, поэтому для нее необходимо инициирование (нагревание или освещение):
Н2 + Сl2 ¾¾®hν 2НCl
13
Взаимодействие брома и йода с водородом происходит лишь при нагревании. Йод с водородом реагирует незначительно, так как образующийся в условиях синтеза иодоводород легко разлагается, и равновесие сильно смещено в сторону исходных веществ. Поэтому лишь НCl в промышленности получают из простых веществ.
Азот и кислород непосредственно с галогенами не взаимодействуют. Лишь фтор взаимодействует с кислородом в тлеющем разряде, образуя при низких температуpax фториды кислорода: O2F2, O3F2 и другие.
Взаимодействие с водой. Фтор энергично разлагает воду, продукты реакции зависят от температуры:
(H2O) + F2 = HF + O2 (> 90оС с водяным паром – с взрывом)
{2Н2О} + 2F2 = 4НF + ОF2↑ (при 0 – 90 оС)
Фтор активно взаимодействует со спиртом, ацетоном, бензолом. Поэтому эти вещества не могут быть использованы в качестве растворителей фтора.
Хлор, бром и иод растворяются в воде, причем их растворимость в воде при 20° С характеризуется следующими значениями, моль/л: хлор – 0,103, бром – 0,225, то есть растворимость брома несколько выше растворимости хлора. Растворимость иода в воде значительно меньше – 0,0013 моль/л. При низких температурах можно выкристаллизовать гидраты хлора и брома, имеющие состав Г2 ·6–8 Н2О. Растворы хлора и брома в воде носят название хлорной и бромной воды. Эти растворы обладают всеми свойствами хлора и брома соответственно. Их окислительные свойства превосходят окислительные свойства сухих хлора и брома. Это объясняется тем, что в водных растворах галогенов (за исключением фтора) происходят реакции диспропорционирования, например для хлора при стандартных условиях:
Cl2 + Н2О НClО + НCl |
(1) |
При переходе от хлора к иоду равновесие (1) в системе все больше смещается в сторону исходных веществ, о чем свидетельствуют константы равновесий данных реакций:
Галоген |
С12 |
Br2 |
I2 |
Константа равновесия |
4 10– 4 |
7 10– 9 |
2 10– 13 |
Как видно из приведенных значений констант равновесия, равновесие (1) существенно смещено влево и, наряду с продуктами взаимо-
14
действия галогенов с водой, в растворах галогенов преимущественно присутствуют молекулярные формы галогенов.
Бактерицидное действие водных растворов хлора связано как с образованием атомарного кислорода, образующегося при разложении НClО, так и с хлорирующим действием хлорноватистой кислоты. Образующаяся в хлорированной воде соляная кислота безвредна, поэтому вода пригодна для употребления.
Растворимость I2 в воде можно повысить, если добавить к ней КI. В результате образуется красно-бурый раствор хорошо растворимых (но нестойких) полииодидов калия (КI3 и др.):
nI2 + КI = КI2n + 1 (n = 1 ÷ 7)
Бром и йод лучше растворяются в органических растворителях. Это свойство брома и йода используется в качественном анализе.
Взаимодействие со щелочами. При взаимодействии фтора со щелочами продукты реакции зависят от концентрации щелочи:
2F2 + 2NaOH(разб) → 2NaF + OF2 + H2O
2F2 + 4NaOH(конц) → 4NaF + O2 + 2H2O
Продукты взаимодействия хлора со щелочами зависят от температуры:
Сl2 + 2KОН → KСlО + KСl + Н2О 3Сl2 + 6KОН ¾t ® KСlО3 + 5KСl + 3Н2О
Раствор, полученный при пропускании хлора через раствор гидроксида натрия, называют "жавелевой водой". Он обладает окислительными свойствами и применяется для отбеливания тканей, бумаги и т.д. Отбеливающее действие "жавелевой воды" связано с поглощением ею углекислого газа из воздуха, который переводит гипохлоритионы в молекулы слабой хлорноватистой кислоты:
NaС1О + СО2 + H2O NaНСО3 + НС1О
С1О– + СО2 + H2O НСО3- + НС1О
Молекулы хлорноватистой кислоты неустойчивы и легко отщепляют кислород, который отбеливает материал, окисляя окрашенные примеси.
При взаимодействии хлора с гашеной известью Ca(OH)2 образуется хлорная (белильная) известь CaOCl2:
C12 + Ca(OH)2 → CaOCl2 + H2O
15
Хлорную известь можно рассматривать как смешанную соль соляной и хлорноватистой кислот или смесь СаС12, Са(С1О)2 и Са(ОН)2. Хлорная известь можно представить в виде смешанной соли:
При взаимодействии щелочи с I2 не образуется NaIO, образуется
NaIO3:
6I2 + 12NaOH → 10NaI + 2NaIO3 + 6H2O
Взаимодействие с сероводородом. Галогены способны отнимать водород от других веществ:
H2S + Br2 = S + 2HBr
Реакция замещения водорода в предельных углеводородах: CH4 + Cl2 ¾¾®hν CH3Cl + HCl.( радикальный механизм)
Реакция присоединения к непредельным углеводородам:
C2H4 + Cl2 = C2H4Cl2
В ряду Cl2 – Br 2 – I 2 – неметаллические свойства ослабевают, что связано с увеличением размера атома. У I2 появляются приметы металлических свойст. I2, реагирует с концентрированной HNO3, в неводном растворе образует катион I+:
I2 + 10HNO3 конц. → 2HIO3 + 10NO2 + 4H2O I2 + AgNO3 ¾эфир¾¾® AgI + INO3
Для иода характерна особая реакция – он соединяется с крахмалом с образованием синего продукта:
(С6Н10 O5)n +I2 (С6Н10 O5)n · I2
белый синий
При нагревании равновесие смещается влево, и синяя окраска исчезает. Крахмал применяется как индикатор дли обнаружения иода, присутствующего в малых концентрациях.
Особенности химии фтора. Фтор в реакциях проявляет только окислительные свойства, в соединениях имеет единственную степень окисления –1. Фтор реагирует со сложными веществами, в нем горит
H2O, песок (SiO2):
SiO2 + 2F2 → Si+4F4 + O2
16
Эта реакция происходит вследствие того, что тетрафторид кремния более прочное соединение, чем оксид. НOf , 298 SiO2 = –910,9 кДж/моль, а
НOf , 298 SiF4 = –1614,9 кДж/моль, кроме того, реакция сопровождается увеличением энтропии.
Галогеноводороды
Получение галогеноводородов. HF не получают взаимодействи-
ем простых веществ (реакция H2 + F2 = 2HF протекает со взрывом). Получают фтороводород из фторидов:
СaF2 + H2SO4 → CaSO4↓ + 2HF↑ KHF2 ¾t ® KF + HF
В промышленности HCl получают взаимодействием простых веществ, хлорированием углеводородов:
Н2 + Сl2 ¾¾®hν 2НCl CH4 + Cl2 ¾¾®hν CH3Cl + НСl
В лаборатории HCl получают взаимодействием концентрированной серной кислоты на твердые хлориды, гидролизом кислотных галогенидов
NaCl(тверд.) + Н2SO4 (конц.) ¾t ® NaНSO4 +НСl
BCl3 + H2O → H3BO3 + HCl↑
HI и HBr нельзя получить реакциями обменного взаимодействия соответствующих галогенидов с концентрированной серной кислотой, поскольку восстановительные свойства бромоводорода и иодоводорода более ярко выражены, протекает окислительно-восстановительная реакция с образованием различных продуктов:
2NaBr + 2H2SO4 → Br2 + SO2 + Na2SO4 + 2H2O
8NaI + 5H2SO4 → 4I2 + H2S + 4Na2SO4 + 4H2O HBr и HI получают гидролизом галогенидов фосфора:
PBr5 + 4H2O → H3PO4 + 5HBr-
PBr3 + 3H2O → 3HBr↑+ H3PO3-
PI3 + 3H2O → H3PO3 + 3HI
17
При стандартных условиях галогеноводороды - газообразные вещества с резким запахом, хорошо растворимые в воде. Водные растворы галогеноводородов являются кислотами.
Характеристика галогеноводородов
|
|
HF |
HCl |
HBr |
HI |
Длина связи, нм |
0,092 |
0,128 |
0,141 |
0,160 |
|
|
|
|
длина связи увеличивается |
|
|
Энергия |
связи, |
565 |
431 |
304 |
297 |
кДж/моль |
|
|
|
|
|
|
|
|
энергия связи уменьшается |
|
|
Константа |
дис- |
6,61 · 10− 4 |
|
|
|
социации |
|
|
сильные килоты |
|
|
|
|
|
|
|
|
|
|
|
возрастает сила кислот |
|
|
Температура |
–83,35 |
–114,17 |
–86,8 |
–50,76 |
|
плавления, оС |
|
|
|
|
|
Температура |
20 |
–85 |
–66,38 |
–35,55 |
|
кипения, оС |
|
|
|
|
|
возрастает
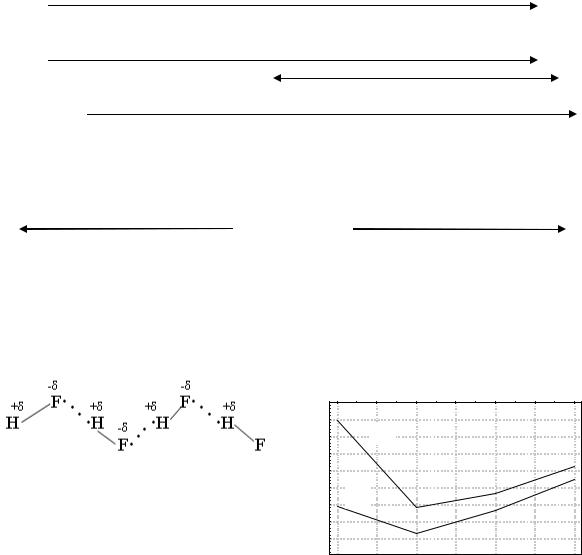
В молекулах галогеноводородов образуется ковалентная полярная связь. Общая электронная пара, за счет которой осуществляется связь, сильно смещена в сторону галогена. Особенно сильно происходит поляризация связи в HF, что обусловлено самой высокой электроотрицательностью фтора. Вследствие этого между молекулами HF образуются прочные водородные связи. Наличие водородных связей объяс
|
|
|
|
t, oC |
|
|
|
|
|
|
|
|
20 |
|
|
|
|
|
|
|
|
|
2 |
|
|
|
|
|
|
|
-20 |
|
|
|
|
няет аномально высокие темпе- |
-60 |
|
|
|
||||
ратуры |
плавления |
и |
кипения |
|
|
|
||
1 |
|
|
|
|||||
фтороводорода (рис. 1.4). От НСl |
-100 |
|
|
|
||||
к HBr и HI температуры плавле- |
-140 |
|
|
|
||||
ния и кипения монотонно увели- |
|
|
|
|||||
HF |
HCl |
HBr |
HI |
|||||
чиваются, так как с ростом мас- |
||||||||
|
Рис. 1.4. Температуры |
|
||||||
сы и размеров молекул усилива- |
|
|
||||||
ется межмолекулярное |
взаимо- |
плавления (1) и кипения (2) НГ |
||||||
действие. |
|
|
|
|
|
|
||
Жидкий HF образует цепочки, состоящие из молекул HF:- (HF)4, |
||||||||
(HF)6, (HF)8,. Вследствие наличия сильной водородной связи даже в |
||||||||
18

парах молекулы HF ассоциированы. При t = 3500ºС связь H – F разрывается.
HF может смешиваться с Н2О в неограниченном количестве, образуя слабую плавиковую кислоту, при этом между молекулами HF и Н2О также возникают водородные связи.
Безводный HF – неэлектролит, а в водном растворе возможны процессы ионизации:
HF + H2O H3O+ + F–
F– + HF HF −2
2HF + H2O H3O+ + HF −2
HF хранят в сосудах из платины или полиэтилена. В стеклянном сосуде хранить нельзя т. к. в стекле есть SiO2, и плавиковая кислота разрушает стекло:
SiO2 + 4HF = SiF4 + 2H2O (реакция травления стекла)
В избытке плавиковой кислоты образуется гексафторокремниевая кислота:
SiF4 + 2HF = H2[SiF6]
Водные растворы НCl, НBr, НI – сильные кислоты, галогенидионы проявляют восстановительные свойства, например:
4HCl- + O2 2H2O-2 + 2Cl20 (процесс Дикона)
DH оf , 298 , кДж/моль –91,8 |
0 |
–241,82 |
0 |
||
S о298 , Дж/(моль × К) |
186,8 |
205,04 |
188,72 |
222,9 |
|
DНо298 |
= –116,44 |
кДж. DS о298 = –129 Дж/К. |
|
||
DG о298 |
= DНо298 – ТDS = –77998 Дж |
|
|||
Расчет показывает, что процесс может протекать в прямом и обратном направлениях; при t < 903 К (630оС) окислитель - кислород, при более высоких – хлор. Однако при обычных условиях кислород не взаимодействует с HCl в заметной степени, для ускорения реакции смесь хлороводорода и кислорода необходимо нагревать и использовать катализатор (хлориды меди(II) и железа(III)). Ранее процесс Дикона использовали для получения хлора.
Восстановительные свойства НГ усиливаются. Иодоводород окисляется на воздухе до иодноватой кислоты:
2HI− + 3O2 → 2HI+5O3
19
Усиление восстановительных свойств НГ прослеживается в реакциях с H2SO4:
HCl + H2SO4. - реакция не идет
6HBr + H2SO4(конц). → 3Br2 + SO2 + 4H2O
8HI + H2SO4(конц) → 4I2 + H2S + 4H2O
НCl при взаимодействии с сильными окислителями окисляется до свободного хлора:
PbO2 + 4HCl → PbCl2 + Cl2 + H2O
Соляная кислота представляет собой бесцветную, дымящую на воздухе жидкость. Она проявляет свойства, характерные для кислот.
Химические свойства соляной кислоты:
|
Реагенты. Характерные реакции |
Примеры реакций |
С простыми веществами |
2HCl + Mg → MgCl2 + H2− |
|
Реагирует с металлами, расположенными в |
||
электрохимическом ряду до водорода |
2HCl + Fe → FeCl2 + H2− |
|
|
|
|
Со сложными веществами |
2HCl + CuO → CuCl2 + H2O |
|
1) |
С основными и амфотерными оксидами |
|
2) |
С основаниями и амфотерными гидро- |
2HCl + Cu(OH)2 → CuCl2 + 2H2O |
ксидами |
3HCl + Fe(OH)3 → FeCl3 + 3H2O |
|
|
|
|
3) |
С аммиаком |
HCl + NH3 → NH4Cl |
4) |
C cолями, если образуется газ, осадок |
HCl + Na2CO3 → 2NaCl + CO2↑ + H2O |
или слабый электролит |
HCl + AgNO3 → AgCl↓ + HNO3 |
|
|
|
|
|
|
2HCl + K2SiO3 → 2KCl + H2SiO3↓ |
Для HF также характерны реакции с Ме, с основными оксидами, с основаниями и некоторыми солями, например:
Zn + 2HF = ZnF2 +H2
3HF + Al(OH)3 = AlF3 +3H2O
2HF + KOH = KHF2 + H2O
NH3 +2HF = NH4HF2
Как и другие бинарные соединения выделяют фториды различной природы: основные – фториды металлов; амфотерные – фториды амфотерных элементов; кислотные – соединения фтора с неметаллами:
20
