
Ко 2 сессии / Малашонок Неорганическая химия
.pdf
Наиболее тугоплавки металлы V В и VI В групп. У них максимально возможное число неспаренных электронов, а, следовательно, наибольшее число ковалентных связей. Дальнейшее заполнение приводит к уменьшению числа ковалентных связей и падению температур плавления.
2.Вследствие незаполненности d-подуровня и наличия близких по энергии незаполненных ns- и np-подуровней, катионы d-элементов склонны к комплексообразованию; их комплексные соединения, как правило, окрашены и парамагнитны.
3.Для d-элементов характерен большой набор валентных состояний и, как следствие этого, изменение кислотно-основных и окисли- тельно-восстановительных свойств в широких пределах.
Поскольку часть валентных электронов находится на s-орбиталях, то проявляемые ими низшие степени окисления, как правило, равны +2. Исключение составляют элементы, ионы которых Э3+ и Э+ имеют устойчивые конфигурации d0, d5 и d10: Sc3+, Fe3+, Cu+, Ag+, Au+.
Соединения, в которых d-элементы находятся в низшей степени окисления, образуют кристаллы ионного типа, в химических реакциях проявляют основные свойства и являются, как правило, восстановителями.
Устойчивость соединений, в которых d-элементы находятся в высшей степени окисления (равной номеру группы), увеличивается в пределах каждого переходного ряда слева направо, достигая максимума для 3d-элементов у Mn, а во втором и третьем переходных рядах
–у Ru и Os соответственно. В пределах одной подгруппы стабильность соединений высшей степени окисления уменьшается в ряду 5d > 4d > 3d, о чем свидетельствует характер изменения значений стандартных энергий Гиббса образования однотипных соединений, например:
|
|
|
CrO3 |
MoO3 |
WO3 |
Mn2O7 |
Tc2O7 |
Re2O7 |
|
|
|
|
|
|
|
|
|
о |
, 298 |
,кДж/моль |
–506 |
–677 |
–763 |
–543,4 |
–936,3 |
–1165 |
G f |
|
|
|
|
|
|
Это явление связано с тем, что при увеличении главного квантового числа в пределах одной подгруппы происходит уменьшение разности энергий (n – 1) d- и ns-подуровней. Соединения, в которых d-элементы находятся в высших степенях окисления, имеют кислотный характер, являются окислителями (CrO3 и K2CrO4, Mn2O7,
KMnO4).
231
Соединения, в которых d-элементы находятся в промежуточных степенях окисления, проявляют амфотерные свойства и окислительновосстановительную двойственность.
Поскольку для d-элементов в пределах подгруппы устойчивость высших степеней окисления сверху вниз растет, то окислительные свойства соединений высшей степени окисления резко падают. Так, соединения хрома (VI) (CrO3, K2CrO4, K2Cr2O7) и марганца(VII) (Mn2O7, KMnO4) – сильные окислители, а WO3, Re2O7 и соли соответствующих им кислот (H2WO4, HReO4) восстанавливаются с трудом.
4.Сходство d-элементов с элементами главных подгрупп в полной мере проявляется у элементов третьей группы ns2np1 и (n – 1) d1ns2.
Свозрастанием номера группы оно уменьшается; элементы VIII А подгруппы – газы, VIII В – металлы. В первой группе снова появляется отдаленное сходство (все элементы – металлы), а элементы I В подгруппы – хорошие проводники; это сходство усиливается во второй группе, так как d-электроны Zn, Cd и Hg не участвуют в образовании химической связи.
5.d-элементы III В–VII В подгрупп в высших степенях окисления по свойствам подобны соответствующим p-элементам. Так, в высших степенях окисления Mn(VII) и Cl(VII) являются электронными аналогами. Подобие электронных конфигураций (s2p6) приводит к подобию
свойств соединений семивалентных марганца и хлора. Mn2O7 и Cl2O7 в обычных условиях малоустойчивые жидкости, являющиеся ангид-
ридами сильных кислот с общей формулой НЭО4. В низших степенях окисления марганец и хлор имеют различное электронное строение, что обусловливает резкое отличие свойств их соединений. Например,
низший оксид хлора Cl2O (s2p4) – газообразное вещество, являющееся ангидридом хлорноватистой кислоты (HClO), тогда как низший оксид марганца MnO (d5) представляет собой твердое кристаллическое вещество основного характера.
6.Восстановительная способность металла определяется не толь-
ко его энергией ионизации (М – ne– → Мn+; ∆Hоиониз > 0), но и энтальпией гидратации образовавшегося катиона (Мn+ + mH2O → Мn +·mH2O;
∆Hогидр< 0). Энергии ионизации d-элементов в сравнении с другими металлами велики, но они компенсируются большими энтальпиями гидратации их ионов. Вследствие этого электродные потенциалы большинства d-элементов отрицательны.
В периоде с ростом порядкового номера восстановительные свойства металлов уменьшаются, достигая минимума у элементов I В
232
группы. Тяжелые металлы VIII В и I В групп за свою инертность названы благородными.
7.На кислотно-основные свойства гидроксидов d-элементов влияют те же факторы (величина ионного радиуса и заряд иона), что и на гидроксиды p-элементов.
Гидроксиды низших степеней окисления d-элементов обычно проявляют основные свойства, а отвечающие высшим степеням окисления – кислотные. В промежуточных степенях окисления гидроксиды амфотерны. Особенно отчетливо изменение кислотно-основных свойств гидроксидов при изменении степени окисления проявляется в
соединенинях марганца. В ряду Mn(OH)2 – Mn(OH) 3 – Mn(OH) 4 – H2MnO4 – HMnO 4 свойства гидроксидов меняются от слабого основания Mn(OH)2 через амфотерные Mn(OH)3 и Mn(OH)4 к сильным ки-
слотам H2MnO4 и HMnO4.
В пределах одной подгруппы гидроксиды d-элементов одинаковой степени окисления характеризуются увеличением основных свойств при движении сверху вниз. Например, в III В группе Sc(OH)3
–слабое, а La(OH)3 – сильное основание. Элементы IVВ группы Ti, Zn, Hf образуют амфотерные гидроксиды Э(OH)4, но кислотные свойства их ослабевают при переходе от Ti к Hf.
8.Отличительной особенностью переходных элементов является образование фаз переменного состава. Это, во-первых, твердые растворы внедрения и замещения и, во-вторых, соединения переменного состава. Твердые растворы образуются элементами с близкими электроотрицательностями, атомными радиусами и одинаковыми кристаллическими решетками. Чем больше отличаются элементы по своей природе, тем менее они растворяются друг в друге и тем более склонны к образованию химических соединений. Такие соединения могут иметь как постоянный, так и переменный состав. В отличие от твердых растворов, в которых сохраняется решетка одного из компонентов, для соединений характерно образование новой решетки и новых химических связей. Другими словами, к химическим соединениям относят лишь те фазы переменного состава, которые резко отличаются по строению и свойствам от исходных.
Для соединений переменного состава характерны следующие особенности:
а) Состав этих соединений зависит от способа получения. Так, в зависимости от условий синтеза оксиды титана имеют состав TiO 1,2–
1,5 и TiO1,9–2,0 ; карбиды титана и ванадия – TiC 0,6–1,0 и VС 0,58–1,09 , нитрид
титана TiN 0,45–1,00 .
233

б) Соединения сохраняют свою кристаллическую решетку при значительных колебаниях количественного состава, то есть имеют
широкую область гомогенности. Так, TiC0,6–1,0 , как следует из формулы, сохраняет решетку карбида титана при недостатке в ней до 40%
атомов углерода.
в) Природа связи в таких соединениях определяется степенью заполнения d-орбиталей металла. Электроны внедренного неметалла заселяют вакантные d-орбитали, что приводит к усилению ковалентности связей. Именно поэтому доля металлической связи в соединениях начальных элементов d-рядов (IV–V групп) понижена.
Наличие ковалентной связи в них подтверждается большими положительными энтальпиями образования соединений, более высокими твердостью и температурой плавления, меньшей электропроводностью по сравнению с образующими их металлами
Стандартные окислительно-восстановительные потенциалы всех металлов первого переходного ряда за исключением меди (и серебра во втором переходном ряду) в системах М2+/М отрицательны. Металлы первого переходного ряда за исключением меди расположены в электрохимическом ряду напряжений до водорода. Поэтому они должны вытеснять водород из минеральных кислот. Однако некоторые из них реагируют с кислотами медленно, потому что на поверхности металла образуется защитный слой оксида. Это объясняет пассивность таких металлов, как хром, в коррозионных средах.
Нахождение металлов в природе. Самыми распространенными в земной коре металлами являются:
Al, Fe, Ca, Mg, Na, K, Ti, Mn,…
распространенность возрастает
Редкие металлы – это металлы, массовая доля которых в земной коре ≤ 0,01% (например: Ti, Pt, Pd).
Рассеянные металлы – это металлы, которые не образуют собственных руд (например: Sc, Tl, Hf).
Форма нахождения металлов в природе определяется их химической активностью. Малоактивные металлы встречаются в природе, как в соединениях, так и в свободном виде (самородные металлы): Au, Cu, Ag, Pt, Hg. Химически активные металлы находятся в природе только в виде соединений.
Получение металлов из их соединений – это задача металлур-
гии. Металлургия – это наука о промышленных способах получения металлов из руд. Любой металлургический процесс является процес-
234
сом восстановления ионов металла с помощью различных восстановителей, в результате которого получаются металлы в свободном виде. Металлургическими методами получают большинство металлов и множество сплавов. В зависимости от способа проведения металлур-
гического процесса различают пирометаллургию, гидрометаллургию и электрометаллургию.
Общие способы получения металлов
Наименование и сущность |
Примеры |
Примечание |
||||||
способа |
|
|
|
|
|
|
|
|
Пирометаллургический: |
а) восстановление водородом: |
Получают |
ме- |
|||||
получение металлов с помо- |
MoO3 + 3H2 = Mo + 3H2O; |
таллы |
высокой |
|||||
щью реакций восстановле- |
WO3 + 3H2 = W + 3H2O. |
чистоты. |
|
|||||
ния, протекающих при высо- |
|
|
|
|||||
ких температурах. В качест- |
б) восстановление углеродом, |
Получают |
ме- |
|||||
ве восстановителей исполь- |
оксидом углерода: |
|
|
таллы |
Fe, |
Cu, |
||
зуют H2, C, CO, Al, Mg, Са. |
2Fe2O3 +3C = 4Fe + 3CO2; |
Cd, Sn, Pb, Ge и |
||||||
|
Fe2O3 +3CO = 2Fe + 3CO2; |
другие. |
|
|
||||
|
|
|
|
|||||
|
CuO + CO = Cu + CO2. |
Получают |
Mn, |
|||||
|
в) металлотермия : |
|||||||
|
Cr2O3 + 2 Al = 2 Cr + Al2O3; |
Cr, Ti, W и дру- |
||||||
|
гие. |
|
|
|||||
|
(алюмотермия) |
|
|
|||||
|
|
|
|
|||||
Гидрометаллургический: |
(CuOH)2CO3 + |
|
2H2SO4 = |
Получают |
ме- |
|||
получение металлов из рас- |
= 2CuSO4 + 3H2O+ CO2, |
таллы |
Cu, |
Ni, |
||||
творов солей. |
CuSO4 + Fe = FeSO4 + Cu↓ |
Ag, Au, |
Zn, |
Cd, |
||||
|
Mo. |
|
|
|||||
Электрометаллургический: |
Восстановление |
из водных |
Получают ме- |
|||||
получение металлов из рас- |
растворов солей |
|
(гидроэлек- |
|||||
|
таллы Cu, Ni, |
|||||||
творов или расплавов солей |
трометаллургия): |
|
|
|||||
|
|
Ag, Zn, Cd, Со и |
||||||
и оксидов с помощью элек- |
|
|
|
|
|
|||
|
|
|
|
|
другие. |
|
||
|
|
|
|
|
|
|||
CuSO4 + 2H2O Сu + |
|
|||||||
трического тока |
|
|||||||
|
|
|
||||||
|
+ О2 + H2SO4 |
|
|
|
||||
235
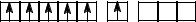
ТЕМА 10. d - ЭЛЕМЕНТЫ VI В ГРУППЫ
Общая характеристика элементов
Электронная конфигурация хрома:
3d |
4s |
4p |
Сr
Атом Cr имеет 6 неспаренных электронов: пять d-электронов на пяти d-орбиталях и 1 электрон на внешней s-орбитали. У атомов хрома и молибдена наблюдается «проскок» одного электрона с ns- на (n-1)d-подуровень и образование стабильной конфигурации d5. Максимальная степень окисления +6. Общая характеристика элементов представлена в табл.11.1.
|
|
|
|
|
|
|
Таблица 11.1 |
|
|
Некоторые свойства d-элементов VI группы |
|
||||
|
|
|
|
|
|
|
|
Ме- |
Электрон- |
|
Атом- |
Энергия |
Электрод- |
tпл.,оС |
Характер- |
талл |
ная конфи- |
|
ный ра- |
ионизации, |
ный потен- |
|
ные степе- |
|
гурация |
|
диус, нм |
кДж/моль |
циал, |
|
ни окис- |
|
|
|
|
|
ЕоМе+3/Ме, В |
|
ления |
Cr |
...3d54s1 |
|
0,127 |
653 |
-0,744 |
1907 |
+2, +3, +6 |
|
|
|
|
|
|
|
|
Mo |
...4d55s1 |
|
0,139 |
684 |
-0,20 |
2623 |
+2, +3,+4, |
|
|
|
|
|
|
|
+6 |
W |
...5d46s2 |
|
0,140 |
759 |
– |
3422 |
+2, +3,+4, |
|
|
|
|
|
|
|
+6 |
Как и в других подгруппах d-элементов, в ряду Cr–Mo–W увеличивается энергия ионизации, следовательно, химическая активность металлов понижается. Вследствие лантаноидного сжатия атомные радиусы Мо и W близки, поэтому молибден и вольфрам по свойствам ближе друг к другу, чем к хрому.
В соединениях хром, молибден, вольфрам проявляют все степени окисления от +2 до +6. Для хрома состояние +3 наиболее устойчиво. При переходе от хрома к вольфраму наблюдается тенденция к возрастанию устойчивости соединений с высшей степенью окислениия +6. Рост степени окисления сопровождается усилением кислотных и окислительных свойств и увеличением ковалентного характера связей.
Cr, Mo, W – это очень твердые и тугоплавкие металлы. Вольфрам самый тугоплавкий из металлов, он – лучший материал для нитей и спиралей ламп накаливания. Высокая температура плавления свиде-
236

тельствует о заметном ковалентном вкладе в химическую связь. У d- элементов этот ковалентный вклад обусловлен наличием неспаренных электронов на d-оболочке. Наличие 6 неспаренных электронов в кристаллах d-элементов 6 группы обеспечивает максимальный ковалентный вклад и самые высокие tпл среди металлов.
В природе хром и его аналоги в свободном состоянии не встреча-
ются. Важнейшие минералы:
Fe(CrO2)2 – хромит (хромистый железняк), PbCrO4 – крокоит;
MoS2 – молибденит (молибденовый блеск); (Fe, Mn)WO4 – вольфрамит;
CaWO4 – шеелит.
Получение. Хром получают в виде феррохрома (сплава с железом), восстанавливая углем хромистый железняк в электрических печах:
Fe(CrO2)2 + 4C ® Fe + 2Cr + 4CO
сплав
Выплавленный феррохром используют для получения нержавеющей стали.
Чистый хром можно получить алюмотермическим путем из оксида Cr(III) или восстановлением кремнием в присутствии CaO:
Cr2O3 + 2Al ¾t ® 2Cr + Al2O3
2Cr2O3 + 3Si + 3CаO ¾t ® 4Cr + 3CaSiO3
Cr2O3 получают сплавлением хромистого железняка с содой в присутствии кислорода и последующим восстановлением углем:
4Fe(CrO2)2 + 7O2 + 8Na2CO3 ¾t ® 8Na2CrO4 + 2Fe2O3 +8CO2
2Na2CrO4 + H2SO4 ® Na2Cr2O7 + Na2SO4 + H2O
Na2Cr2O7 + 2C ¾t ® Cr2O3 + Na2CO3 + CO
В гидрометаллургическом методе молибден извлекают путем флотации из различных руд, в которых содержатся соли молибденовой кислоты, и чаще всего в виде парамолибдата аммония
(NH4)6Mo7O24 × 4H2O.
Молибден и вольфрам получают восстановлением их оксидов или галогенидов водородом:
4MoS2 + 14O2 ® 4MoO3 + 8SO2
MoO3 + 3H2 ® Mo + 3H2O
237
4FeWO4 + 4Na2CO3 + O2 ¾¾®t 4Na2WO4 + 2Fe2O3 + 4CO2
Na2WO4 + 2HCl → 2NaCl + H2WO4 H2WO4 ¾¾®t WO3 + H2O
WO3 + H2 → W + H2O
Если из руды получают WF6, то восстанавливают его:
WF6 + 3H2 → W + 6HF
Металлы получают в виде порошков. Их переводят в слиток методом порошковой металлургии: подвергают холодному прессованию под высоким давлением, затем спекают в инертной атмосфере. Металлы высокой степени чистоты получают через карбонилы, которые легко чистят перегонкой и далее разлагают при нагревании:
Ме СО Р,t Ме СО
+ 6 ¾¾® ( )6
Ме(СО)6 ¾¾®t Ме + 6СО
Химические свойства
В компактном состоянии хром, молибден и вольфрам устойчивы, но порошки легко сгорают в кислороде при нагревании до 800ºС, при этом образуются оксиды в характерных для этих металлов степенях окисления:
4Cr + 3O2 → 2Cr2+3O3;
(W) 2Mo + 3O2 → 2Mo+6O3
При комнатной температуре хром, молибден и вольфрам взаимодействуют с фтором, а при нагревании с остальными галогенами:
2Cr + 3Г2 → 2CrГ3 (Г = F, Cl, Br);
Cr + I2 → CrI2
(W) Mo + 3F2 → MoF6; 2Mo + 5Cl2 → 2MoCl5;
W + 3Cl2 → WCl6
Сплавлением металлов с серой образуются сульфиды, кристаллические вещества переменного состава:
2Cr + 3S ¾t ® Cr2S3
238
(W) Mo + 2S ¾t ® MoS2 (дисульфид)
При нагревании хром, молибден, вольфрам соединяются с азотом с образованием нитридов MeN, Me2N и др. (нитриды Мо и W можно получить взаимодействием металла с газообразным аммиаком). С
углеродом образуют карбиды Cr3C2, Cr4C, Mo2C, W2C, MoC, WC.
Нитриды и карбиды металлов VI В группы – сверхтвердые, тугоплавкие, химически инертные соединения. WC по твердости не уступает алмазу. Все они являются соединениями внедрения. Атомы неметаллов находятся в пустотах кристаллической решетки металлов.
Металлы VI В группы, как и остальные d-элементы, с водородом химически не взаимодействуют. Хром при высоких температурах растворяет водород, образуя твердые растворы внедрения. Молибден и вольфрам водород практически не поглощают.
Хром, молибден, вольфрам стоят в ряду напряжений до водорода (хром находится между цинком и железом), однако они являются довольно инертными металлами. Это обусловлено пассивацией – образованием на поверхности тонкой, но плотной оксидной пленки. Наиболее сильно пассивируется хром. При температуре красного каления хром, молибден и вольфрам реагируют с парами воды, образуя окси-
ды:
2Cr + 3H2O ¾¾®t Cr2O3 + 3H2
Мо + 2Н2О ¾¾®t МоО2 + 2Н2
В непассивном состоянии хром довольно активен и реагирует с
кислотами-неокислителями HCl и H2SO4 (разб), с образованием со-
единений Cr2+, поскольку в этих условиях пассивирующая пленка разрушается:
Cr + 2 HCl → CrCl2 + H2;
Cr + H2SO4 → CrSO4 + H2,
Cr+2 + 2e– = Cr; E0 = –0,91 B
Кислоты-окислители HNO3, H2SO4 (конц) на хром не действуют, а еще больше пассивируют его. Молибден и вольфрам легко растворяются в горячей смеси HNO3 и HF:
Mo + 6HNO3 + 8HF → H2[MoF8] + 6NO2 + 6H2O
и в расплавах щелочей в присутствии окислителей:
W + 3NaNO3+2NaOH → Na2WO4 + 3NaNO2 + H2O
239
Соединения металлов VI В группы
Для всех элементов VI В группы известны кислородные соединения со степенями окисления +6, +4. Хром образует кислородные соединения в степенях окисления +2, +3, поэтому низшие оксиды получены только для хрома.
Оксид хрома (II) CrO – основный оксид, черное, тугоплавкое вещество, нерастворимое в воде. CrO реагирует с кислотами с образованием солей:
CrO + H2SO4 → CrSO4 + H2O
CrO получают осторожным обезвоживанием Cr(OH)2 в восстановительной атмосфере:
Cr(OH)2 → CrO + H2O
Гидроксид Cr(OH)2 – слабое нерастворимое основание коричневого цвета, взаимодействует с кислотами:
Cr(OH)2 + 2HCl → CrCl2 + 2H2O
Получают гидроксид действием аммиака или щелочей на соли Cr(II) в инертной среде:
CrCl2 + 2NaOH → Cr(OH)2↓ + 2NaCl
Соединения Cr(II) являются сильными восстановителями, так как степень окисления +2 для хрома не характерна. Cr(OH)2 легко окисляется кислородом воздуха, а CrO даже при растирании на воздухе окисляется до Cr2O3:
4Cr(OH)2 + O2 + 2H2O→ 4Cr(OH)3.
Оксид хрома (III) Cr2O3 – самое устойчивое соединение хрома. Cr2O3 – темно-зеленое тугоплавкое вещество. Применяется в качестве абразивного материала (паста ГОИ) и добавки к корунду при выращивании кристаллов рубина.
Cr2O3 в компактном состоянии инертен, не растворяется в воде, растворах кислот и щелочей. Амфотерные свойства этот оксид проявляет, взаимодействуя при сплавлении с дисульфатами и щелочами:
Cr2O3 + 3 K2S2O7 → Cr2(SO4)3 + 3K2SO4
Cr2O3 + 2NaOH → 2NaCrO2 + H2O (метахромит натрия)
В мелкодисперсном состоянии Cr2O3 растворяется в сильных кислотах и щелочах:
240
