
- •Общая химия Учебное пособие
- •Предисловие
- •Глава 1. Основные понятия химии. Современная номенклатура неорганических веществ. Химические свойства и способы получения неорганических соединений. Химические реакции Основные понятия общей химии
- •Важнейшие классы неорганических соединений и их номенклатура
- •Важнейшие химические свойства и способы получения оксидов, оснований, кислот, амфотерных гидроксидов и солей
- •Химические реакции. Классификация химических реакций
- •I. Классификация реакций по числу и составу реагирующих веществ
- •II. Классификация реакций по тепловому эффекту
- •III. Классификация реакций по фазовому составу веществ
- •IV. Классификация химический реакций
- •Примеры решения типовых задач
- •Литература
- •Тема: Важнейшие химические свойства и способы получения оксидов, оснований, кислот, амфотерных гидроксидов и солей
- •Тема: Классификация химических реакций
- •Контрольная работа №1 Задание 1.
- •Задание 2.
- •Задание 3.
- •Задание 4.
- •Глава 2. Строение атома. Периодическая система и Периодический закон д.И. Менделеева в свете современных представлений о строении атома. Химическая связь. Комплексные соединения Строение атома
- •Последовательность заполнения электронных состояний в атоме:
- •Периодический закон и периодическая система д. И. Менделеева в свете современных представлений о строении атома
- •Химическая связь
- •Механизмы образования химической связи (метод валентных связей)
- •Комплексные соединения
- •Литература
- •Карапетьянц м.Х., Дракин с.И. Общая и неорганическая химия. – м.: Химия, 1993. – 558 с.
- •Примеры решения типовых задач
- •Задачи и упражнения для самостоятельной работы Тема: Строение атома
- •Тема: Периодическая система элементов
- •Тема: Химическая связь и строение молекул
- •Тема: Комплексные соединения
- •Контрольная работа №2
- •Глава 3. Термодинамика химических процессов Основные понятия термодинамики
- •Первый закон термодинамики
- •Второй закон термодинамики
- •Третий закон термодинамики
- •Энергия Гиббса
- •Литература
- •Карапетьянц м.Х., Дракин с.И. Общая и неорганическая химия. – м.: Химия, 1993. – 558 с.
- •Примеры решения типовых задач
- •Задачи и упражнения для самостоятельной работы
- •Глава 4. Химическая кинетика. Обратимость химических реакций. Химическое равновесие Основные понятия химической кинетики
- •Факторы, влияющие на скорость химических реакций
- •Обратимость химических реакций. Химическое равновесие
- •Смещение химического равновесия
- •Литература
- •Карапетьянц м.Х., Дракин с.И. Общая и неорганическая химия. – м.: Химия, 1993. – 558 с.
- •Примеры решения типовых задач
- •Задачи и упражнения для самостоятельной работы Тема: Химическая кинетика
- •Тема: Обратимость химических реакций. Химическое равновесие
- •Контрольная работа №3 по разделам «Термодинамика» и «Химическая кинетика»
- •Задание 3.
- •Задание 4.
- •Задание 5.
- •Итоговый тест Вариант 1
- •Вариант 2
- •Вариант 3
- •Вариант 4
- •Вариант 5
- •Литература
- •Карапетьянц м.Х., Дракин с.И. Общая и неорганическая химия. – м.: Химия, 1993. – 558 с.
- •Некоторые константы и величины
- •Соотношение между некоторыми единицами в различных системах.
- •Значения газовой постоянной в различных единицах измерения
- •Электродные потенциалы
- •Содержание
- •Для заметок
Литература
Глинка Н. Л. Общая химия. – М.: Химия, 2006. – 720 с.
Глинка Н.Л. Задачи и упражнения по общей химии. – Л. Химия, 1985. – 264 с.
Карапетьянц м.Х., Дракин с.И. Общая и неорганическая химия. – м.: Химия, 1993. – 558 с.
Коровин В.Н. Общая химия. – М.: Высшая школа, 2000. – 557 с.
Коровин Н.В., Масленникова Г.Н. и др. Курс общей химии. – М.: Высшая школа, 1990. – 445 с.
Суворов А.В., Никольский А.Б. Общая химия. – СПб: Химиздат, 2001. – 512 с.
Примеры решения типовых задач
Задача 1. Распределите электроны по уровням, напишите электронную формулу атома Ca.
Решение: заряд ядра атома определяем по порядковому номеру элемента; число уровней равно номеру периода, в котором находится элемент; максимальное число валентных электронов определяется номером группы, т.к. элемент расположен в главной подгруппе. На первых двух уровнях максимальное число электронов – 2 и 8 соответственно (определяем по формуле 2n2, где n – номер периода). Общее число электронов предпоследнего энергетического уровня просчитываем.
Итак, электроны в атоме кальция распределяются по уровням следующим образом: +20 )2 )8 )8 )2.
Электронная формула: 1s22s22p63s23p64s2 (валентные электроны).
Задача 2. Напишите электронную формулу элемента № 82.
Решение: № элемента 82, следовательно, у него 82 электрона. Воспользуемся принципами и схемой заполнения электронных состояний в атоме. Электронная формула атомаPbимеет вид:
1s22s22p63s23p64s23d104p65s24d105p66s24f145d106p2.
Задача 3. Напишите электронную структуру элемента с номером 24, укажите его семейство и приведите аналоги.
Решение:воспользуемся принципами и схемой заполнения электронных состояний в атоме. Электронная формула атомаCrимеет вид: 1s22s22p63s23p64s13d5. Поскольку последний электрон при заполнении перешел вd-состояние, то этоd-элемент. Электронными аналогами его будут все элементы, имеющими конфигурациюns1(n-1)d5. В случае хрома его электронным аналогом является молибден.
Задача 3.Распределите электроны по уровням, напишите электронную формулу атомаFeв основном и возбужденном состоянии, укажите квантовые состояния его валентных электронов и распределите их по квантовым ячейкам.
Решение:заряд ядра атома определяем по порядковому номеру элемента (+ 26); число уровней – по номеру периода (4). Так как железо расположено в побочной подгруппе, то валентные электроны его распределяются междуs– подуровнем внешнего энергетического уровня иd– подуровнем предвнешнего уровня, общее число электронов равно 8 (номер группы). Так, если в 4sсостоянии находятся 2 электрона, то в 3d-состоянии – 6 (номер группы минус 2). На первых двух уровнях максимальное число электронов – 2 и 8 соответственно (определяется удвоенным квадратом главного квантового числа – 2n2). Общее число электронов предпоследнего энергетического уровня атома железа просчитываем, оно равно 14.
Итак, в невозбужденном атоме железа электроны распределяются следующим образом: +26 )2 )8 )14 )2.
Электронная формула атома железа в невозбужденном состоянии имеет вид: 1s22s22p63s23p63d64s2 ( валентные электроны).
Порядок заполнения квантовых ячеек подуровня электронами определяется правилом Гунда по принципу наибольшего суммарного спина:
3d4s

В возбужденном атоме железа один s– электрон переходит на 4р – подуровень. В возбужденном состоянии электроны распределяются по квантовым ячейкам следующим образом:
Fе *: 1s22s22p63s23p63d64s14p1 или ... 3d64s14p1
3d 4s 4p1

Задача 4. Определите квантовые числа последнего состояния (электрона) в атоме железа.
Решение. Электронная конфигурация железа: 1s22s22p63s23p64s23d6.
 3d4s
3d4s
ml= -2; -1; 0; +1; +2
Следовательно, последний электрон приходит на 3d-орбиталь, ему соответствует следующий набор квантовых чисел:n=3,l=2,ml= -2,ms = -1/2.
Задача 2. Напишите электронные формулы ионовMn2+,S2-, укажите число неспаренных электронов.
Решение:
1. Распределение электронов по энергетическим уровням у атома Mn(d-элемент): 1s22s22p63s23p63d54s2 (валентные электроны).
3d4s

При образовании положительных ионов у d- элементов первыми всегда удаляютсяs-электроны внешнего слоя, т.е. для ионаMn+2справедлива электронная формула: 1s22s22p63s23p63d54s0(валентные электроны).
3d4s

Число неспаренных электронов равно 5.
2. При образовании отрицательных ионов происходит дальнейшее заполнение энергетических подуровней согласно правилу Клечковского, то есть для атома серы S: 1s22s22p63s23p4 (валентные электроны).
3s 3p
Для иона S2– произойдет «достройка» 3р-подуровня: 1s22s22p63s23p6.
3s 3p

Число неспаренных электронов равно 0.
Задача 4.Укажите положение элемента в периодической системе (период, группу, подгруппу), если последний электрон в его атоме находится в состоянии: а) 3d6; б) 4p2. Ответ обоснуйте.
Решение:
а) последний электрон атома вd– состоянии, следовательно, это элемент побочной подгруппы. В атомах элементов побочных подгрупп последний валентный электрон попадает наd– подуровень предпоследнего энергетического уровня, из этого следует, чтоn=4. Величину главного квантового числа (4) определяет номер периода. Так как 4s-состояние заполняется электронами раньше, чем 3d, то общее число электронов, которые могут быть валентными, равно 4: 3d24s2. Значит, это элемент 4-го периодаIVгруппы побочной подгруппы – титан (Ti).
б)электрон в атоме вp– состоянии, следовательно, это элемент главной подгруппы. В атомах элементов главных подгрупп валентные электроны расположены на внешнем энергетическом уровне, отсюда величина главного квантового числа 4 (номер периода). Так какp-состояние внешнего уровня заполняется электронами послеs– состояния, то общее число валентных электронов 4, что определяет номер группы. Следовательно, это элемент 4-го периодаIVгруппы главной подгруппы – германий.
Задача 5. Определите вид химической связи в веществах: CH4, Ar, Cа, RbF, Si, ZnSe. Какой тип кристаллической решетки они имеют в конденсированном состоянии? Укажите, какие частицы находятся в узлах их кристаллической решетки.
Решение: для кристаллов метана и аргона характерна молекулярная решетка. В узлах первой кристаллической решетки находятся неполярные молекулыCH4, между которыми действуют дисперсионная составляющая ван-дер-ваальсовых сил. Дисперсионное взаимодействие проявляется и в кристаллах между одноатомными молекулами аргона.
Кальций – металл, для него характерна металлическая решетка. Связь между катионами кальция, находящимися в узлах решетки, и обобществленными электронами – металлическая.
В соединении RbFтипичная ионная связь, так как ΔЭОRbF= 4,1 – 0,86 = 3,24. Для кристалловRbFхарактерна ионная решетка, в узлах которой находятся положительные ионыRb+и отрицательные ионыF-.
Кристаллический кремний (неметалл) имеет ковалентную кристаллическую решетку типа алмаза, в которой каждый атом кремния связан с четырьмя соседними атомами неполярной ковалентной связью.
Между атомами цинка и селена, находящимися в узлах кристаллической решетки, действует полярная ковалентная связь, так как ΔЭОZnSe= 2,4 – 1,7= 0,7.
Задача 6.Рассмотрите строение молекулыBCl3с позиции метода валентных связей: укажите квантовые состояния валентных электронов в атомах, образующих связи в молекуле, форму и валентные углы между связями; нарисуйте модель молекулыBCl3и определите полярна ли она.
Решение: определяем валентные электроны в атомах, образующих связи, и распределяем их по квантовым ячейкам: В…2s22p1. Атом бора в молекулеBCl3образует три химические связи, следовательно, он находится в возбуждённом состоянии:B*….2s12p2. Происходит гибридизацияsp2электронных орбиталей с образованием трех гибридных электронных облаков. В образовании связи у хлора участвует p-электрон:Cl…3s23p5. СвязиB–Cl образованы перекрытием гибридного электронного облака атома В иp-электронного облака атомаCl. Направленность гибридных электронных облаков трехвалентного атома В определяет направленность связей и форму молекулыBCl3. СвязиB–Clнаправлены под углом 1200, молекулаBCl3имеет форму плоского треугольника. Схема образования связей в молекулеBCl3:
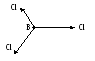
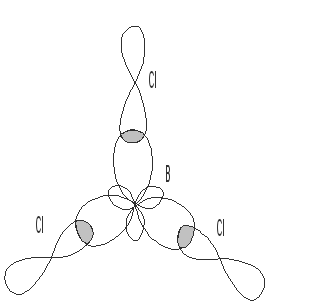
Векторы дипольных моментов связей μсв>0 направлены в сторону атома с большей электроотрицательностью. Суммарный дипольный момент молекулы равен 0, т.е. молекула неполярна, хотя все связи B-Cl полярны.
Задача 7. Почему комплексный ион [Cu(NH3)2]+ имеет линейное строение?
Решение: Линейное строение иона является следствием образования двух гибридных 4sp-орбиталей иона Cu+, которые акцептируют электронные пары молекул аммиака.
Задача 8. Комплексный ион [Zn(NH3)4]2+ имеет тетраэдрическое строение. Какие орбитали комплексообразователя используются для образования связей с молекулами аммиака?
Решение: Тетраэдрическое строение характерно для sp3-гибридных орбиталей. Ион Zn2+ имеет свободные 4s и 4p-орбитали, гибридизация которых приводит к образованию 4 sp3-орбиталей.
Задача 9. Почему ион [NiCl4]2- парамагнитен (тетраэдр), а ион [Ni(CN)4]4- диамагнитен (плоский квадрат)?
Решение: Ионы Cl- слабо взаимодействуют с ионами Ni2+. Электронные пары от Cl- поступают на орбитали с главным квантовым числом 4. При этом оставшиеся у иона никеля 3d-электроны остаются неспаренными и ион [NiCl4]2- –парамагнитен.
В [Ni(CN)4]4 - вследствие sp2d-гибридизации происходит спаривание электронов никеля и комплексный ион становится диамагнитен. Ион [NiCl4]2- –внешнеорбитальный и высокоспиновый, так как электронные пары от хлора поступают на свободные орбитали с более высоким квантовым числом 4.
Ион [Ni(CN)4]4- – внутриорбитальный и низкоспиновый, так как электронные пары акцептируются гибридной орбиталью, включающей «внутренние» 3d – подуровни атома никеля; все электроны спарены, при гибридизации образуется комплексный ион плоского строения.
Задача 10. Константа нестойкости иона [Ag(CN)2]- составляет 1·10-21. Вычислите концентрацию ионов серебра в 0,05 М растворе К[Ag(CN)2], содержащем, кроме того, 0,01 моль/л KCN.
Решение: Вторичная диссоциация комплексного иона протекает по уравнению: [Ag(CN)2]- ↔ Ag+ + 2CN- .
В присутствии избытка ионов CN-, создаваемого в результате диссоциации KCN (которую можно считать полной), это равновесие смещено влево настолько, что количеством ионов CN- , образующимся при вторичной диссоциации, можно пренебречь. Тогда [CN-] = C KCN = 0,01моль/л. По той же причине равновесная концентрация ионов [Ag(CN)2]- может быть приравнена общей концентрации комплексной соли (0,05 моль/л). По условию задачи: Kн = [Ag+] · [CN-]2 / [Ag(CN)2]- = 1·10-21
Отсюда выражаем концентрацию ионов Ag+:
[Ag+] = 1·10-21 · [Ag(CN)2]- / [CN-]2 .
Подставив значения концентраций ионов CN- и [Ag(CN)2]-, получим:
[Ag+] = 1·10-21 · 0,05/(0,01)2= 5·10-19 моль/л .
