
Hepatology-I-1
.pdf
Hepato_2003_Last_With_Index.qxd 10.02.2003 18:39 Page 391
X. ЦИРРОЗ ПЕЧЕНИ И ПОРТАЛЬНАЯ ГИПЕРТЕНЗИЯ
портальной гипертензии. В ранней стадии цирроза печени исследование выявляет нормальные или увеличенные размеры печени, признаки очаго вой жировой инфильтрации. В терминальной стадии заболевания размеры печени уменьшаются, ее контуры становятся неровными, увеличиваются размеры хвостатой доли, выражен коллатеральный кровоток, появляется спленомегалия и асцит.
Портальная гипертензия ведёт к образованию спонтанных портоси стемных коллатералей, которые в клинической практике можно визуали зировать с помощью неинвазивных методов. Диагностика проявлений пор тосистемного шунтирования имеет большое клиническое значения в связи с высокой специфичностью получаемых параметров.
Варикозное расширение вен пищевода и желудка выявляется эндо скопически с частотой от 2 до 70%. Существуют проблемы эндоскопиче ской диагностики варикозной трансформации желудочных вен в связи с их более глубоким расположением. Вены желудка могут являться как про должением пищеводных вен, так и располагаться изолированно, преиму щественно в своде желудка. Последний вариант чаще наблюдается при тромбозе селезёночной вены.
Несмотря на низкую чувствительность, эндоскопия характеризуется высокой специфичностью, достигающей 100%. Иными словами, обнару жение варикозного расширения вен пищевода с высокой степенью вероят ности свидетельствует о наличии синдрома портальной гипертензии.
На поздних стадиях цирроза печени (стадия сформировавшегося цир роза и дистрофическая стадия) эндоскопия носит уже не столько диагно стический характер, сколько позволяет выявить и оценить возможные факторы риска развития кровотечения и решить вопрос о необходимости первичной профилактики геморрагии.
Ангиографическая характеристика изменений гепатолиенальной зоны при циррозе печени
Ангиографическое исследование позволяет получить изображение сосудов, динамику прохождения рентгеноконтрастного вещества по арте риям и венам, а также накопление этих препаратов в печени и селезенке. Часть признаков (диаметры селезеночной и печеночной артерий, селезе ночной и воротной вен, величина портовертебрального угла) могут быть точно измерены по ангиограммам. В то же время многие признаки весьма трудно поддаются количественному выражению. Это касается особенно стей структуры, ветвления, плотности сосудистого рисунка, длительности нахождения рентгеноконтрастного вещества в различных по калибру сосу
391

Hepato_2003_Last_With_Index.qxd 10.02.2003 18:39 Page 392
РУКОВОДСТВО ПО ХИРУРГИИ ПЕЧЕНИ И ЖЕЛЧЕВЫВОДЯЩИХ ПУТЕЙ
дах, динамики изменения плотности накопления контрастного вещества в паренхиме печени и селезенки.
Качественное получение изображения является основой ангиографи ческого исследования и зависит от уровня установки катетера, объема и скорости введения контрастного вещества, а также его концентрации.
Длительный латентный период развития цирроза печени и порталь ной гипертензии приводил к многочисленным изменениям, выявляемым во время вазографической диагностики. Если нарушения сосудистой структу ры печени являются следствием цирроза печени, то перестройка внепече ночных отделов портальной системы и селезенки отражают изменения связанные с наличием портальной гипертензии. Изучение этих изменений методом ангиографии требует выполнения ряда последовательных этапов. Осуществление артериографии для детальной оценки изменений гепато лиенальной области включает три самостоятельные процедуры.
Первой является целиакография. Метод дает возможность получить обзорную картину сосудов печени и селезенки, а также селезеночной и во ротной вен. В случаях перераспределения кровотока к селезенке на целиа кограммах изображение сосудов печени может оказаться низкого качества без визуализации мелких артериальных ветвей и недостаточно плотным контрастированием паренхимы. Выполнение суперселективной артерио графии из общей или собственной печеночной артерии с высоким каче ством изображения позволяет дифференцировать объемные образования печени различной природы: узлы регенерации, кисты, опухолевые очаги.
Для хорошего контрастирования селезенки, селезеночной и воротной вен необходима постановка катетера в селезеночную артерию для выпол нения возвратной спленопортографии.
Выполнение чрескожной чреспеченочной портографии обеспечивает четкую визуализацию большинства отделов портальной системы и позволя ет измерить величину венозного давления. Однако метод несет потенциаль но наибольший риск в силу неблагоприятных факторов — уменьшения и по вышения плотности печени, нарушения свертывающей системы крови.
На ангиограммах печени изменения структуры артериальной системы носят полиморфный характер. Ветви печеночной артерии искривлены, извиты и истончены, а в отдельных случаях выпрямлены (рис. 10.1).
К числу основных признаков следует отнести гиповаскуляризацию пе чени за счет мелких артериальных ветвей и уменьшение степени интенсив ности накопления рентгеноконтрастного вещества.
Наличие патологических сосудов с признаками локальной гиперва скуляризации и неравномерным накоплением рентгеноконтрастного ве щества является типичным для гепатоцеллюлярного рака печени. Диффе
392

Hepato_2003_Last_With_Index.qxd 10.02.2003 18:39 Page 393
X. ЦИРРОЗ ПЕЧЕНИ И ПОРТАЛЬНАЯ ГИПЕРТЕНЗИЯ
ренциальная диагностика таких состояний представляется трудной, осо бенно при резко выраженной деформации сосудистого рисунка в дистро фической стадии цирроза печени. Суперселективная ангиография печени с введением рентгеноконтрастного вещества в собственную печеночную ар терию существенно улучшает визуализацию.
Артериальный сосудистый рисунок селезенки при циррозе печени и портальной гипертензии повергается незначительным изменениям, об условленным увеличением ее размеров. Степень выпрямления внутриор ганных ветвей зависит от размеров органа.
Спленомегалия выявляется у большинства больных (до 90 %). Наи более часто наблюдается смещение селезеночной вены медиально с обра зованием ее изгибов вследствие уменьшения расстояния от ворот селезен ки до впадения в воротную вену (рис. 10.1 б).
Изучение портальной циркуляции может быть осуществлено с использо ванием двух видов ангиографического исследования — чрескожной чреспече ночной портографии и артериальной возвратной сплено и мезентерикопорто графии. По результатам возвратной портографии можно отчетливо визуализи ровать крупные вены и выраженные коллатерали, установить величину портовертебрального угла. В то же время внутрипеченочные ветви воротной вены, коллатерали с низким уровнем кровотока прослеживаются неотчетливо.
Высокое качество визуализации практически всех отделов портально го тракта при чрескожной катетеризации воротной вены и ее притоков со четается с получением данных об уровне давления крови (рис. 10.2).
а |
б |
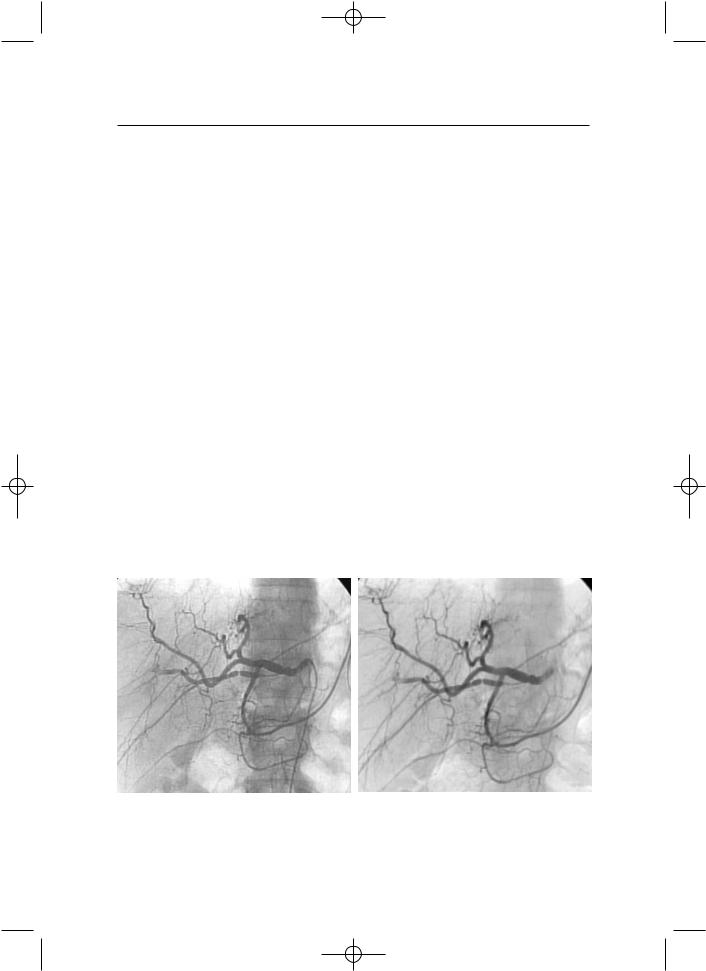
Рис. 10.1 Ангиограммы печени и селезенки при циррозе печени:
а — артериальная фаза; артериальный рисунок печени обеднен и деформирован, селе: зеночная артерия расширена; б — паренхиматозная фаза; накопление контрастного вещества в печени уменьшено, селезенка интенсивно накапливает препарат, селезе:
ночная вена расширена, контрастируется расширенная левая желудочная вена.
393

Hepato_2003_Last_With_Index.qxd 10.02.2003 18:39 Page 394
РУКОВОДСТВО ПО ХИРУРГИИ ПЕЧЕНИ И ЖЕЛЧЕВЫВОДЯЩИХ ПУТЕЙ
Основным коллатеральным путем оттока является система расширенной левой желудочной вены. Отмечается четкая корреляция наличия ретроград ного кровотока в левой и коротких желудочных венах с данными эндоскопиче ского исследования пищевода и желудка.
Состояние внутрипеченочной архитектоники ветвей воротной вены отражает изменения, степень которых зависит от клинической стадии цир роза печени. Они характеризуются деформацией сосудистого рисунка и уменьшением числа мелких терминальных ветвей. В стадии сформировав шегося цирроза отмечается широкий спектр изменений в виде чередования участков умеренной и выраженной деформации, которые носят диффуз ный характер, практически одинаково часто встречаясь в различных сег ментах правой и левой долей.
В последние десятилетия показания к назначению сложных инвазив ных методов сосудистой диагностики претерпели изменения. Важная роль в скрининговой диагностике принадлежит ультразвуковому исследова нию. Кроме того, ультразвуковое исследование успешно применяется как метод динамического контроля. Использование эндоскопической диагно стики и цветного дуплексного исследования позволяет ответить на пода вляющее число вопросов ранее требовавших назначения ангиографиче ской процедуры. Однако ангиографическая диагностика не утратила свое го значения в случаях сочетанных заболеваний, а также для
предоперационной оценки состояния артериального и венозного русла перед про ведением внутрисосудистых вмешательств.
Анализ данных чре скожной чреспеченочной портографии позволяет установить прямые призна ки нарастания портальной гипертензии при циррозе печени. Увеличение диаметра селезеночной вены, уменьше ние портовертебрального угла и наличие коллатераль ного кровотока, выявленные по результатам артериогра фии, позволяют оценить степень портальной гипер тензии. Прямая портогра
394

Hepato_2003_Last_With_Index.qxd 10.02.2003 18:39 Page 395
X. ЦИРРОЗ ПЕЧЕНИ И ПОРТАЛЬНАЯ ГИПЕРТЕНЗИЯ
фия стала назначаться не столько для диагностики, как для выполнения эмболизации вен желудка.
Современные рентгеновские установки с цифровой записью изобра жения позволяют значительно повысить качество изображения, быстроту получения данных исследований и облегчили хранение информации. Тра диционные методы ангиографического исследования, за исключением воз можно прямой спленопортографии, являются до настоящего времени эта лонными и в значительной степени служат методическим стандартом даже в лабораториях, оснащенных самой совершенной техникой.
Использование способов субтракции или вычитания несомненно повышает качество изображения сосудов и органов в паренхиматозной фазе исследования, однако для этого необходим исключительно высокий уровень кооперации с больным (рис. 10.3).
Повышению качества результатов диагностики способствует исполь зование специальной программы «Landmark», когда осуществляется ча стичное вычитание фона. В этом режиме в меньшей степени сказываются двигательные артефакты при повышении контрастности изображения (рис. 10.4).
Использование преимуществ каждого из вариантов цифровой записи рентгеновского изображения сосудов с комбинацией субтракции и частич ного вычитания фона позволяет оттенить наиболее значимые изменения в различных фазах прохождения рентгеноконтрастного вещества.
Таким образом, только сочетание анализа данных аналоговой серий ной съемки с результатами математической обработки субтракционных
а |
б |
Рис. 10.3 Ангиограммы селезенки.
а— рентгенография выполнена в аналоговом режиме; б — рентгенография выполнена
врежиме субтракции, дыхательные движения во время съемки не позволили получить полноценное вычитание фона для изолированного изображения сосудов
395
Hepato_2003_Last_With_Index.qxd 10.02.2003 18:39 Page 396
РУКОВОДСТВО ПО ХИРУРГИИ ПЕЧЕНИ И ЖЕЛЧЕВЫВОДЯЩИХ ПУТЕЙ
ангиограмм позволяет достоверно оценить характер поражения сосудистой системы и органов.
С точки зрения риска развития осложнений наиболее опасным явля ется чрескожный доступ при катетеризации воротной вены, так как кон троль возможного кровотечения из пункционного канала не может контро лироваться мануальной компрессией. Обязательная пломбировка хирур гической желатиновой губкой по мере извлечения катетера из печени помогает избежать кровотечений. Бессимптомные артериопортальные внутрипеченочные фистулы в проекции пункционного канала после чре скожной портографии выявляются у 10% больных.
После использования стандартного бедренного и подмышечного доступов редко наблюдается развитие небольших локальных гематом.
Несмотря на перенесение акцента на неинвазивную диагностику состояния печени, селезенки и портальной системы, данные ангиографи ческого исследования в сложных клинических ситуациях способствуют окончательной формулировке диагноза и уточннению характера течения процесса и степени перестройки сосудистых систем гепатолиенальной зо ны при циррозе печени. Низкая частота осложнений при использовании современного инструментария позволяет относить ангиографию к числу методов уточненной диагностики у больных циррозом печени.
а |
б |
Рис. 10.4 Ангиограммы печени больной Г.
а — ангиограмма в аналоговом режиме рентгенографии; б — ангиограмма в режиме "Landmark" c частичным субтрагированием фона рентгеноконтрастного изображения системы общей печеночной артерии
396

Hepato_2003_Last_With_Index.qxd 10.02.2003 18:39 Page 397
АСЦИТИЧЕСКИЙ
СИНДРОМ
Отечно асцитический синдром развивается преимущественно у боль ных циррозом печени. С момента появления перманентного асцита про должительность жизни больного составляет 1–3 года. После появления в брюшной полости асцитической жидкости усугубляются нарушения функ ционального состояния печени, других органов и систем организма, осложняя задачу лечения этой группы больных.
Патогенез асцитического синдрома при портальной гипертензии сло жен и до конца не изучен. Однако в последние годы были получены новые данные об участии различных факторов в развитии асцита у этой категории больных.
Лечение больных циррозом печени, осложненным асцитическим син дромом, до настоящего времени продолжает оставаться одной из трудных проблем современной гепатологии. Считается, что наличие стационарного асцита является противопоказанием к хирургическому лечению, а операции, проведенные в условиях асцита, сопровождаются высокой летальностью.
Предложено много способов купирования резистентных асцитов — от операции Кальба и ее модификаций до сосудистых и органных портоси стемных анастомозов, что свидетельствует об отсутствии достаточного эф фекта от какой либо из них.
Патофизиологические механизмы формирования асцита
В патогенезе асцитического синдрома принимают участие регионар ные и системные факторы. Среди регионарных факторов развития и про грессирования асцита наибольшее значение имеет постсинусоидальный уровень блока при портальной гипертензии и нарушение печеночной лим фодинамики. На системном уровне ведущее значение принадлежит за держке натрия и воды.
Синусоидальная гипертензия
Синусоидальная гипертензия является ключевым понятием при рас смотрении патогенетических аспектов формирования асцита. Данный тер мин следует отличать от более общего синдрома — портальной гипертензии.
397

Hepato_2003_Last_With_Index.qxd 10.02.2003 18:39 Page 398
РУКОВОДСТВО ПО ХИРУРГИИ ПЕЧЕНИ И ЖЕЛЧЕВЫВОДЯЩИХ ПУТЕЙ
Синусоидальная гипертензия определяется не только внутрипеченочной локализацией преимущественного уровня резистентности, но и преобла данием постсинусоидального блока.
В соответствие с законом Старлинга, повышение синусоидального давления является фактором, увеличивающим проникновение элементов плазмы через стенку синусоида в перисинусоидальное простраство Диссе, а затем в лимфатические сосуды.
При отсутствии грубых морфологических изменений в печени в условиях синусоидальной гипертензии онкотический градиент между синусоидом и пространством Диссе малозначим, что связано с высокой проницаемостью для альбумина синусоидального эндотелия. В этих условиях избыточный пе реход жидкости в простраство Диссе обусловлен преимущественно повыше нием синусоидального гидростатического давления.
Прогрессирование цирротического процесса сопровождается ком плексом морфо функцинальных изменений синусоидов, результатом которых является снижение проницаемости эндотелия для альбумина. Это связано с перисинусоидальным отложением коллагена, утратой проницаемости синусоидальным эндотелием, капилляризацией синусоидов. Прогрессиро вание патологического процесса приводит к тому, что пропотевание элементов плазмы в интерстициальное простраство печени определяется как гидростатическим, так и онкотическим градиентами.
Снижение проницаемости «синусоидального» барьера приводит к из менению физико химических свойств печеночной лимфы и асцитической жидкости. Наиболее значимые в клиническом аспекте изменения состава асцитической жидкости связаны со снижением концентрации белка.
Роль портосистемных коллатералей
К сожалению, значению этого фактора в патогенезе асцитического синдрома уделялось незаслуженно мало влияния. Вместе с тем, в литера туре можно встретить достаточное количество фрагментарных упомина ний о формировании индивидуальных патогенетических профилей пор тальной гипертензии. Так, было отмечено, что среди пациентов с цирро зом печени пищеводно желудочное кровотечение развивается лишь у трети больных [Борисов А.Е. и соавт. 2001, Paquet K J, 1995]. У других на протяжении всего наблюдения основной клинической проблемой ос тается асцитический синдром, а геморрагия если и отягощает заболева ние, то обычно развивается в его финале. Еще ни одному автору не уда лось аргументированно объяснить отмеченные факты. Попытки связать закономерности клинического течения портальной гипертензии с уров нем портального давления оказались безуспешными. Один из важных
398

Hepato_2003_Last_With_Index.qxd 10.02.2003 18:39 Page 399
X. ЦИРРОЗ ПЕЧЕНИ И ПОРТАЛЬНАЯ ГИПЕРТЕНЗИЯ
факторов, определяющий патогенетический тип портальной гипертен зии, связан с преимущественным уровнем блока (допеченочный, преси нусоидальный, синусоидальный, постсинусоидальный, надпеченочный). Очевидно, что для асцитообразования необходима именно постсинус оидальная гипертензия.
Даже при схожем типе портальной гипертензии различия могут быть об условлены локализацией и степенью распространения предсуществующих пор тосистемных коллатералей, а также потенциальными возможностями к их ра скытию. Оба этих фактора генетически детерминированы, что вносит существен ный вклад в индивидуальный характер проявлений портальной гипертензии.
Характер клинических проявлений портосистемных коллатералей определяется взаимодействием с другими гемодинамическими факторами. Для возникновения варикозного расширения вен пищевода и желудка необходимы анатомические предпосылки для формирования портоази гального оттока. Обычно это сочетается с хорошо выраженными сосудами спленоренальной зоны. С другой стороны, большой объем портосистемно го шунтирования приводит к нивелированию портальной гипертензии.
Особенности портосистемного шунтирования при циррозе печени влияют на характер кавальной гипертензии. Возрастающий объем шунти рующейся крови при ригидном диафрагмальном кольце приводит к гемоди намической перегрузке нижней полой вены. Развитие периваскулярного отека сопровождается флебитом и перифлебитом, с вовлечением в процесс и устьев печеночных вен. Это может приводить к стенозированию нижней полой вены в области диафрагмального кольца с появлением синдрома Бад да Киари [Борисов А.Е. и соавт., 2000]. Кавальная гипертензия с образова нием надпеченочного постсинусоидального блока создает дополнительные препятствия оттоку крови из печени, усугубляя нарушения портального кро вообращения. Возникает порочный круг, приводящий к декомпенсации как регионарной висцеральной, так и общей венозной гемодинамики.
Таким образом, особенности портосистемного шунтирования могут оказывать влияние на индивидуальный гемодинамический и клинический профиль портальной гипертензии.
Значение лимфатической гипертензии
Печень является одним из главных «генераторов» лимфы в организ ме человека. Приблизительно 50% лимфы, проходящей по грудному про току, образуется в печени.
Печеночная лимфа имеет низкое содержание триглицеридов, что объясняет отличие асцитической жидкости от содержимого брюшной по лости при хилоперитонеуме.
399

Hepato_2003_Last_With_Index.qxd 10.02.2003 18:39 Page 400
РУКОВОДСТВО ПО ХИРУРГИИ ПЕЧЕНИ И ЖЕЛЧЕВЫВОДЯЩИХ ПУТЕЙ
В нормальных условиях существует равновесие между образованием лимфы в печени и ее адекватным оттоком. Развитие цирроза печени явля ется классическим примером нарушения данного равновесия, поскольку в этом случае происходит как увеличение продукции лимфы, так и наруше ние ее адекватного оттока из печени.
Причиной нарушения равновесия лимфатической системы является постсинусоидальный блок оттока, формирующийся при циррозе печени. При циррозе количество лимфы, оттекающей из печени, может увеличи ваться до 2000–9000 мл в сутки. Это приводит к расширению лимфатиче ских сосудов по основным и дополнительным путям оттока лимфы. Богатая белком лимфа проникает в брюшную полость через эти тонкостенные лимфатические сосуды, а также через глиссонову капсулу из находящихся под ней расширенных лимфатических коллекторов.
Главной лимфатической магистралью в организме человека является грудной проток, собирающий лимфу из органов живота, грудной полости, шеи, головы, конечностей. Повышенная продукция лимфы, имеющая ме сто при циррозе печени, ведет к усиленному «сбросу» ее в грудной проток. В начальных стадиях заболевания отмечается ускорение тока лимфы по протоку, увеличение ее дебита. Наряду с этим, происходит повышение да вления лимфы в протоке и расширение его в диаметре без существенного нарушения его дренажной способности. В этот период проявляется важ ная компенсаторная роль грудного протока. Когда количество продуциру емой лимфы начинает превосходить дренажную способность грудного про тока, создаются условия для асцитообразования. Таким образом, суще ствует «функциональная резистентность» терминальной части грудного протока, играющяя важную роль в патогенезе асцита при циррозе печени.
Роль висцеральной лимфодинамики
Прогрессирование портальной гипертензии вызывает резкие измене ния не только в лимфатической системе печени, но и нарушения лимфоди намики во всех органах брюшной полости и париетальной брюшине.
В отличие от печеночных синусоидов, патофизиологические гипертен зивные изменения, затрагивающие интестинальные капилляры, не способ ствуют активному асцитообразованию. Имеются доказательства снижения площади интестинального капиллярного обмена вследствие портальной ги пертензии. Роль гиперпродукции спланхнической лимфы может несколько повыситься при выраженной гипоальбуминемии и снижении онкотическо го градиента, что может иметь место на поздних стадиях цирроза печени, при печеночной недостаточности или в постгеморрагическом периоде. Большинство данных свидетельствует о малой значимости изменений ме
400
