- •Группы риска по развитию рахита.
- •Лекарственные препараты витамина д:
- •Рекомендации по дозам холекальциферола для профилактики гиповитаминоза д
- •Патогенез
- •Клиника
- •Диагностика
- •Лечение
- •3.Гипервитаминоз д. Причины. Патогенез. Клинические формы. Диагностика. Дифференциальная диагностика. Лечение. Осложнения
- •Этиология
- •Патогенез
- •Клиника
- •Диагностика
- •Дифференциальный диагноз
- •Лечение
- •Осложнения и исход
- •4.Атопический дерматит. Этиология. Патогенез. Клиника. Диагностика. Дифференциальный диагноз. Современные принципы терапии. Исходы. Атопический дерматит
- •Этиология
- •Патогенез
- •Диагностика
- •Дифференциальная диагностика
- •Лечение
- •5.Токсикоз у детей раннего возраста. Этиология. Патогенез. Клиника. Диагностика. Дифференциальный диагноз. Современные принципы терапии. Исходы
- •7.Хронические расстройства питания. Питания (гипотрофия, паратрофия, гипостатура). Классификация. Этиология. Патогенез. Клиника. Диагностика. Лечение хронические расстройства питания
- •Этиология
- •Классификация хронических расстройств питания у детей раннего возраста (г. И.Зайцева, л. А. Строганова, 1981):
- •Основные клинические проявления гипотрофии у детей раннего возраста
- •Этиология
- •Патогенез
- •Клинические проявления
- •Диагноз и дифференциальный диагноз
- •Диагностика
- •Принципы диетотерапии у больных гипотрофией в период выяснения толерантности к пище
- •8.Железодефицитная анемия у детей раннего возраста. Этиология. Патогенез. Классификация. Клиника. Диагностика. Дифференциальная диагностика. Лечение. Профилактика железодефицитная анемия
- •Этиология
- •Патогенез
- •9.Острые пневмонии у детей раннего возраста. Этиология. Патогенез. Классификация. Клинические проявления пневмоний различных форм. Диагностика. Лечение. Осложнения
- •Типичные ошибки
- •10. Деструктивная пневмония у детей раннего возраста. Этиология. Клиника. Особенности клинического течения и диагностики в зависимости от этиологии пневмонии. Диагностика. Лечение
- •Лечение:
- •11. Острый бронхит у детей раннего возраста. Этиология. Патогенез. Классификация. Особенности проявлений в зависимости от клинических форм. Диагностика. Лечение
- •Этиология
- •Классификация впс
- •Диагностика впс
- •Критерии степени тяжести ба
- •Дифференциальная диагностика ба и обструктивного бронхита у детей раннего возраста
- •Этиология
- •Патогенез
- •Клиническая картина
- •Диагностика
- •Лечение
- •18.Хронические гастриты и гастродуодениты: классификация, этиология, патогенез. Клиника, диагностика, лечение. Диспансерное наблюдение. Хронический гастрит, гастродуоденит
- •20.Острый и хронический гломерулонефрит: этиология, патогенез, классификация. Клинические проявления различных форм. Дифференциальная диагностика. Принципы лечения различных форм.
- •21. Острый пиелонефрит: этиология, патогенез, классификация. Особенности клинической картины у детей различного возраста. Диагностика. Принципы лечения
- •Классификация пиелонефрита у детей (м.Я. Студеникин и соавт., 1980 г. С дополнениями в.Г. Майданника и соавт., 2002)
- •26.Врождённая дисфункция коры надпочечников (адреногенитальный синдром). Классификация. Клиника вирильной и сольтеряющей форм. Дифференциальный диагноз. Неонатальный скрининг. Лечение и профилактика.
- •Жалобы и анамнез
- •Физикальное обследование
- •Лабораторная диагностика
- •3.3Терапия радиоактивным йодом
- •4. Узловой/многоузловой зоб, диагностика у взрослых и детей
- •5. Узловой/многоузловой зоб, лечение у взрослых и детей
- •28.Тиреоидные гормоны их физиологическая роль в различные периоды онтогенеза. Симптомы гипо – и гипертиреоза у детей.
- •29.Диффузный токсический зоб у детей и подростков. Этиология. Патогенез. Клинические синдромы. Диагностика. Лечение. Диспансерное наблюдение.
- •4.Лечение
- •30.Гипотиреоз у детей и подростков. Классификация, патогенез первичного и вторичного гипотиреоза. Клинические синдромы. Лечение и профилактика. Критерии эффективности лечения гипотиреоза.
- •31.Врожденный гипотиреоз. Группа риска. Клинические признаки в периоде новорожденности. Скрининг новорожденных. Критерии диагноза
- •II этап — медико-генетическая лаборатория
- •32.Определение понятия «ожирение». Классификация. Конституционально-экзогенное и гипоталамическое ожирение. Этиология. Клинические проявления. Дифференциальный диагноз. Лечение. Прогноз.
- •2. Диагностика
- •2.4 Инструментальная диагностика
- •33.Критерии оценки физического развития. Нарушение роста у детей. Гипофизарный нанизм. Гигантизм. Низкорослость. Дифференциальный диагноз. Лечение. Прогноз.
- •35. Хроническая недостаточность коры надпочечников. Этиология. Патогенез, клиническая картина. Неотложная помощь. Лечение. Прогноз.
- •36. Болезнь и синдром Иценко-Кушинга. Определение. Этиология. Клиническая картина. Осложнения. Диагностика. Дифференциальный диагноз. Лечение.
33.Критерии оценки физического развития. Нарушение роста у детей. Гипофизарный нанизм. Гигантизм. Низкорослость. Дифференциальный диагноз. Лечение. Прогноз.
Физическое развитие
Физическое развитие (ФР) - динамический процесс роста (увеличение длины, массы тела, развитие отдельных частей тела и др.) и биологического созревания ребёнка в том или ином периоде детства. Основной показатель ФР - рост. Выделяют четыре группы признаков ФР (табл. 2.7).
Таблица 2.7. Группы признаков физического развития
Признаки |
Показатель |
Антропометрические |
Длина тела, масса, окружности головы, груди, плеча, бедра, голени |
Функциональные |
Жизненная ёмкость лёгких, кистевая и становая сила, физическая работоспособность и т.п. |
Соматоскопические |
Форма позвоночника, степень жироотложения, развитие мускулатуры, осанка, форма конечностей и т.д. |
Биологические |
Зубная формула, пропорции тела, линейный рост, развитие вторичных половых признаков |
Дефицит антидиуретического гормона (вазопрессина) способствует возникновению несахарного диабета центрального генеза, развивающегося, как правило, вследствие оперативного лечения опухолей гипоталамо-гипофизарной области. Его клинико-лабораторные проявления: полиурия, полидипсия, никтурия, энурез.
Критерии диагностики:
• полиурия (суточный диурез - 2-20 л);
• осмоляльность мочи ниже 200 мосм/л, низкий удельный вес мочи (<1005), при этом цвет мочи варьирует от светло-желтого до бесцветного;
• уровень натрия в плазме (осмоляльность плазмы) нормальный или слегка повышен;
• уровень антидиуретического гормона в плазме снижен и не соответствует ее осмоляльности.
В целях уточнения диагноза проводят тест с ограничением выпиваемой жидкости. При несахарном диабете повышения осмоляльности мочи и уменьшения ее количества не происходит, + наличие низкого удельного веса мочи во всех пробах анализа мочи по Зимницкому.
Нарушения роста у детей – группа заболеваний различной этиологии, сопровождающихся отклонением показателей физического развития ребенка от возрастных норм. Чаще проявляется задержкой роста, намного реже встречаются заболевания, приводящие к ускоренному росту. Нарушения роста у детей почти всегда сопровождаются симптоматикой со стороны сердечно-сосудистой системы и желудочно-кишечного тракта (в зависимости от этиологии). Проводится оценка физического развития на основании специально разработанных таблиц, а также комплексная лабораторная диагностика. Лечение этиотропное, применяется заместительная гормональная терапия, нейрохирургические и другие операции.
Причины и классификация нарушений роста у детей
Часть заболеваний связана с эндокринными нарушениями. Это могут быть патологии метаболизма соматотропина, его недостаточное или избыточное образование либо изменение чувствительности периферических рецепторов к данному гормону, нарушения роста у детей встречается при патологиях обмена других гормонов, в частности, гормонов щитовидной железы, надпочечников, половых гормонов и некоторых центральных гормонов, таких как АКТГ и рилизинг-факторы.
Некоторые соматические патологии тоже могут являться причиной нарушений роста у детей. Прежде всего, это группа скелетных дисплазий и хромосомных заболеваний, сопровождающихся низкорослостью. Патологии почек, печени и желудочно-кишечного тракта также иногда сопровождаются задержкой роста. Обычно это связано с недостаточностью питания (нерациональная диета, голодание) или усвоения пищи. Вместе с тем, печень опосредованно участвует в процессе роста ребенка, поскольку именно здесь под влиянием соматотропного гормона образуются инсулиноподобные факторы роста, которые напрямую воздействуют на клетки-мишени, запуская анаболические реакции.
Симптомы нарушений роста у детей
Стоит отметить, что задержка роста встречается гораздо чаще, нежели ускоренный рост и развитие. В случае задержки внутриутробного развития сразу после рождения ребенка можно заметить, что параметры его физического развития в той или иной степени отстают от нормы. Однако чаще заподозрить нарушения роста у детей можно примерно с 3-4 лет, когда есть возможность проследить динамику роста. Как правило, с этого времени отставание определяется не только педиатром, но и родителями малыша. Это может быть пропорциональная задержка роста (туловище и конечности равномерно отстают в размерах от возрастной нормы) и диспропорциональная форма (конечности либо короткие, либо длинные по отношению к туловищу).
Хромосомные синдромы, в клинике которых присутствуют нарушения роста у детей, также проявляются специфическими изменениями внешности (например, синдром Дауна или синдром Шерешевского-Тернера).
. Недостаточность гормональной функции щитовидной железы, помимо низкорослости, проявляется характерной вялостью ребенка, низким артериальным давлением и брадикардией, при гиперфункции железы симптомы противоположны, рост ускорен.
Половые гормоны в некоторой степени потенцируют физическое развитие ребенка. Они участвуют в образовании ядер окостенения и закрытии зон роста в эпифизах костей по окончании пубертатного периода.
Диагностика нарушений роста у детей
Существуют определенные нормативы– центильные таблицы, содержащие количественные границы роста, веса и других показателей для детей разных возрастов. Если показатели пациента на протяжении одного-двух лет выходят за рамки, указанные для конкретного возраста, можно говорить об ускорении или задержке физического развития.
1.На начальном этапе исключают любые соматические патологии, способные вызывать нарушения роста у детей.
Проводят ЭКГ и ЭхоКГ-диагностику для оценки состояния сердечно-сосудистой системы. Патологии желудочно-кишечного тракта диагностируют на основании результатов биохимического анализа крови, абдоминального УЗИ и рентгенологического исследования (по показаниям).
Далее выполняют лабораторное исследование функции щитовидной и других периферических желез, поскольку технически периферические железы исследовать проще, чем центральные. Определяют уровень тироксина, глюкокортикоидов, половых гормонов. Это позволяет обнаружить возможное снижение или повышение функции какой-либо из этих желез внутренней секреции и начать соответствующую терапию. Если у ребенка не выявлено отклонений от нормы, осуществляют скрининг дефицита или избытка соматотропного гормона и инсулиноподобных факторов роста. Помимо лабораторной диагностики, на данном этапе проводят определение костного возраста (R-грамма кисти и лучезапястного сустава), МРТ головного мозга ребенку и исследование кариотипа.
При подозрении на нарушения роста у детей, связанные с метаболизмом соматотропина, выполняют однократное измерение уровня его базальной секреции, а также несколько стимуляционных тестов. Дефицит соматотропного гормона подтверждается при уровне стимулированной секреции ниже 7 нг/мл. Концентрация 7-10 нг/мл свидетельствует о частичном дефиците соматотропина. Такой результат обычно говорит в пользу точечной мутации гена гормона роста. Наряду с этим проводится определение концентраций пролактина и тиреотропного гормона, поскольку при некоторых опухолях и генетических мутациях имеет место множественная недостаточность гипофизарных гормонов. Тесты высокоинформативны и позволяют врачу определиться с тактикой лечения.
Лечение и прогноз нарушений роста у детей
Проводится этиотропная терапия заболеваний. Если нарушения роста у детей связаны с гормональными причинами, назначается заместительная гормональная терапия, либо используются антагонисты гормонов, которые синтезируются в избыточном количестве. Для лечения соматотропной недостаточности применяется синтетический соматотропин. Большинство гормонопродуцирующих опухолей можно удалить хирургическим путем. Как правило, рецидивы подобных новообразований встречаются редко. Нарушения роста у детей с соматическими заболеваниями корригируются по показаниям, однако в большинстве случаев лечение основного заболевания приводит к нормализации физического развития. Всем детям обязательно назначается полноценная диета и витаминотерапия.
Прогноз чаще благоприятный. В большинстве случаев удается компенсировать недостаточность соматотропного и других гормонов. Одним из важнейших факторов успешного лечения является своевременная диагностика нарушений роста у детей, а она очень часто невозможна ввиду слабой выраженности отклонений от нормы либо присутствия других, более опасных симптомов. Малейшая задержка в терапевтической коррекции физического развития может привести к резкому снижению чувствительности организма к лечению. Кроме того, некоторые причины нарушений роста у детей, например, хромосомные заболевания, устранить невозможно.
гипофизарный нанизм
– эндокринное заболевание, в основе которого лежит нарушение синтеза гормона роста (соматотропина) в передней доле гипофиза, что приводит к задержке роста скелета, внутренних органов и физическому недоразвитию. Гипофизарный нанизм характеризуется аномальной низкорослостью: рост мужчин ниже 130 см, рост женщин ниже 120 см; отмечается отставание в развитии костно-мышечной системы, гипогонадизм, уменьшение размеров внутренних органов, гипотензия, брадикардия и др.
Диагностика гипофизарного нанизма предполагает определение базальной концентрации СТГ в сыворотке крови, проведение фармакологических проб, рентгенографии черепа, кистей рук и лучезапястных суставов.
Лечение гипофизарного нанизма включает заместительную терапию соматотропином, анаболическими стероидами, тиреоидными препаратами, половыми гормонами
Гипофизарный нанизм – клинический синдром, обусловленный абсолютной или относительной соматотропной недостаточностью гипофиза (недостатком секреции соматотропного гормона или нарушением тканевой чувствительности к нему). Понятием нанизм (микросомия, наносомия, карликовость) в широком смысле обозначают ряд патологических состояний, выражающихся в отставании роста и физического развития по сравнению со средней возрастной, половой, популяционной и расовой нормой. Нанизм может являться самостоятельным генетическим заболеванием или выступать симптомом ряда эндокринных и неэндокринных заболеваний.
Причины
Соматотропная недостаточность, лежащая в основе гипофизарного нанизма, может быть обусловлена тремя группами причин: врожденным дефицитом соматотропного гормона (СТГ), приобретенным гипосоматотропным состоянием и периферической резистентностью тканей к воздействию СТГ.
1. Врожденная недостаточность соматотропина может быть связана с генетическими дефектами (мутацией гена гормона роста, мутацией гена рецептора к соматолиберину и др.) либо аномалиями развития гипоталамо-гипофизарной системы (анэнцефалией, врожденной аплазией, гипоплазией или эктопией гипофиза).
2. Приобретенный гипофизарный нанизм развивается при:
Опухолях гипоталамо-гипофизарной области (краниофарингиоме, гамартоме, нейрофиброме, герминоме, аденоме гипофиза) или других отделов головного мозга (например, глиоме зрительного перекреста).
Травмах мозга. В некоторых случаях к гипофизарному нанизму могут приводить черепно-мозговые травмы, родовые травмы, повреждение ножки гипофиза при хирургических вмешательствах,
Прочих церебральных заболеваниях: нейроинфекциях (вирусные, бактериальные энцефалиты и менингиты),аутоиммунном гипофизите, гидроцефалии, аневризмах сосудов гипофиза и т. д.
Токсическом поражением гипофиза. последствиями химиотерапии или облучения (при лейкемии, ретинобластоме, пересадке костного мозга и т. д.).
3. Гипофизарный нанизм вследствие нечувствительности тканей-мишеней к гормону роста может развиваться при дефиците СТГ-рецепторов, отсутствии биологической активности соматотропного гормона, резистентности к инсулиноподобному фактору роста 1.
Наряду с изолированной недостаточностью СТГ, при гипофизарном нанизме может отмечаться снижение синтеза других гормонов гипофиза: гонадотропинов, ТТГ, АКТГ, что сопровождается недостаточностью функции соответствующих периферических эндокринных желез (половых, щитовидной, надпочечников), что также влияет на рост и физическое развитие. В этом случае в эндокринологии говорят о пангипопитуитарной форме карликовости.
Классификация
Различают нанизм с пропорциональным и непропорциональным телосложением.
От случаев нанизма следует отличать семейные (конституциональные) формы низкорослости, которые рассматриваются как вариант индивидуального физического развития и не являются патологией.
Симптомы гипофизарного нанизма
Дети рождаются с нормальными весоростовыми показателями. Задержка роста при врожденном гипофизарном нанизме обычно становится заметна к возрасту 2-3 лет и в дальнейшем нарастает. Скорость роста у детей с гипофизарным нанизмом составляет 1,5-2 см в год (при норме – 7-8 см). У взрослых мужчин рост не превышает 130 см, у женщин - 120 см. Телосложение пропорциональное, однако могут сохраняться пропорции, свойственные детскому возрасту.
Кожные покровы у пациентов с гипофизарным нанизмом бледные, сухие, морщинистые, с желтоватым или мраморным оттенком, что обусловлено тиреоидной недостаточностью. Волосы на голове часто тонкие, сухие, ломкие. Недоразвитие костей лицевого черепа обусловливает наличие мелких черт лица («кукольное лицо»), западение переносицы.
Распределение подкожно-жировой клетчатки может быть различным – от слабого развития до избыточного отложения жира по «кушингоидному» типу (на груди, животе, бедрах). Отмечается задержка окостенения скелета, слабое развитие мышечной системы, нарушение смены зубов. Из-за недоразвития гортани у взрослых с гипофизарным нанизмом сохраняется высокий детский тембр голоса. В соответствии с низким ростом и массой тела отмечается уменьшение размеров внутренних органов (спланхномикрия). Нередко при гипофизарном нанизме выявляется брадикардия и артериальная гипотензия.
Нарушение гонадотропной функции гипофиза приводит к задержке и неполноценности полового развития (гипогонадизму). У юношей с гипофизарным нанизмом наблюдается отсутствие оволосения по мужскому типу, гипоплазия яичек, крипторхизм, микропенис; у девушек - аменорея, микромастия, гипоплазия матки и яичников.
Интеллектуальное развитие при гипофизарном нанизме, как правило, сохранно. Могут отмечаться такие психологические особенности, как негативизм, замкнутость, снижение самооценки, инфантильное поведение. При наличии дополнительных жалоб на головную боль, рвоту, нарушение зрения следует заподозрить внутричерепную патологию. При пангипопитуитарном нанизме определяются признаки вторичного гипокортицизма и гипотиреоза.
Диагностика
Антропометрия
Основная роль при диагностике гипофизарного нанизма принадлежит определению базального уровня СТГ в сыворотке крови, циркадного ритма секреции и резервов на фоне стимуляции. У пациентов с гипофизарным нанизмом исходный уровень СТГ значительно снижен, при проведении стимулирующих тестов с инсулином, тиреолиберином, аргинином и др. повышается незначительно.
Рентгенография турецкого седла выявляет его детскую форму («стоячий овал») и широкую (т. н. ювенильную) спинку. При увеличении размеров турецкого седла и наличии участков обызвествления, в первую очередь, следует думать об опухоли.
Рентгенография лучезапястных суставов и кистей позволяет определить рентгенологический («костный») возраст. При гипофизарном нанизме отмечается значительное замедление процессов окостенения скелета.
Для выяснения формы нанизма необходимо исследование инсулиноподобного фактора роста (соматомедина-С), ТТГ, ЛГ, ФСГ, Т3, Т4, кортизола в плазме и моче, антител к тиреоглобулину, микросомальной фракции тироцитов и др. Для исключения опухолевого поражения проводится КТ (МРТ) головного мозга.
Кариотипирование. У всех девочек с низкорослостью (рост < -2,0 SDS), даже в возрасте младше 2 лет, вне зависимости от наличия или отсутствия клинической симптоматики синдрома Шерешевского- Тернера, необходимо исследовать кариотип.
Молекулярно-генетическое исследование. Исследуют гены, участвующие в формировании гипоталамо-гипофизарной оси, развитии передней доли гипофиза, регулирующие синтез и секрецию гормона роста. У пациентов с изолированным дефицитом гормона роста - GH-1, у пациентов с множественным дефицитом гормонов аденогипофиза - HESX-1, LHX-3, PROP1, POU1F1
При гипофизарном нанизме пациент должен быть проконсультирован эндокринологом, гинекологом (женщины), андрологом (мужчины), неврологом или нейрохирургом, офтальмологом, генетиком.
Лечение гипофизарного нанизма
У детей младшего возраста для исключения диагностических ошибок на протяжении 6-12 мес. выдерживают период наблюдения, во время которого особое внимание уделяется полноценному питанию, общеукрепляющей терапии, приему витаминов (А и D) и минералов (фосфора, кальция). Отсутствие динамики роста и физического развития является основанием для перехода к гормонотерапии.
Основу патогенетического лечения гипофизарного нанизма составляет заместительная терапия препаратами гормона роста, которая проводится прерывистыми курсами (по 2-3 мес. с такими же интервалами). Соматотропин человека назначается пациентам с доказанной эндогенной недостаточностью гормона и дифференцировкой скелета, не превышающей возрастных показателей 13-14 лет. Лечение с помощью СТГ проводится до закрытия зон роста или до достижения приемлемых ростовых параметров.
В терапии гипофизарного нанизма применяются анаболические стероиды (метандиенон, нандролон), оказывающие стимулирующее действие на уровень эндогенного СТГ, синтез белков и рост. Лечение стероидными гормонами продолжается несколько лет с периодической заменой препаратов. Лечение анаболическими средствами целесообразно начинать с 5-7 лет. Для стимуляции функции половых желез в возрасте старше 16 лет юношам назначается хорионический гонадотропин и малые дозы андрогенов, девушкам - малые дозы эстрогенов.
В дальнейшем, после закрытия зон роста, пациентов с гипофизарным нанизмом переводят на постоянный прием половых гормонов в соответствии половой принадлежностью. При этом женщинам показан прием комбинированных эстрогенгестагенных препаратов, мужчинам - андрогенов пролонгированного действия.
При гипотиреозе назначается L–тироксин, тиреоидин; при недостаточности соматолиберина - его синтетические аналоги; при гипофункции коры надпочечников - глюкокортикостероиды. При органической патологии ЦНС может потребоваться противовоспалительная, рассасывающая, дегидратационная терапия. В случае выявления опухолей гипофиза показано их хирургическое удаление, иногда – проведение лучевой терапии.
Гигантизм – патологическая высокорослость, обусловленная чрезмерной выработкой гормона роста (соматотропного гормона) передней долей гипофиза и проявляющаяся уже в детском возрасте. Наблюдается увеличение роста свыше 2 м, непропорциональность телосложения с преимущественным удлинением конечностей, при этом голова кажется очень маленькой. У больных наблюдается расстройство физического и психического состояния, половой функции. При гигантизме трудоспособность ограничена, высок риск бесплодия. Основным диагностическим критерием гигантизма, помимо яркой клинической картины, является выявление повышения СТГ в крови.
Гигантизм (или макросомия) развивается у детей с незавершенными процессами окостенения скелета, чаще встречается у подростков мужского пола, определяется уже в возрасте 9-13 лет и прогрессирует на протяжении всего периода физиологического роста. При гигантизме скорость роста ребенка и его показатели намного превышают анатомо-физиологическую норму и к концу пубертатного периода достигают более 1,9 м у женщин и 2 м у мужчин при сохранении относительно пропорционального телосложения.
Причины гигантизма
Гигантизм и акромегалия являются двумя возрастными вариациями одних и тех же патологических процессов: гиперплазии и гиперфункции клеток гипофиза, продуцирующего соматотропный гормон (гормон роста). Повышенная секреция гормона роста может наблюдаться при поражениях гипофиза в результате опухолей железы (аденомы гипофиза), интоксикации, нейроинфекций (энцефалита, менингита, менингоэнцефалита),
черепно-мозговых травм.
Нередко причиной гигантизма служит понижение чувствительности эпифизарных хрящей, обеспечивающих рост костей в длину, к воздействию половых гормонов. В результате этого кости долго сохраняют способность увеличения в длину, даже в постпубертатном периоде. Гиперсекреция соматотропина после закрытия зон роста костей и завершения окостенения скелета приводит к акромегалии.
Симптомы гигантизма
Скачок увеличения длины тела при гигантизме происходит в 10-15 лет. Пациенты отличаются высоким ростом и темпами его увеличения, жалуются на быструю утомляемость и слабость, головокружения, головные боли, ухудшение зрения, боли в суставах и костях. Снижение памяти и работоспособности ведет к ухудшению успеваемости в школе. Гигантизм характеризуется гормональными нарушениями, расстройством психической и половой функции (инфантилизм). У женщин при гигантизме развивается первичная аменорея или раннее прекращение менструальной функции, бесплодие, у мужчин - гипогонадизм. Другими гормональными проявлениями гигантизма служат несахарный диабет, гипо- или гипертиреоз, сахарный диабет. Отмечается сначала увеличение мышечной силы, а затем мышечная слабость и астения.
При гигантизме возможно развитие артериальной гипертензии, миокардиодистрофии, сердечной недостаточности, эмфиземы легких, дистрофических изменений печени, бесплодия, сахарного диабета, нарушений функции щитовидной железы.
Диагностика гигантизма
Диагноз гигантизма устанавливается на основании внешнего осмотра пациента, результатов лабораторных, рентгенологических, неврологических и офтальмологических исследований. При гигантизме лабораторно определяется высокое содержание СТГ в крови.
Для выявления опухолей гипофиза проводится рентгенография черепа, КТ и МРТ головного мозга. При наличии аденомы гипофиза определяется увеличенное турецкое седло (ложе гипофиза). Рентгенограммы кистей рук показывают несоответствие между костным и паспортным возрастом. При офтальмологическом обследовании пациентов с гигантизмом выявляется ограничение зрительных полей, застойные явления в глазном дне.
Лечение гигантизма
Принципы лечения гигантизма аналогичны лечению акромегалии. Для нормализации уровня гормона роста при гигантизме применяются аналоги соматостатина, для более быстрого закрытия зон роста костей - половые гормоны. Этиологическое лечение гигантизма при аденомах гипофиза предусматривает применение лучевой терапии или их оперативное удаление в сочетании с медикаментозной поддержкой агонистами дофамина.
При евнухоидном типе гигантизма лечение направлено на устранение полового инфантилизма, ускорение окостенения скелета и прекращение его дальнейшего роста. Лечение частичного гигантизма включает ортопедическую коррекцию при помощи пластических операций.
Прогноз и профилактика гигантизма
При адекватной терапии гигантизма прогноз для жизни относительно благоприятный. Однако, многие пациенты не доживают до старости и погибают от осложнений заболевания. Большинство пациентов, страдающих гигантизмом, бесплодны, их трудоспособность резко снижена.
Обеспокоенность родителей должно вызывать резкое, значительное увеличение роста ребенка в период полового созревания по сравнению с его сверстниками. Своевременное медицинское вмешательство позволит предотвратить осложнения.
Низкорослость (дефицит роста) – рост ниже 3 перцентили или ниже 2 стандартных отклонений (< -2.0 SDS) от популяционной средней для данного хронологического возраста и пол

Диагностика
Жалобы родителей и/или ребенка:
• на отставание в росте.
Анамнез:
• уточнить рост других членов семьи – родителей, братьев и сестер ребенка;
• темпы роста родителей в детстве;
• длина и масса тела ребенка при рождении;
• возраст, в котором впервые замечено снижение темпов роста ребенка.
Физикальное обследование:
• отставание длины тела ребенка от средних показателей более чем на 2 SDS;
• стигмы дизэмбриогенеза («готическое» небо, низкий рост волос на шее, крыловидные складки шеи, антимонголоидный разрез глаз, широкая грудная клетка, отек тыла стоп и др.)
• клинические признаки дефицита выработки тропных гормонов гипофиза: синдромы гипотиреоза, гипокортицизма, гипогонадизма.
Лабораторные исследования:
• Снижение уровня ИРФ-1 в крови при СТГ-недостаточности;
• Кариотип 45Х0 – при синдроме Шерешевского-Тернера;
• Снижение в крови уровней ТТГ и свТ4 при сопутствующем вторичном гипотиреозе;
• Снижение уровней АКТГ и кортизола при сопутствующем вторичном гипокортицизме;
• Снижение уровней ЛГ, ФСГ, тестостерона при сопутствующем вторичном гипогонадизме у мальчиков,
• Снижение уровней ЛГ, ФСГ эстрадиола при сопутствующем вторичном гипогонадизме у девочек;
• При СТГ-недостаточности проведение стимуляционных тестов с инсулином и клофелином выявляет недостаточный выброс СТГ.
• Отсутствие генов Prop-1, Pit-1 или их дефектность указывают на генетическую обусловленность СТГ-недостаточности.
Инструментальные исследования:
• отставание костного возраста на 2 и более лет при рентгенографии левой кисти с лучезапястным суставом указывает на эндокринный генез низкорослости;
• изменения в области гипоталамуса и гипофиза при МРТ с контрастным усилением свидетельствуют об органической природе дефицита СТГ;
• отсутствие яичников и гипо-, аплазия матки и труб по данным УЗИ органов малого таза у девочек подтверждает наличие синдрома Шерешевского-Тернера;
• гипоплазия яичек по данным УЗИ у мальчиков подтверждает наличие сопутствующего вторичного гипогонадизма.
Тактика лечения
Немедикаментозное лечение
• высокая физическая активность;
• полноценное питание;
• достаточной продолжительности ночной сон;
• профессиональная психологическая поддержка ребенка.
Медикаментозное лечение Тактика медикаментозного лечения определяется причиной низкорослости. СТГ-недостаточность, синдром Шерешевского-Тернера, ЗВУР, синдром Прадера – Вилли, дефицит SHOX-гена являются показаниями для назначения одного из препаратов генноинженерного человеческого гормона роста – соматропина [4,5,6].
С учетом суточного физиологического ритма препараты гормона роста следует вводить 1 раз в сутки перед сном - в 22.00.
Заместительная терапия соматропином продолжается до достижения прогнозируемого (целевого) роста, который высчитывается по формулам:
для мальчиков: рост отца + рост матери/ 2 + 6,5 см,
для девочек: рост отца + рост матери/ 2 - 6,5 см
При эндокриннозависимых вариантах низкорослости, обусловленных гипотиреозом, гипогонадизмом, гипокортицизмом, болезнью Иценко-Кушинга и др. проводится терапия основного заболевания (см. соответствующие клинические протоколы).
Дети с эндокринно-независимыми формами не нуждаются в какой-либо заместительной гормональной терапии, назначается терапия основного заболевания.
Медикаментозное лечение, оказываемое на амбулаторном уровне
Перечень основных лекарственных средств (имеющих 100% вероятность применения):
• соматропин шприц-ручка; флакон;
34. Половое развитие. Варианты нарушения полового развития. Понятие о преждевременном половом развитии. Клиника, дифференциальный диагноз.
Выделяют две группы половых нарушений: нарушение дифференцировки пола и нарушение темпов полового развития (преждевременное развитие и задержка).
Гормональная регуляция полового созревания
Функционирование репродуктивной системы человека регулируется ЦНС.
Гипоталамус синтезирует гонадотропин-релизинг-гормон, или гонадотропин, который в допубертатном периоде вырабатывается в постоянном режиме, при возникновении импульсной секреции (вызванной активацией нейромедиаторов), инициирует пубертат.
Под влиянием гонадотропина передняя доля гипофиза вырабатывает фол-ликулостимулирующий гормон (ФСГ) и лютеинизирующий гормон (ЛГ). ЛГ стимулирует образование андрогенов в клетках Лейдига у мужчин и в текаклетках фолликулов у женщин. ФСГ обеспечивает созревание гранулёзы фолликулов в яичниках у женщин и ароматизирование в ней андрогенов в эстрогены; у мужчин - регулирует сперматогенез.
Андрогены воздействуют на дифференцировку и развитие мужских половых органов, мужское половое поведение, активизируют синтез белка в мышцах, усиливают активность потовых и сальных желёз, активируют волосяные фолликулы.
Эстрогены способствуют увеличению размеров влагалища и матки, стимулируют развитие молочных желёз, перераспределяют жир в организме по женскому типу, повышают минерализацию костей.
Половое созревание начинается не ранее 8 лет у девочек и 9 лет у мальчиков. Этот процесс включает:
• пубертатный скачок роста (спурт);
• изменение состава тканей организма;
• изменения концентрации половых гормонов, рост гонад; появление вторичных половых признаков.
Клинически важно оценить сроки и последовательность появления вторичных половых признаков.
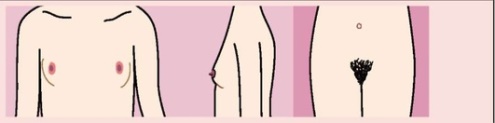
Время появления вторичных половых признаков индивидуально и зависит от многих факторов. Порядок появления вторичных половых признаков в норме у детей разного пола представлен на рис. 10.17.
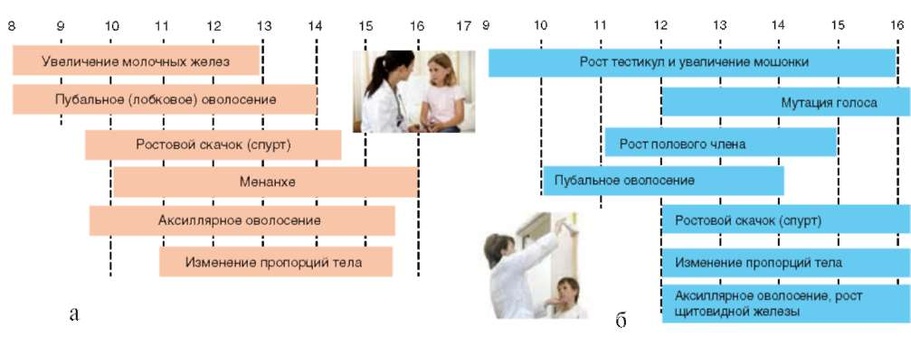
Оценку полового развития мальчиков и девочек проводят по шкале Д. Taн- нepa (1968) (табл. 10.24).
Таблица 10.24. Оценка полового развития мальчиков и девочек по шкале Д. Tаннера (1968)
Девочки |
||
Стадия |
Развитие грудных желёз |
Лобковое и аксиллярное оволосение |
I |
Πрепубертатное; увеличение только соска |
Πрепубертатное; отсутствие волос |
|
|
|
II |
Уплотнение грудных желёз заметно или пальпируется; увеличение ареол |
Редкие волосы, длинные, прямые или слегка вьющиеся, минимум пигментированных волос, в основном на половых губах |
|
|
|
III |
Дальнейшее увеличение грудных желёз и ареол без выделения контуров |
Более тёмные и грубые волосы, распространяющиеся по лобку, аксиллярное оволосение в центре подмышечной впадины |
|
|
|
IV |
Выступание ареолы и соска над грудной железой |
Густые, взрослого типа волосы, не распространяющиеся на медиальную поверхность бедер. Аксиллярное оволосение в центре подмышечной впадины
|
|
|
|
Продолжение табл. 10.23
Девочки |
||
Стадия |
Развитие грудных желёз |
Лобковое и аксиллярное оволосение |
V |
Взрослые контуры грудной железы с выступанием только соска |
Волосы взрослого типа, распространяющиеся в форме классического треугольника. Аксиллярное оволосение по всей подмышечной впадине |
|
|
|
Мальчики |
||
Стадия |
Развитие половых органов |
Лобковое и аксиллярное оволосение |
I |
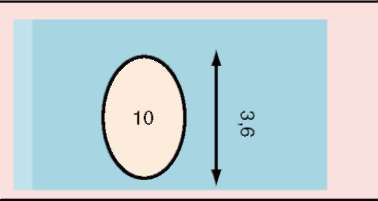
Πрепубертатная длина яичек менее 2,5 см |
Отсутствует. На животе могут быть пушковые волосы. |
|
|
|
II |
Яичко больше 2,5 см в длину. Мошонка тонкая и красноватая |
Редкие, длинные, тонкие прямые или слегка вьющиеся, слабо пигментированные волосы; главным образом у корня полового члена, аксиллярное оволосение отсутствует |
|
|
|
III |
Рост полового члена в длину и ширину и дальнейший рост яичек |
Волосы темнеют утолщаются, становятся вьющимися и распространяются на лобок, единичные пигментированные волосы в центре подмышечной впадины |
|
|
|
Окончание табл. 10.23
Мальчики |
||
Стадия |
Развитие половых органов |
Лобковое и аксиллярное оволосение |
IV |
Дальнейшее увеличение полового члена, яички большие, пигментация мошонки |
Как у взрослых, но не распространяется на внутреннюю поверхность бедер, аксил-лярное оволосение в центре подмышечной впадины |
|
|
|
V |
Половые органы взрослого по размеру и форме |
Как у взрослых: в виде перевернутого треугольника, распространяется на внутреннюю поверхность бедер, но не распространяется вверх по белой линии живота. Аксиллярное оволосение по всей подмышечной впадине |
|
|
|
Нарушение дифференцировки пола
Половая дифференцировка - сложное понятие, включающее несколько категорий. Это прежде всего генетический пол, на его основе формируется гонадный пол. Под воздействием гормонов складывается фенотипический, или гражданский, пол. И наконец, социальный пол завершает процесс половой дифференцировки.
• Генетический пол детерминирован набором половых хромосом (кариотип - женский 46 XX и мужской 46 XY).
• Гены половых хромосом, обусловливающие формирование половых желёз - гонад, определяют гонадный пол.
• Гормональная активность плодных гонад способствует развитию наружных и внутренних половых органов новорождённого, формируя фенотипический пол.
• Социальный, психологический пол - половое самосознание, психосексуальная ориентация и т.д.
Нарушение половой дифференцировки (гермафродитизм, интерсексуализм, бисексуализм и т.д.) - большая группа заболеваний гетерогенной природы.
Этиология и патогенез
Патологические процессы могут затрагивать все этапы формирования пола, но основные нарушения происходят главным образом на ранних этапах: во время формирования генетического и гонадного пола. Истоки этих расстройств следует искать в раннем эмбриогенезе. Причинами нарушений дифференцировки пола могут быть генные и хромосомные аномалии, а также воздействие любых тератогенных факторов (физических, химических, инфекционных и других) во время беременности.
Наружные половые органы развиваются из общих для плодов женского и мужского пола зачатков - полового бугорка, половых складок и валиков. Под влиянием мужского полового гормона тестостерона происходят рост полового бугорка и сращение половых складок с формированием полового члена и мошонки. При отсутствии андрогенов половой бугорок образует клитор, а половые складки и валики - половые губы.
Классификация нарушений дифференцировки пола представлена на
рис. 10.18.

Рис. 10.18. Классификация нарушений половой дифференцировки
Клинические проявления
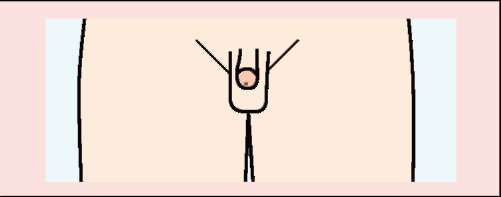
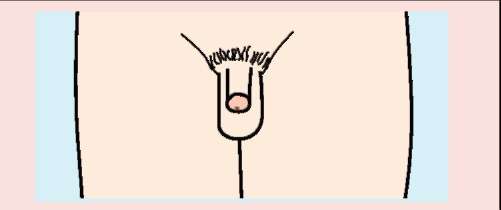
При рождении ребёнка с нарушением внутриутробного формирования пола чаще всего диагностируют неправильное или интерсексуальное строение наружных половых органов. Выраженность этих нарушений может варьировать. Согласно классификации В.А. Прадера (1954), выделяют пять степеней вирилизации (маскулинизации) наружных половых органов: от нормально сформированных женских половых органов до нормальных мужских (рис. 10.19).
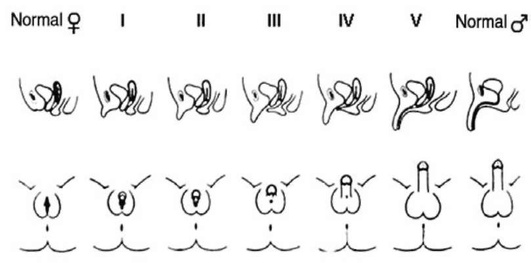
Рис. 10.19. Классификация вирилизации наружных половых органов по Прадеру
• I степень вирилизации: отмечается увеличение клитора при нормально сформированных уртере и влагалище, отверстия которых чётко отделены друг от друга.
• II степень: клитор увеличен в большей степени, отверстия уретры и влагалища расположены близко (иногда разделены только тонкой мембраной).
• III степень: характеризуется сочетанием увеличенного клитора и урогенитального синуса, объединяющего влагалище и мочеиспускательный канал.
• IV степень: отверстие урогенитального синуса расположено у основания гипертрофированного клитора, большие половые губы срастаются, и общий вид наружных половых органов имитирует гипоспадию.
• V степень представлена пенильной уретрой - отверстие урогенитального синуса открывается на головке гипертрофированного клитора, большие половые губы сращены и имеют вид мошонки, при осмотре не вызывает сомнения мужской пол новорождённого.
При сочетании хромосом 46 XX и 46 XY и наличии тканей яичка и яичника (отдельно или совместно в одной гонаде - овотестис) в одном организме имеет место истинный гермафродитизм.
Врождённая дисфункция коры надпочечников развивается вследствие генетического дефицита ферментов, участвующих в синтезе стероидных гормонов в коре надпочечников. Чаще бывает дефицит 21-гидроксилазы - фермента, участвующего в превращении прогестерона в альдостерон и 17-оксипрогесте-рона в кортизол. Снижение концентрации кортизола в сыворотке крови (по механизму отрицательной обратной связи) активирует выработку АКТГ гипофиза, что приводит к гиперстимуляции коры надпочечников. Поскольку
Наиболее распространённая причина маскулинизации наружных половых органов у девочек - врождённая дисфункция коры надпочечников.
21-гидроксилаза не участвует в синтезе андрогенов, под влиянием АКТГ усиливается выработка именно этих гормонов.
Избыток андрогенов вызывает увеличение клитора и гиперпигментацию мошонки у мальчиков, а у девочек внутриутробную вирилизацию наружных половых органов, при сохранении правильного строения внутренних. Кроме этого часто из-за дефицита минералокортикоидов выявляют синдром потери соли, который манифестирует частыми срыгиваниями, вялым сосанием, рвотой, обезвоживанием развитием артериальной гипотензии, гиперкалиемией и гипонатриемией.
У мальчиков неполная маскулинизация также проявляется неправильным строением наружных половых органов. Дисгенезия гонад у мальчиков обычно бывает проявлением генетических синдромов и связана с дефектами генов в Y-хромосоме и/или гипофункцией клеток яичка. Возможно также развитие синдрома нечувствительности периферических рецепторов к андрогенам (тестикулярной феминизации), при полной форме которой выявляют женский фенотип, а при мозаичной - интерсексуальное строение наружных половых органов при наличии нормально сформированных яичек, которые могут локализоваться в полости малого таза, паховых каналах, больших половых губах (в случае женского фенотипа).
Диагностика
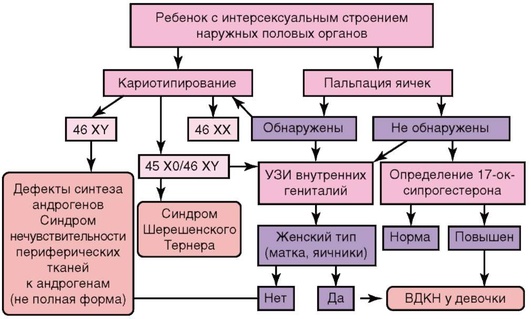
Рис. 10.20. Алгоритм диагностики при интерсексуальном строении наружных половых органов
Диагностика заболевания основана на проведении скрининга новорождённых на 5-е сутки жизни. Определяют предшественник кортизола - 17-окси-прогестерон в крови из пятки ребёнка. При уровне гормона выше 30 нмоль/л у доношенных и 60 нмоль/л у недоношенных ребёнка считают подозрительным по развитию врождённой дисфункции коры надпочечников, и он подлежит дальнейшему обследованию.
Лечение
Нарушения половой дифференцировки у девочек, вызванные материнскими андрогенами, обычно не нуждаются в лечении, в тяжёлых случаях возможна корригирующая пластика наружных половых органов. При нарушениях половой дифференцировки у мальчиков проводят коррекцию строения наружных половых органов в зависимости от выбранного родителями пола.
Лечение при врождённой дисфункции коры надпочечников - пожизненная заместительная терапия глюкокортикоидами (предпочтительнее гидрокортизон) и минералокортикоидами (флудрокортизон).
Профилактика
Тщательное наблюдение за беременной, по показаниям - медико-генетическое консультирование.
Прогноз
При своевременной диагностике, консервативном или хирургическом лечении прогноз благоприятный. В отношении фертильности для большинства больных прогноз сомнительный.
Нарушение темпов полового развития
Классификация нарушений темпов полового созревания представлена на схеме (рис. 10.21).
Появление вторичных половых признаков ранее 8 лет у девочек и ранее 9 лет у мальчиков служит критерием преждевременного полового развития.
• Раннее развитие вторичных половых признаков, характерных для данного пола, с сохранением физиологической последовательности их появления является маркёром истинного преждевременного полового созревания.
При появлении вторичных половых признаков, характерных для лиц противоположного пола, или нарушение порядка их возникновения развивается ложное преждевременное половое созревание.
Выделяют также изолированные формы: преждевременное телархе (изолированное увеличение молочных желёз) и адернархе (изолированный рост волос в лобковой и/или подмышечной областях) у девочек.
Этиология и патогенез
Этиология и патогенез преждевременного полового развития представлены в табл. 10.25. Наиболее частые причины - врождённые и наследственные аномалии, опухоли ЦНС, яичников, надпочечников, приём экзогенных эстрогенов и андрогенов, болезни печени.

Рис. 10.21. Варианты нарушений темпов полового созревания
Таблица 10.25. Причины истинного и ложного преждевременного полового развития
Форма |
Причина |
Истинное преждевременное развитие |
|
Церебральное |
Врождённая аномалия септооптической области. Опухоли головного мозга (глиомы, астроцитомы, гамартомы). Церебральные кисты. Гидроцефалия. Гиперпродукция ТТГ при первичном гипотиреозе. Последствия перенесённых нейроинфекций, травм ЦНС, лучевой терапии области головы, нейрофиброматоз |
Связанное с внеги-пофизарной продукцией гонадотропинов |
Опухоли, продуцирующие хорионический гонадотропин (хориокарцинома, гепатобластома, герминоклеточные опухоли НС и средостения) |
Ложное преждевременное развитие |
|
Ложное изосексуальное у девочек |
Эстрогенпродуцирующие кисты яичников. Дефекты рецепторов ЛГ - синдром Мак-Кьюна-Олбрайта |
Ложное изосексуальное у мальчиков |
Наследственная гиперпродукция андрогенов яичками (тестотоксикоз). Вирильная форма врождённой дисфункции коры надпочечников. Андрогенпродуцирующие опухоли надпочечников |
Ложное гетеросексуальное у девочек |
Эстрогенпродуцирующие кисты яичников Дефекты рецепторов ЛГ - синдром Мак-Кьюна-Олбрайта |
Ложное гетеросексуальное у мальчиков |
Эстрогенпродуцирующие опухоли надпочечников Заболевания печени Приём экзогенных эстрогенов |
Клинические проявления
Преждевременное половое развитие чаще бывает у девочек, что связано с более низкими дозами гонадотропина, необходимыми для запуска пубертата, и проявляется ранним и/или непоследовательным появлением вторичных половых признаков, характерных для женского (по изосексуальному типу) или мужского (по гетеросексуальному типу) пола (рис. 10.22).

Рис. 10.22. Признаки преждевременного полового развития: а - девочка 5 лет, истинное преждевременное половое развитие по изосексуальному типу; б - мальчик 3 лет, истинное преждевременное половое развитие по изосексуальному типу; в - девочка 4 лет, ложное преждевременное половое развитие по гетеросексуальному типу, вирильная форма врождённой дисфункции коры надпочечников
Диагностика
Диагностика преждевременного полового развития представлена на схеме (рис. 10.23). Она обязательно включает определение уровня гормонов и их предшественников (17-ОПГ, ТТГ, тестостерона, эстрадиола, базального и стимулированного уровней ФСГ и ЛГ), УЗИ половых органов и надпочечников, КТ, МРТ надпочечников и головного мозга для исключения опухолей.
Лечение
При выявлении объёмных образований ЦНС, надпочечников или гонад показано хирургическое лечение. При диагностике врождённой дисфункции коры надпочечников показана заместительная терапия препаратами глюкокортикоидов и минералокортикоидов, при гипотиреозе - L-тироксином♠. При обнаружении центрального преждевременного полового развития используют терапию аналогами гонадотропина. Лечение гонадотропинне-зависимого варианта заболевания заключается в назначении блокаторов стероидогенеза.
Профилактика
Профилактика включает пренатальную диагностику врождённых и наследственных нарушений, определяющих половое развитие; динамическую оценку уровня полового развития у детей в препубертатный и пубертатный период.

Рис. 10.23. Алгоритм диагностики преждевременного полового развития (ППР)
Прогноз
Прогноз зависит от причины, вызвавшей преждевременное половое развитие. Фертильный прогноз при наследственных и врождённых аномалиях с наличием грубых пороков развития других органов и систем неблагоприятный. При своевременной терапии возможно восстановление гормонального фона.