
- •Саратовский государственный технический университет
- •Введение
- •1. Тепловые эффекты химических реакций и калориметрия
- •1.1. Теоретическая часть
- •Основные понятия
- •Первый закон термодинамики
- •Второй закон термодинамики
- •Третий закон термодинамики
- •Энергетика химических реакций Тепловые эффекты химических реакций Количество теплоты. Уравнение теплового баланса
- •Термохимические законы Закон Гесса
- •Закон Кирхгофа
- •Закон Лавуазье-Ломоносова-Лапласа
- •Тепловые эффекты фазовых превращений
- •Направленность химических процессов
- •1.2. Экспериментальная часть Основы калориметрии
- •Типы калориметров
- •Работа №1. Определение содержания кислоты (концентрации) по тепловому эффекту нейтрализации
- •Работа №2. Исследование тепловых эффектов химических реакций.
- •Графическая обработка результатов эксперимента
- •1. Определение изменение температуры в ходе химической реакции.
- •2. Расчет систематической погрешности
- •3. Расчет погрешности в определении теплового эффекта реакции
- •Содержание и оформление отчета
- •Вопросы для самоконтроля
- •Задачи для самостоятельного решения
- •2. Идеальные растворы и их свойства
- •2.1. Теоретическая часть Растворы
- •Идеальные растворы
- •Свойства идеальных растворов Понижение давления насыщенного пара растворителя
- •Температура кристаллизации разбавленных растворов
- •Температура кипения разбавленных растворов
- •Изотонический коэффициент
- •Явление осмоса
- •Применение законов идеальных растворов
- •2.2. Экспериментальная часть Работа №1. Определение изотонического коэффициента и степени диссоциации электролита эбулиоскопическим методом
- •Работа №2 Определение молекулярной массы вещества криоскопическим методом
- •Обработка результатов эксперимента
- •Работа №3 Определение осмотического давления раствора неэлектролита
- •Вопросы для самоконтроля
- •Задачи для самостоятельного решения
- •3. Фазовые равновесия
- •3.1. Теоретическая часть
- •Фазовые диаграммы состояния систем
- •Однокомпонентные системы
- •Двухкомпонентные системы
- •Двухкомпонентные конденсированных системы
- •Диаграмма состояния системы с эвтектикой
- •Системы с образованием химических соединений, плавящихся конгруэнтно
- •Системы с образованием химических соединений, плавящихся инкогруэнтно
- •Системы с неограниченной растворимостью компонентов в жидком и ограниченной взаимной растворимостью в твердом состояниях
- •Системы с ограниченной взаимной растворимостью компонентов в жидком состоянии
- •Трехкомпонентные системы
- •3.2. Экспериментальная часть Работа № 1. Построение диаграммы состояния бинарной системы фенол-нафталин
- •Вопросы для самоконтроля
- •Пример решения задач
- •Задачи для самостоятельного решения
- •Литература
- •Приложение 1
- •Приложение 2
- •Оглавление
- •Лабораторный практикум по химической термодинамике
Вопросы для самоконтроля
Что такое фаза, компонент, степень свободы?
Сформулируйте правило фаз Гиббса.
В чем заключается метод термического анализа?
Что такое правило рычага?
Что называют линиями ликвидуса и солидуса, эвтектикой?
Какой вид имеют диаграммы состояния двухкомпонентных систем:
а) с простой эвтектикой;
б) с образованием устойчивого химического соединения;
в) с образованием неустойчивого химического соединения;
г) с неограниченной взаимной растворимостью компонентов в твердом состоянии;
д) с ограниченной растворимостью компонентов в твердом состоянии;
е) с ограниченной взаимной растворимостью компонентов в жидком состоянии
На каждой диаграмме покажите значение отдельных полей, линий, точек, число компонентов, степеней свободы, фаз.
Пример решения задач
На диаграмме состояния системы Pt – Sb:
Указать смысл всех полей, линий и характерных точек.
Рассчитать формулы химических соединений.
Рассмотреть процесс охлаждения расплава, заданного точками М1 и М2 (определить, что происходит в данной точке, определить число фаз и число степеней свободы в точке). Результаты представить в виде таблицы.
Построить кривые охлаждения из точек М1 и М2.
Определить соотношение фаз по правилу рычага при температуре 800ºС и 80 масс.% Sb.
При 800ºС и 80 масс.% Sb рассчитать массы равновесных фаз, полученных из 500 г первоначального состава.
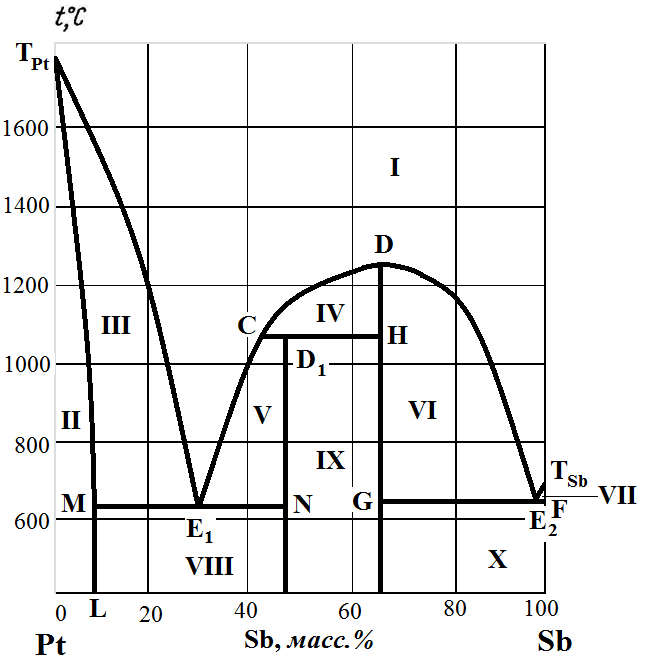
Рис. 3.16. Диаграмма состояния системы Pt – Sb.
Решение:
Компоненты диаграммы Pt – Sb образуют между собой два химических соединения: устойчивое (конгруентно плавящееся) химическое соединение D; неустойчивое (инконгруентно плавящееся) химическое соединение D1 и твердый раствор α сурьмы в платине.
|
Значение полей | |||
|
I |
расплав | ||
|
II |
кристаллы твердого раствора α | ||
|
III |
расплав и кристаллы твердого раствора α | ||
|
IV |
расплав и кристаллы устойчивого химического соединения D | ||
|
V |
расплав и кристаллы неустойчивого химического соединения D1 | ||
|
VI |
расплав и кристаллы устойчивого химического соединения D | ||
|
VII |
расплав и кристаллы сурьмы | ||
|
VIII |
механическая смесь кристаллов твердого раствора α и неустойчивого химического соединения D1 | ||
|
IX |
механическая смесь кристаллов неустойчивого химического соединения D1 и кристаллов устойчивого химического соединения D | ||
|
X |
механическая смесь кристаллов устойчивого химического соединения D и сурьмы | ||
|
Значение линий | |||
|
TPtE1CDE2TSb |
линия ликвидуса (состав расплава) | ||
|
TPtE1 |
линия ликвидуса (состав расплава, равновесного с кристаллами твердого раствора α) | ||
|
E1C |
линия ликвидуса (состав расплава, равновесного с кристаллами неустойчивого химического соединения D1) | ||
|
CD |
линия ликвидуса (состав расплава, равновесного с кристаллами устойчивого химического соединения D) | ||
|
DE2 |
линия ликвидуса (состав расплава, равновесного с кристаллами устойчивого химического соединения D) | ||
|
E2TSb |
линия ликвидуса (состав расплава, равновесного с кристаллами сурьмы) | ||
|
TPtME1ND1HGE2F |
линия солидуса (состав твердой фазы) | ||
|
TPtM |
линия солидуса (состав твердого раствора α, равновесного с расплавом) | ||
|
ME1N |
линия эвтектики (в равновесии три фазы: расплав, кристаллы твердого раствора α, кристаллы неустойчивого химического соединения D1) | ||
|
CD1H |
линия перитектики (в равновесии три фазы: расплав, кристаллы неустойчивого химического соединения D1, кристаллы устойчивого химического соединения D) | ||
|
GE2F |
линия эвтектики (в равновесии три фазы: расплав, кристаллы устойчивого химического соединения D, кристаллы сурьмы) | ||
|
ML |
линия расслоения (состав твердого раствора α, определяет предельную растворимость сурьмы в платине) | ||
|
Значение точек | |||
|
TPt |
температура плавления платины | ||
|
TSb |
температура плавления сурьмы | ||
|
E1 |
точка эвтектики (в равновесии три фазы: расплав, кристаллы твердого раствора α, кристаллы неустойчивого химического соединения D1) | ||
|
E2 |
точка эвтектики (в равновесии три фазы: расплав, кристаллы устойчивого химического соединения D, кристаллы сурьмы) | ||
|
С |
точка перитектики (в равновесии три фазы: расплав, кристаллы неустойчивого химического соединения D1, кристаллы устойчивого химического соединения D) | ||
|
D1 |
температура плавления неустойчивого химического соединения D1 | ||
|
D |
температура плавления устойчивого химического соединения D | ||
|
М |
состав твердого раствора α в точке эвтектики E1 | ||
Рассчитаем состав химических соединений.
М(Pt) = 195 г/моль;
М(Sb) = 121 г/моль.
1) Неустойчивое химическое соединение D1.
По
диаграмме
определяем
соотношение
масс
компонентов:
![]() .
.
Рассчитываем формулу химического соединения:
![]()
Следовательно, формула неустойчивого химического соединения Pt2Sb3.
2)Устойчивое химическое соединение D.
По
диаграмме
определяем
соотношение
масс
компонентов:
![]() .
.
Рассчитываем формулу химического соединения:
![]()
Следовательно, формула неустойчивого химического соединения PtSb3.
Рассмотрим процесс охлаждения расплава заданного состава.
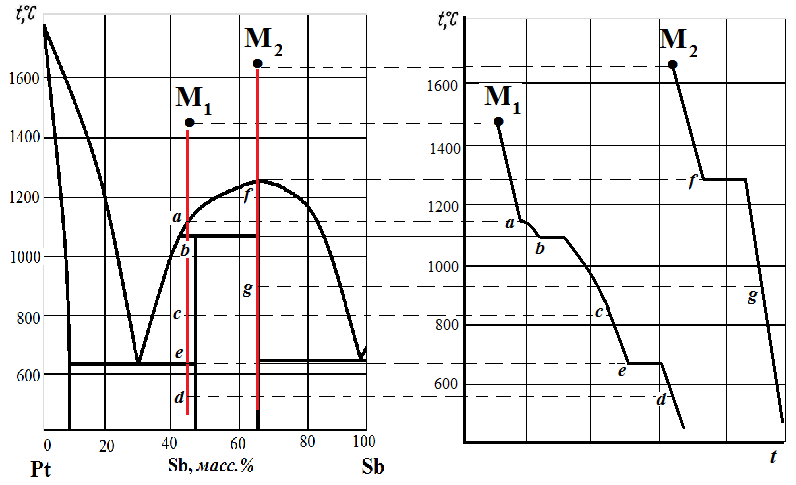
а б
Рис. 3.17. Процесс охлаждения расплава заданного состава (а) и кривые охлаждения (б)
Результат рассмотрения процесса охлаждения расплава из точки М1.
|
Точка |
Что происходит |
Ф |
С |
Что означает число степеней свободы |
|
M1 |
Охлаждение расплава |
1 |
2 |
Можно менять температуру и состав расплава |
|
а |
Появляются первые кристаллы устойчивого химического соединения D |
2 |
1 |
Каждой температуре соответствует определенный состав расплава |
|
b |
Начинается кристаллизация неустойчивого химического соединения D1, ранее выпавшие кристаллы D растворяются, на кривой охлаждения горизонтальный участок |
3 |
0 |
Система инвариантна |
|
c |
Продолжается кристаллизация неустойчивого химического соединения D1 из расплава |
2 |
1 |
Каждой температуре соответствует определенный состав расплава |
|
e |
Одновременно кристаллизуются твердый раствор α и неустойчивое химическое соединение D1, на кривой охлаждения горизонтальный участок |
3 |
0 |
Система инвариантна |
|
d |
Охлаждение механической смеси твердого раствора α и неустойчивого химического соединение D1 |
2 |
1 |
Каждой температуре соответствует определенный состав твердого раствора |
Точка M2 отвечает составу устойчивого (конгруэнтно плавящегося) химического соединения D.
Результат рассмотрения процесса охлаждения расплава из точки M2.
|
Точка |
Что происходит |
Ф |
С |
Что означает число степеней свободы |
|
M2 |
Охлаждение расплава |
1 |
2 |
Можно менять температуру и состав расплава |
|
f |
Появляются первые кристаллы устойчивого химического соединения D, на кривой охлаждения горизонтальный участок |
2 |
0 |
Система инвариантна |
|
g |
Охлаждаются кристаллы устойчивого химического соединения D |
1 |
1 |
Можно менять только температуру |
Определение соотношения масс твердой и жидкой фаз по правилу рычага.
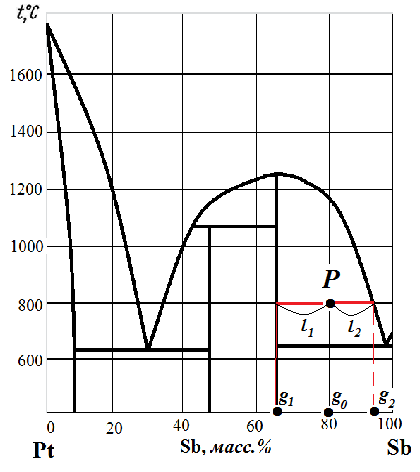
Рис. 3.18. Определение соотношения масс твердой и жидкой фаз по правилу рычага
На диаграмме состояния поставим точку P, соответствующую температуре 800ºС и 80 масс.% Sb. В точке P в равновесии находятся кристаллы устойчивого химического соединения D и расплав. Определим соотношение между фазами по правилу рычага:
![]()
Из
условия
задачи
следует,
что
![]() г.
г.
Решаем совместно систему двух уравнений:
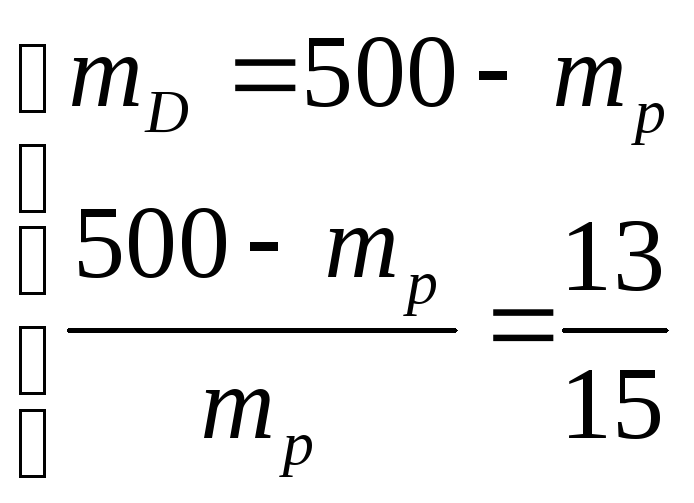
15 (500 mр ) 13 mp
6500 15 mр 13 mp
6500 28 mp
mpасплава 232 г
mD 500 232 267 г
Таким образом, из 500 г первоначального состава масса расплава составит 232 г, а масса кристаллов химического соединения D 267 г.
