
- •Саратовский государственный технический университет
- •Введение
- •1. Тепловые эффекты химических реакций и калориметрия
- •1.1. Теоретическая часть
- •Основные понятия
- •Первый закон термодинамики
- •Второй закон термодинамики
- •Третий закон термодинамики
- •Энергетика химических реакций Тепловые эффекты химических реакций Количество теплоты. Уравнение теплового баланса
- •Термохимические законы Закон Гесса
- •Закон Кирхгофа
- •Закон Лавуазье-Ломоносова-Лапласа
- •Тепловые эффекты фазовых превращений
- •Направленность химических процессов
- •1.2. Экспериментальная часть Основы калориметрии
- •Типы калориметров
- •Работа №1. Определение содержания кислоты (концентрации) по тепловому эффекту нейтрализации
- •Работа №2. Исследование тепловых эффектов химических реакций.
- •Графическая обработка результатов эксперимента
- •1. Определение изменение температуры в ходе химической реакции.
- •2. Расчет систематической погрешности
- •3. Расчет погрешности в определении теплового эффекта реакции
- •Содержание и оформление отчета
- •Вопросы для самоконтроля
- •Задачи для самостоятельного решения
- •2. Идеальные растворы и их свойства
- •2.1. Теоретическая часть Растворы
- •Идеальные растворы
- •Свойства идеальных растворов Понижение давления насыщенного пара растворителя
- •Температура кристаллизации разбавленных растворов
- •Температура кипения разбавленных растворов
- •Изотонический коэффициент
- •Явление осмоса
- •Применение законов идеальных растворов
- •2.2. Экспериментальная часть Работа №1. Определение изотонического коэффициента и степени диссоциации электролита эбулиоскопическим методом
- •Работа №2 Определение молекулярной массы вещества криоскопическим методом
- •Обработка результатов эксперимента
- •Работа №3 Определение осмотического давления раствора неэлектролита
- •Вопросы для самоконтроля
- •Задачи для самостоятельного решения
- •3. Фазовые равновесия
- •3.1. Теоретическая часть
- •Фазовые диаграммы состояния систем
- •Однокомпонентные системы
- •Двухкомпонентные системы
- •Двухкомпонентные конденсированных системы
- •Диаграмма состояния системы с эвтектикой
- •Системы с образованием химических соединений, плавящихся конгруэнтно
- •Системы с образованием химических соединений, плавящихся инкогруэнтно
- •Системы с неограниченной растворимостью компонентов в жидком и ограниченной взаимной растворимостью в твердом состояниях
- •Системы с ограниченной взаимной растворимостью компонентов в жидком состоянии
- •Трехкомпонентные системы
- •3.2. Экспериментальная часть Работа № 1. Построение диаграммы состояния бинарной системы фенол-нафталин
- •Вопросы для самоконтроля
- •Пример решения задач
- •Задачи для самостоятельного решения
- •Литература
- •Приложение 1
- •Приложение 2
- •Оглавление
- •Лабораторный практикум по химической термодинамике
Системы с образованием химических соединений, плавящихся конгруэнтно
Плавление называется конгруэнтным (от латинского слова congruentis – совпадающий), если состав жидкости совпадает с составом твердого химического соединения, из которого жидкость образовалась. Такие химические соединения являются устойчивыми и плавятся без разложения. Диаграмма плавкости двухкомпонентной системы с образованием одного химического соединения, плавящегося конгруэнтно, на которой указаны области существования и равновесные фазы, приведена на рис. 3.7.
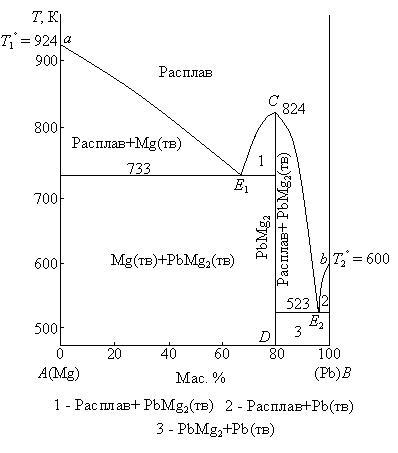
Рис. 3.7. Диаграмма плавкости системы Mg – Pb при Р = const:
1 – расплав + PbMg2(тв); 2 – расплав + Pb(тв); 3 – PbMg2(тв) + Pb(тв)
Эта диаграмма по сути является сочетанием двух диаграмм плавкости, каждая из которых имеет одну эвтектику. Так как в рассматриваемой системе Mg – Pb образуется одно химическое соединение, то из расплава могут кристаллизоваться три твердые фазы: компонент A (Mg), компонент В (Рb) и химическое соединение PbMg2. Прибавление магния или свинца к химическому соединению приводит к понижению температуры начала кристаллизации из расплава химического соединения. В связи с этим линия ликвидуса Е1СЕ2 конгруэнтно плавящегося химического соединения имеет максимум (фигуративная точка С), отвечающий температуре плавления (кристаллизации) химического соединения. Положение этого максимума строго соответствует составу образующегося химического соединения. Система, изображенная диаграмме фигуративной точкой С, условно инвариантна (Сусл = 1 – 2 + 1 = 0). Фигуративные точки, лежащие на линии CD, соответствуют твердому химическому соединению при разных температурах (Сусл = 1 – 1 + 1 = 1). В различных системах вид максимума кривой плавкости химического соединения разный и зависит от степени диссоциации соединения при температуре плавления, протекающей по схеме
|
|
(3.15) |
Чем больше степень диссоциации химического соединения, тем более пологим будет этот максимум. Чем меньше степень диссоциации химического соединения, тем острее максимум на кривой плавления. В пределе, когда степень диссоциации равна нулю, радиус кривизны линий ликвидуса Е1С и Е2С превращается в нуль, что отвечает острому максимуму. Фигуративная точка С, отвечающая недиссоциированному химическому соединению, называется сингулярной, или дальтоновской точкой. Характерной особенностью сингулярных точек является то, что при изменении условий равновесия (в частности, температуры или давления) отвечающий им состав не изменяется. Примерами систем с одним конгруэнтно плавящимся соединением являются системы Sn – Mg, Mg – Si, CaCl2 – KCl.
Если компоненты А и В образуют несколько химических соединений, плавящихся конгруэнтно, на диаграмме плавкости каждому химическому соединению отвечает свой максимум. Примерами систем с образованием нескольких химических соединений, плавящихся конгруэнтно, являются системы Ag – Ca, Ce – Sn, Cu – Mg, Al2O3 – СаО, РbО – PbCrO4, Ag2S – Sb2S3, Na2O – SiO2.
Системы с образованием химических соединений, плавящихся инкогруэнтно
Плавление называется инконгруэнтным (от латинского слова incongruentis – несовпадающий), если состав жидкости не совпадает с составом твердого химического соединения, из которого жидкость образовалась. Такие химические соединения являются неустойчивыми и разлагаются при более низких температурах, чем их температура плавления. Диаграмма плавкости двухкомпонентной системы с образованием одного химического соединения, плавящегося инконгруэнтно, на которой указаны области существования и равновесные фазы в системе, приведена на рис. 3.8.

Рис. 3.8. Диаграмма плавкости системы CuCl – KCl при Р = const:
1 – KCl(тв) + 2KCl·CuCl(тв); 2 – расплав + 2KCl·CuCl(тв).
При образовании химического соединения, плавящегося инконгруэнтно, максимум, отвечающий температуре плавления этого соединения (фигуративная точка F), не реализуется и попадает в область, находящуюся под линией ликвидуса одного из компонентов (в системе CuCl – КСl компонента В). Такой максимум называется скрытым. Это связано с тем, что химическое соединение устойчиво только до температуры, отвечающей фигуративной точке D. При этой температуре химическое соединение распадается на жидкий расплав (фигуративная точка С) и кристаллы компонента В. Точка С называется переходной, или перитектической точкой. В процессе распада химического соединения расплав находится в равновесии с двумя твердыми фазами (химическое соединение и компонент В), поэтому система условно инвариантна (Сусл = 2 – 3 + 1 = 0). При исчезновении кристаллов химического соединения система становится условно моновариантной (Cусл =2 – 2 + 1 = 1). Линия DG – линия твердого химического соединения (Сусл = 1 – 1 + 1 = 1). Примерами систем с одним инконгруэнтно плавящимся соединением являются системы К – Na, Au – Sb, C6H5I – SbCl3.
Если компоненты А и В образуют несколько химических соединений, плавящихся инконгруэнтно, на диаграмме плавкости каждому химическому соединению отвечает свой скрытый максимум. Примерами систем с образованием нескольких химических соединений, плавящихся инконгруэнтно, являются системы ZnCl2 – H2O, MgSO4 – H2O, MgCl2 – H2O.
