
- •5720100 – Лечебное дело
- •Isbn 978-9943-05-412-7
- •Предисловие
- •Глава I. Учение о растворах
- •§ 1. Роль растворов в жизнедеятельности организмов. Вода как растворитель
- •§ 2. Растворимость газов в жидкостях
- •§ 3. Кессонная болезнь
- •§ 4. Закон и.М. Сеченова
- •§ 5. Осмос и осмотическое давление
- •§ 6. Закон вант-гоффа
- •§ 7. Роль осмоса и осмотического давления в биологических системах. Плазмолиз и гемолиз
- •§ 8. Коллигативные свойства растворов
- •1. Коллигативные свойства ионных растворов
- •2. Понижение давления насыщенного пара растворителя над раствором
- •3. Понижение температуры замерзания растворов
- •4. Повышение температуры кипения растворов
- •5. Взаимосвязь между коллигативными свойствами растворов и осмотическим давлением. Определение осмотического давления криоскопическим методом
- •6. Применение криоскопии и эбуллиоскопии
- •§ 9. Экспериментальная часть
- •§ 10. Обучающе-контролирующие тесты
- •1. Укажите 4 характерных признака явления осмоса:
- •2. Укажите 3 фактора, от которых зависит величина осмотического давления:
- •3. Укажите 3 зависимости, выражающие закон Вант-Гоффа:
- •4. Выберите 3 ответа, формулирующие закон Вант-Гоффа:
- •5. Укажите 4 характеристики явления гемолиза в организме:
- •6. Укажите 4 характеристики явления плазмолиза в организме:
- •7. Выберите 3 формулировки изотонического, гипотонического и гипертонического растворов:
- •8. Укажите 4 фактора, объясняющие суть закона Рауля:
- •9. Выберите 5 правильных ответов, характеризующих законы криоскопии и эбуллиоскопии:
- •10. Выберите 3 ответа, характеризующие изотонический коэффициент:
- •11. Выберите 3 физических свойства разбавленных растворов, зависящие от концентрации растворенных веществ в растворе:
- •12. Назовите 3 условия, при которых происходит явление осмоса:
- •Глава II. Электрохимия
- •§ 1. Электропроводимость растворов электролитов. Кондуктометрическое титрование
- •Удельное сопротивление ряда биологических Жидкостей
- •Предельная молярная электропроводимость ионов в воде (18 °c)
- •§ 2. Потенциалы и электродвижущие силы
- •Некоторые стандартные потенциалы восстановления
- •Стандартные окислительно-восстановительные потенциалы
- •§ 3. Гальванические элементы
- •§ 4. Типы электродов
- •§ 5. Электрохимия в медицине
- •§ 6. Экспериментальная часть
- •Вопрос 1. Почему при бесконечном разведении раствора скорости движения различных ионов не будут зависеть друг от друга?
- •§ 7. Потенциометрия. Потенциометрическое титрование
- •Потенциалы электродов сравнения при различных температурах
- •§ 8. Экспериментальная часть
- •Метод «круглого стола»
- •§ 8. Обучающе-контролирующие тесты
- •1. Укажите 5 ответов, дающих характеристику электропроводимости:
- •16. Выберите 4 ответа, отражающие изменения кривой кондуктометрического титрования сильной кислоты сильным основанием:
- •17. Выберите 4 ответа, отражающие изменения кривой кондуктометрического титрования слабой кислоты сильным основанием:
- •18. Выберите 4 ответа, отражающие изменения кривой при титровании смеси сильной и слабой кислот:
- •19. Укажите 4 ответа с данными об электропроводимости биологических жидкостей при различных заболеваниях:
- •20. Укажите 3 ответа со значениями электропроводности при различном состоянии кислотности в желудке:
- •21. Укажите 5 видов и характеристику потенциалов, возникающих на границах раздела фаз:
- •36. Укажите 4 типа электродов и их правильные характеристики:
- •Коллоидная химия
- •Глава III. Физико-химия поверхностных явлений
- •§ I. Поверхностные явления и их значение в биологии и медицине
- •§ 2. Поверхностная энергия и поверхностное натяжение
- •Поверхностное натяжение некоторых веществ в жидком состоянии на границе с воздухом или паром
- •§ 3. Адсорбция и поверхностное натяжение
- •§ 4. Поверхностно-активные и поверхностно- инактивные вещества
- •§ 5. Изотермы поверхностного натяжения
- •§ 6. Адсорбция на границе раздела жидкость – газ и жидкость – жидкость
- •§ 7. Адсорбция на границе раздела твердое тело – газ и твердое тело – жидкость (раствор)
- •§ 8. Ориентация молекул в поверхностном слое и структура биологических мембран
- •§ 9. Адсорбция из растворов электролитов
- •§ 10. Хроматография, ее сущность и применение в биологии и медицине
- •§ 11. Экспериментальная часть
- •Задания для самостоятельной работы
- •Конкурс «кот в мешке»
- •§ 12. Обучающе-контролирующие тесты
- •7. Укажите 3 ответа, поясняющие уравнение Фрейндлиха:
- •8. Укажите 4 ответа, поясняющие уравнение Ленгмюра:
- •9. Укажите 3 ответа с правильной характеристикой трех частей изотермы адсорбции Ленгмюра:
- •10. Укажите 3 операции, проводимые при определении величины адсорбции на твердой поверхности:
- •11. Выберите 5 характеристик гидрофильности или гидрофобности некоторых видов поверхности:
- •12. Выберите 3 правила, которым подчиняется адсорбция растворенного вещества на твердой поверхности:
- •13. Укажите 5 примеров молекулярной и ионной адсорбции на угле:
- •24. Укажите 3 фактора, от которых зависит адсорбция газов твердым адсорбентом:
- •25. Укажите 3 фактора, от которых зависит адсорбция на границе твердое тело – раствор.
- •Глава IV. Физико-химия дисперсных систем
- •§ 1. Дисперсные системы и их классификация
- •Изменение удельной поверхности при дроблении
- •1 См3 вещества
- •Классификация систем по степени дисперсности
- •Классификация дисперсных систем по агрегатном состоянию дисперсной фазы и дисперсионной среды
- •§ 2. Коллоидное состояние. Методы получения и очистки коллоидных растворов
- •Диспергирование Конденсация
- •§ 3. Молекулярно-кинетические свойства коллоидных систем
- •§ 4. Оптические свойства коллоидных систем
- •§ 5. Классификация коллоидных систем
- •§ 6. Возникновение двойного электрического слоя и его строение
- •§ 7. Строение коллоидных частиц
- •§ 8. Электрокинетическне явления. Электрофорез и использование его в медицине
- •§ 9. Устойчивость коллоидных систем
- •Коагуляция золей As2s3 и Fe(oh)3 электролитами
- •§ 10. Пептизация. Коллоидная защита
- •§ 11. Аэрозоли и их Практическое Значение
- •§ 12. Суспензии, методы их получения и свойства
- •§ 13. Эмульсии, методы их получения и свойства
- •§ 14. Коллоидные поверхностно-активные вещества (пав)
- •§ 15. Экспериментальная часть
- •§ 16. Обучающе-контролирующие тесты
- •1. Укажите 4 характеристики состава и свойств дисперсных систем:
- •2. Укажите 3 типа дисперсных систем согласно классификации по размеру частиц:
- •19. Укажите 4 характеристики поверхностно-активных и поверхностно-инактивных веществ.
- •20. Физическая и коллоидная химия. Под ред. А.П. Беляева. Изд. Группа «гэотар-Медиа», – м.:, 2010. Оглавление
- •Коллоидная химия
- •Сталина Салиховна касымова физическая и коллоидная химия
§ 4. Оптические свойства коллоидных систем
При прохождении через дисперсную систему свет отражается, поглощается или рассеивается частицами. Рассеяние света наблюдается в том случае, когда длина волны видимого света больше диаметра частицы дисперсной фазы. Отражение света частицами наблюдается, если размеры частиц превышают длину волны, т.е. в грубодисперсных системах. Коллоидные частицы по размеру меньше или соизмеримы с длинами волн видимого света, поэтому световые лучи от них не отражаются и они не видны в оптическом микроскопе. Для коллоидных частиц наблюдается только светорассеяние. Это можно проследить на следующем опыте. Если на прозрачный коллоидный раствор в сосуде (рис. 7) направить пучок световых лучей и наблюдать его сбоку на темном фоне, то можно увидеть в жидкости светлый конус. Это так называемый эффект или конус Тиндаля.
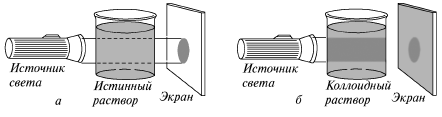
Рис. 9. Прохождение света через истинный раствор и коллоид.
Пучок света проходит через раствор, не рассеиваясь (а); коллоидные частицы рассеивают проходящий через раствор пучок света, в результате он становится видимым (б); диффузный пучок света не дает на экране четкого изображения
Рассеяние света мелкими частицами впервые описал М.В. Ломоносов, затем в 1857 г. исследовал М. Фарадей. Д. Тиндаль в 1869 г., изучая природу туманов, обнаружил светящийся в жидкости конус, названный его именем. Эффект Тиндаля теоретически был описан английским физиком Д. Рэлеем. Он установил, что интенсивность светорассеяния зависит не только от размеров коллоидных частиц и длины световой волны, но и от объема частиц растворенного вещества. Если допустить, что раствор достаточно разбавлен, что коллоидные частицы шарообразны, не поглощают свет, не электропроводны, то интенсивность светорассеяния по Рэлею будет иметь следующий вид:
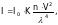
где I – интенсивность света, рассеянного единицей объема золя;
Io – интенсивность падающего света;
К – константа для данного золя, зависящая от разности показателей преломления дисперсной фазы и дисперсионной среды;
n – число частиц в единице объема;
V – объем одной частицы дисперсной фазы;
– длина волны падающего света.
Уравнение Рэлея справедливо для непроводящих частиц. Так как интенсивность светорассеяния пропорциональна квадрату объема частиц, то для растворов с частицами очень незначительного объема или равного объему частиц растворителя, светорассеяние практически не наблюдается. Обратная пропорциональность рэлеевского рассеяния четвертой степени длины волны падающего света показывает, что рассеяние коротких волн (УФ часть спектра) происходит более интенсивно. Отсюда следует, что при освещении золей белым проходящим светом, они приобретают красноватый, а при боковом освещении -голубоватый оттенок. С этим связан красноватый цвет при восходе и заходе Солнца за счет прошедшего через атмосферу света. Красный цвет выбран в качестве сигнала опасности именно потому, что он виден в туманную погоду на большие расстояния, чем любой другой вследствие малого рассеяния. Голубой цвет неба и синий цвет морской воды также объясняется светорассеянием коллоидных аэро- и гидрозолей.
На явлении рассеяния света коллоидными частицами были основаны важные методы изучения коллоидных систем: ультрамикроскопия и нефелометрия.
Ультрамикроскопия. Отражение света поверхностью частиц возможно при условии, если их размеры превышают длину волны, т.е. в грубодисперсных системах. Коллоидные же частицы, имеющие размеры 10-7–10-5 см, соизмеримы с длинами волн видимого света (3,9·10-5 – 7,6·10-5 см). В связи с этим свет не отражается от них, и они не видны в обычные оптические микроскопы, так как световые волны огибают коллоидные частицы и не дают тени, а рассеянная часть света очень незначительна и в условиях проходящего света не заметна. Если же использовать сильное боковое освещение, то каждая коллоидная частица становится источником рассеянного света и на темном фоне наблюдается в виде светящейся точки. Прибор, при помощи которого можно увидеть эффект рассеяния света отдельными коллоидными частицами, называется ультрамикроскопом. Ультрамикроскоп сконструирован в 1903 г. Г. Зидентопфом и Р. Зигмонди. Принцип работы ультрамикроскопа сводится к наблюдению в нем конуса Тиндаля. Свет от осветителя не попадает в объектив микроскопа, а также в глаз наблюдателя, поэтому фон поля зрения ультрамикроскопа темный и в нем заметен слабый свет, рассеиваемый коллоидными частицами. Видны светящиеся точки, яркость которых зависит от интенсивности падающего света, поэтому применяются более яркие источники света.
Ультрамикроскопия позволяет изучать кинетические свойства коллоидных растворов (например, броуновское движение), определять число частиц в единице объема. Зная общую массу диспергированного вещества и, определив число частиц в единице объема, можно вычислить массу одной частицы, а затем определить ее размер и объем. Найденное значение размера частиц отвечает среднему размеру.
