
- •5720100 – Лечебное дело
- •Isbn 978-9943-05-412-7
- •Предисловие
- •Глава I. Учение о растворах
- •§ 1. Роль растворов в жизнедеятельности организмов. Вода как растворитель
- •§ 2. Растворимость газов в жидкостях
- •§ 3. Кессонная болезнь
- •§ 4. Закон и.М. Сеченова
- •§ 5. Осмос и осмотическое давление
- •§ 6. Закон вант-гоффа
- •§ 7. Роль осмоса и осмотического давления в биологических системах. Плазмолиз и гемолиз
- •§ 8. Коллигативные свойства растворов
- •1. Коллигативные свойства ионных растворов
- •2. Понижение давления насыщенного пара растворителя над раствором
- •3. Понижение температуры замерзания растворов
- •4. Повышение температуры кипения растворов
- •5. Взаимосвязь между коллигативными свойствами растворов и осмотическим давлением. Определение осмотического давления криоскопическим методом
- •6. Применение криоскопии и эбуллиоскопии
- •§ 9. Экспериментальная часть
- •§ 10. Обучающе-контролирующие тесты
- •1. Укажите 4 характерных признака явления осмоса:
- •2. Укажите 3 фактора, от которых зависит величина осмотического давления:
- •3. Укажите 3 зависимости, выражающие закон Вант-Гоффа:
- •4. Выберите 3 ответа, формулирующие закон Вант-Гоффа:
- •5. Укажите 4 характеристики явления гемолиза в организме:
- •6. Укажите 4 характеристики явления плазмолиза в организме:
- •7. Выберите 3 формулировки изотонического, гипотонического и гипертонического растворов:
- •8. Укажите 4 фактора, объясняющие суть закона Рауля:
- •9. Выберите 5 правильных ответов, характеризующих законы криоскопии и эбуллиоскопии:
- •10. Выберите 3 ответа, характеризующие изотонический коэффициент:
- •11. Выберите 3 физических свойства разбавленных растворов, зависящие от концентрации растворенных веществ в растворе:
- •12. Назовите 3 условия, при которых происходит явление осмоса:
- •Глава II. Электрохимия
- •§ 1. Электропроводимость растворов электролитов. Кондуктометрическое титрование
- •Удельное сопротивление ряда биологических Жидкостей
- •Предельная молярная электропроводимость ионов в воде (18 °c)
- •§ 2. Потенциалы и электродвижущие силы
- •Некоторые стандартные потенциалы восстановления
- •Стандартные окислительно-восстановительные потенциалы
- •§ 3. Гальванические элементы
- •§ 4. Типы электродов
- •§ 5. Электрохимия в медицине
- •§ 6. Экспериментальная часть
- •Вопрос 1. Почему при бесконечном разведении раствора скорости движения различных ионов не будут зависеть друг от друга?
- •§ 7. Потенциометрия. Потенциометрическое титрование
- •Потенциалы электродов сравнения при различных температурах
- •§ 8. Экспериментальная часть
- •Метод «круглого стола»
- •§ 8. Обучающе-контролирующие тесты
- •1. Укажите 5 ответов, дающих характеристику электропроводимости:
- •16. Выберите 4 ответа, отражающие изменения кривой кондуктометрического титрования сильной кислоты сильным основанием:
- •17. Выберите 4 ответа, отражающие изменения кривой кондуктометрического титрования слабой кислоты сильным основанием:
- •18. Выберите 4 ответа, отражающие изменения кривой при титровании смеси сильной и слабой кислот:
- •19. Укажите 4 ответа с данными об электропроводимости биологических жидкостей при различных заболеваниях:
- •20. Укажите 3 ответа со значениями электропроводности при различном состоянии кислотности в желудке:
- •21. Укажите 5 видов и характеристику потенциалов, возникающих на границах раздела фаз:
- •36. Укажите 4 типа электродов и их правильные характеристики:
- •Коллоидная химия
- •Глава III. Физико-химия поверхностных явлений
- •§ I. Поверхностные явления и их значение в биологии и медицине
- •§ 2. Поверхностная энергия и поверхностное натяжение
- •Поверхностное натяжение некоторых веществ в жидком состоянии на границе с воздухом или паром
- •§ 3. Адсорбция и поверхностное натяжение
- •§ 4. Поверхностно-активные и поверхностно- инактивные вещества
- •§ 5. Изотермы поверхностного натяжения
- •§ 6. Адсорбция на границе раздела жидкость – газ и жидкость – жидкость
- •§ 7. Адсорбция на границе раздела твердое тело – газ и твердое тело – жидкость (раствор)
- •§ 8. Ориентация молекул в поверхностном слое и структура биологических мембран
- •§ 9. Адсорбция из растворов электролитов
- •§ 10. Хроматография, ее сущность и применение в биологии и медицине
- •§ 11. Экспериментальная часть
- •Задания для самостоятельной работы
- •Конкурс «кот в мешке»
- •§ 12. Обучающе-контролирующие тесты
- •7. Укажите 3 ответа, поясняющие уравнение Фрейндлиха:
- •8. Укажите 4 ответа, поясняющие уравнение Ленгмюра:
- •9. Укажите 3 ответа с правильной характеристикой трех частей изотермы адсорбции Ленгмюра:
- •10. Укажите 3 операции, проводимые при определении величины адсорбции на твердой поверхности:
- •11. Выберите 5 характеристик гидрофильности или гидрофобности некоторых видов поверхности:
- •12. Выберите 3 правила, которым подчиняется адсорбция растворенного вещества на твердой поверхности:
- •13. Укажите 5 примеров молекулярной и ионной адсорбции на угле:
- •24. Укажите 3 фактора, от которых зависит адсорбция газов твердым адсорбентом:
- •25. Укажите 3 фактора, от которых зависит адсорбция на границе твердое тело – раствор.
- •Глава IV. Физико-химия дисперсных систем
- •§ 1. Дисперсные системы и их классификация
- •Изменение удельной поверхности при дроблении
- •1 См3 вещества
- •Классификация систем по степени дисперсности
- •Классификация дисперсных систем по агрегатном состоянию дисперсной фазы и дисперсионной среды
- •§ 2. Коллоидное состояние. Методы получения и очистки коллоидных растворов
- •Диспергирование Конденсация
- •§ 3. Молекулярно-кинетические свойства коллоидных систем
- •§ 4. Оптические свойства коллоидных систем
- •§ 5. Классификация коллоидных систем
- •§ 6. Возникновение двойного электрического слоя и его строение
- •§ 7. Строение коллоидных частиц
- •§ 8. Электрокинетическне явления. Электрофорез и использование его в медицине
- •§ 9. Устойчивость коллоидных систем
- •Коагуляция золей As2s3 и Fe(oh)3 электролитами
- •§ 10. Пептизация. Коллоидная защита
- •§ 11. Аэрозоли и их Практическое Значение
- •§ 12. Суспензии, методы их получения и свойства
- •§ 13. Эмульсии, методы их получения и свойства
- •§ 14. Коллоидные поверхностно-активные вещества (пав)
- •§ 15. Экспериментальная часть
- •§ 16. Обучающе-контролирующие тесты
- •1. Укажите 4 характеристики состава и свойств дисперсных систем:
- •2. Укажите 3 типа дисперсных систем согласно классификации по размеру частиц:
- •19. Укажите 4 характеристики поверхностно-активных и поверхностно-инактивных веществ.
- •20. Физическая и коллоидная химия. Под ред. А.П. Беляева. Изд. Группа «гэотар-Медиа», – м.:, 2010. Оглавление
- •Коллоидная химия
- •Сталина Салиховна касымова физическая и коллоидная химия
§ 8. Обучающе-контролирующие тесты
1. Укажите 5 ответов, дающих характеристику электропроводимости:
1) способность раствора электролита проводить электрический ток;
2) обратна электрическому сопротивлению;
3) зависит от длины проводника;
4) зависит от площади поперечного сечения проводника;
5) зависит от удельного сопротивления;
6) способность растворов электролитов к диссоциации;
7) обратна напряжению проводника;
8) обратна силе тока;
9) зависит от напряжения проводника;
10) зависит от потенциала.
2. Укажите 3 ответа, характеризующих удельную электропроводимость:
1) обратна удельному сопротивлению;
2) это электропроводимость 1 см3 раствора при l = 1 см и S = 1 см2;
3) единица измерения – См/см или Ом-1 см-1;
4) равно половине удельного сопротивления;
5) это электропроводимость 1 мл раствора при l = 10 см и S = 10 см2;
6) единица измерения Ом/см.
3. Укажите 3 ответа, характеризующих молярную электропроводимость:
1) это электропроводимость одного моля вещества между электродами с l = 1 см;
2) прямо пропорциональна удельной электропроводимости;
3) единицей измерения является См. см2/моль или Ом-1 см2 моль-1;
4) это величина электропроводимости 1 см3 раствора с l =1 см и S = 1 см2;
5) это электропроводимость 1 см2 поверхности раствора;
6) прямо пропорциональна сопротивлению.
4. Выберите 4 проводника первого рода:
1) металлы; 2) металлические сплавы;
3) уголь; 4) графит;
5) соли; 6) кислоты;
7) основания; 8) оксиды.
5. Выберите 5 проводников второго рода:
1) раствор соляной кислоты; 6) кусок железа;
2) раствор гидроксида натрия; 7) проволока из меди;
3) раствор хлорида натрия; 8) уголь;
4) расплав оксида кальция; 9) графит;
5) расплав сульфата меди; 10) сплав золота и серебра.
6. Укажите 3 случая использования значений молярной электропроводимости:
1) для расчета степени диссоциации электролита;
2) для расчета константы диссоциации электролита;
3) для экспрессной электродиагностики;
4) для расчета потенциала;
5) для расчета электродвижущей силы;
6) в медстатистике.
7. Какие 5 величин дают возможность рассчитывать степень диссоциации в электрохимии:
1) сопротивление; 2) удельная электропроводимость; 3)молярная электропроводимость; 4) подвижность ионов;
5) постоянная сосуда К; 6) напряжение;
7) сила тока; 8) частота света;
9) заряд ионов;
10) величина электроотрица тельности ионов.
8. Укажите 4 фактора, от которых зависит степень диссоциации электролита:
1) природа электролита; 2) природа растворителя;
3) температура; 4) концентрация раствора;
5) природа металла; 6) природа неметалла;
7) давление; 8) объем раствора.
9. Укажите 3 ответа с указанием степени диссоциации и силы электролита:
1) у слабых электролитов степень диссоциации меньше 3%;
2) у средних электролитов степень диссоциации от 3 до 30%;
3) у сильных электролитов степень диссоциации больше 30%;
4) у слабых электролитов степень диссоциации меньше единицы;
5) у средних электролитов степень диссоциации равна единице;
6) у сильных электролитов степень диссоциации больше единицы.
10. Укажите какие 4 величины необходимы для расчета константы диссоциации в электрохимии:
1) концентрация электролита;
2) молярная электропроводимость при данной концентрации раствора;
3) подвижность катионов;
4) подвижность анионов;
5) объем электролита; 6) температура;
7) заряд катиона; 8) заряд аниона.
11. Укажите 4 фактора, от которых зависит скорость движения ионов в растворах электролитов:
1) природа ионов; 5) давление;
2) природа растворителя; 6) объем раствора;
3) температура; 7) заряд иона;
4) концентрация растворенного вещества;
8) объем растворителя.
12. Назовите 3 условия скорости движения ионов, т.е. абсолютной скорости ионов:
1) при разности потенциалов 1 В;
2) при длине 1 м;
3) выраженная в метрах в секунду;
4) при разности потенциалов 10 В;
5) при длине 1 м; 6) выраженная в метрах на единицу длины.
13. Укажите 3 ответа с правильным отражением закона Кольрауша:
1)
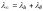 ;
;
2) молярная электропроводимость при бесконечном разведении равна сумме подвижностей катионов и анионов;
3) закон справедлив для слабых электролитов;
4)
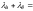 æ;
æ;
5) удельная электропроводимость равна сумме подвижностей катионов и анионов;
6) закон справедлив для растворов сильных электролитов.
14. Укажите 3 преимущества кондуктометрического титрования:
1) позволяет проводить определения в окрашенных и мутных растворах;
2) позволяет вести определения в биологических жидкостях;
3) позволяет вести определения в присутствии окислителей и восстановителей;
4) позволяет точно определять концентрацию вещества;
5) простота; 6) дешевизна.
15. Укажите 5 правильных пунктов, отражающих этапы процесса кондуктометрического титрования:
1) измеряется сопротивление проводника после каждой порции рабочего раствора;
2) рассчитывается удельная электропроводность;
3) строится зависимость удельного сопротивления от объема прилитого рабочего раствора;
4) определяется точка эквивалентности по месту изгиба кривой;
5) производится расчет нормальности раствора;
6) измеряется разность потенциалов в растворе;
7) определяется ЭДС;
8) рассчитывается объем рабочего раствора;
9) фиксируется точка эквивалентности по изменению цвета индикатора;
10) рассчитывается молярная доля раствора.
