- •Предмет и задачи органической химиии, ее место в системе медицинского образования.
- •Концепция гибридизации атомных орбиталей: три валентных состояния атома угерода; строгая и нестрогая гибридизация. Концепция электронных смещений: индуктивный эффект.
- •Концепция электронных смещений: мезомерный эффект.
- •4. Оптическая изомерия. Хиральность. Абсолютная (r/s) и относительная (d/l) конфигурация. Способы разделения рацематов. Стереохимия реакций нуклеофильного замещения и нуклеофильного присоединения.
- •I. Алканы (предельные углеводороды, парафины)
- •Реакции синтеза алканов.
- •2.4.3. Реакции изомеризации
- •Способы получения и природные источники
- •3) Аммонолиз галогеналканов — это взаимодействие галогеналканов с аммиаком, приводящее к получению аминов (или их солей):
- •2. Галогеналканы могут быть получены из спиртов и других галогеналканов с помощью реакции замещения, например:
- •4. Галогеналканы могут быть получены из альдегидов, кетонов и карбоновых кислот действием pCl5, pBr3 или sf4 при нагревании.
- •1) Образование металлоорганического производного (если использется металл, а не заранее приготовленное металлоорганическое соединение):
- •2) Взаимодействие образовавшегося, в данном случае, натрийорганического соединения с другой молекулой алкилгалогенида:
- •Особенности строения, изомерия, физических свойств, химического поведения многоатомных спиртов. Механизмы реакций.
- •2.Получение простых эфиров
- •III. Свойства простых эфиров
- •1. Кислотное расщепление простых эфиров
- •2. Радикальные реакции простых эфиров
- •12. Нитро- и нитрозосоединения: строение, получения, кислотно-основные свойства. Свойства соединений, имеющих α-водородные атомы. Нитроловые кислоты и псевдонитролы.
- •Получение нитросоединений
- •Псевдонитролы
- •13. Тиоспирты и тоиэфиры. Особенности строения, химических свойств. Реакции окисления. Способы получения.
- •2 . Эффект сопряжения
- •4.3.3. Строение и свойства сопряжённых диенов
- •Строение тройной связи
- •Номенклатура алкинов
- •2 Атома с → этан → этин;
- •3 Атома с →пропан → пропин и т.Д.
- •Присоединение галогенов (Cl2 и Br2)
- •2. Присоединение галогеноводородов к алкинам.
- •3. Реакция гидратации (Реакция Кучерова)
- •4. Присоединение hcn.
- •5. Присоединение спиртов.
- •Галогеналканы
- •. Классификация, номенклатура, изомерия
- •3.2.2. Строение и свойства
- •18. Особенности химического поведения непредельных спиртов
- •20.Непредельные альдегиды и кетоны: кетен, акролеин, кротоновый альдегид - особенности их свойств и способов получения
- •23. Производные карбоновых кислот.
- •6.5.2. Строение
- •6.5.3. Химические свойства
- •25.Дикарбоновые кислоты
- •27. Гидроксикислоты: классификация, номенклатура, оптическая изомерия. Химические свойства. Отношение к нагреванию. Способы получения. Способы разделения рацематов. Нахождение в природе.
- •2.1. Получение α-гидроксикислот
- •2.2. Получение β-гидроксикислот
- •2.3. Получение γ-гидроксикислот
- •28. Оксокислоты: номенклатура, изомерия, способы получения и химические свойства.
- •29. Ацетоуксусная кислота и ацетоуксусный эфир: строение, свойства, получение и использование для синтезов.
- •Присоединение этилового спирта к дикетену
- •Сложноэфирная конденсация Кляйзена
- •30. Аминокислоты: номенклатура, изомерия. Способы получения. Химические свойства. Отношение к нагреванию. Лактим-лактамная таутомерия.
- •1. Из карбоновых кислот через их галогенопроизводные в радикале
- •2. Гидролиз пептидов и белков
- •4. Микробиологический синтез
- •Отношение к нагреванию.
- •Лактим-лактамная таутомерия.
- •34. Алициклические углеводороды: номенклатура, строение, свойства. Особенности поведения малых циклов. Терпены, терпеноиды, каротиноиды.
- •34. Алициклические углеводороды: номенклатура, строение, свойства. Особенности поведения малых циклов. Терпены, терпеноиды, каротиноиды.
- •35. Бензол, его строение и свойства. Ароматичность. Реакции присоединения, окисления, замещения в сравнении с предельными и непредельными углеводородами. Методы синтеза бензольного кольца.
- •37.Монозамещенные бензола
- •38. Ароматические углеводы.
- •41.Реакции нуклеофильного замещения в ароматическом кольце.
- •42. Ароматические сульфокислоты.
- •Применение
- •43. Ароматические нитросоединения
- •Свойства: Химические свойства
- •Реакции нуклеофильного замещения
- •44.Фенолы и спирты.
- •Классификация
- •Электронное строение[
- •Физические свойства
- •В живых организмах
- •Химические свойства[
- •1. Реакции с участием гидроксильной группы
- •2. Реакции с участием бензольного кольца]
- •Способы получения[
- •Применение фенолов[
- •Классификация спиртов[
- •Номенклатура спиртов[ Систематическая номенклатура[
- •Другие номенклатуры[
- •10.5.1. Классификация, номенклатура, изомерия фенолов и ароматических спиртов
- •10.5.1. Классификация, номенклатура, изомерия фенолов и ароматических спиртов
- •Строение и физические свойства[
- •Методы синтеза[
- •Химические свойства[
- •Применение[
- •45. Ароматические амины
- •Номенклатура ароматических аминов
- •Изомерия ароматических аминов
- •Способы получения ароматических аминов Способы получения первичных аминов
- •4. Реакция Гофмана
- •Способы получения вторичных аминов
- •Способы получения третичных аминов
- •Физические свойства ароматических аминов
- •Химические свойства ароматических аминов
- •1. Кислотно-основные свойства аминов
- •1) Основные свойства аминов
- •2. Реакции аминов как нуклеофильных реагентов
- •1. Алкилирование ароматических аминов
- •2. Ацилирование ароматических аминов
- •3. Реакции с альдегидами и кетонами
- •Окисление ароматических аминов
- •3. Реакции электрофильного замещения в бензольном кольце
- •1. Реакция галогенирования
- •2. Реакция сульфирования
- •Реакционная способность[
- •Номенклатура
- •Свойства[
- •Реакционная способность
- •Синтез[
- •Азокрасители[
- •Получение солей диазония
- •Химические свойства
- •1. Замещение на гидроксигруппу
- •2. Замещение на галоген
- •3. Замещение на cn
- •Понятие об азокрасителях
Реакционная способность
Алифатические азосоединения при нагревании или при облучении ультрафиолетом разлагаются с выделением азота и образованием свободных радикалов, поэтому некоторые из них, в частности, 2,2'-азо-бис-изобутиронитрил, разлагающийся при 60—100 °C, используются в качестве инициаторов радикальной полимеризации:
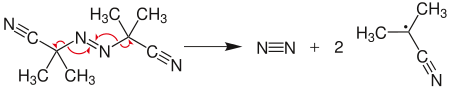
Термическое разложение симметричных алифатических азосоединений также используется в синтетической практике для получения алифатических соединений путём рекомбинации образующихся при их разложении радикалов[2]:
{\displaystyle {\mathsf {R{\text{-}}N{\text{=}}N{\text{-}}R\rightarrow R{\text{-}}R+N_{2}}}}
Ароматические азосоединения более стабильны за счет сопряжения — так, бензолазоэтан C6H5—N=N—C2H5 кипит при 180 °C почти без разложения.
Алифатические азосоединения с атомами водорода в α-положении под действием кислот претерпевают перегруппировку в гидразоны:
{\displaystyle {\mathsf {R{\text{-}}CH_{2}{\text{-}}N{\text{=}}N{\text{-}}R'\rightarrow R{\text{-}}CH{\text{=}}N{\text{-}}NH{\text{-}}R'}}}Под действием восстановителей (NaBH4, цинк в щелочной среде и т. п.) азосоединения превращаются в гидразосоединения (1,2-замещённые гидразины):
{\displaystyle {\mathsf {R^{1}{\text{-}}N{\text{=}}N{\text{-}}R^{2}+[H]\rightarrow R^{1}{\text{-}}NH{\text{-}}NH{\text{-}}R^{2}}}}В случае использования сильных восстановитей возможно восстановление in situ промежуточно образующихся гидразинов с образованием первичных аминов:
{\displaystyle {\mathsf {R^{1}{\text{-}}N{\text{=}}N{\text{-}}R^{2}+[H]\rightarrow R^{1}{\text{-}}NH_{2}+R^{2}NH_{2}}}}Мягкие окислители (например, пероксид водорода в уксусной кислоте, надкислоты) превращают азосоединения в азоксисоединения:
{\displaystyle {\mathsf {C_{6}H_{5}{\text{-}}N{\text{=}}N{\text{-}}C_{6}H_{5}+H_{2}O_{2}\rightarrow C_{6}H_{5}{\text{-}}N(O){\text{=}}NC_{6}H_{5}+H_{2}O}}}а сильные (дымящая азотная кислота на холоду) — в нитросоединения, разрушая азогруппу:
{\displaystyle {\mathsf {C_{6}H_{5}{\text{-}}N{\text{=}}N{\text{-}}C_{6}H_{5}+4Cl_{2}+4H_{2}O\rightarrow 2C_{6}H_{5}NO_{2}+8HCl}}}Электрондефицитные азосоединения — азокарбонильные соединения и, особенно, азодикарбоксилаты — выступают в качестве диенофилов в реакции Дильса — Альдера[3].
Синтез[
Стандартным методом синтеза алифатических и алкиларилазосоединений является дегидрирование N,N'-дизамещенных гидразинов действием различных окислителей (дихромат калия, оксид ртути[какой?], бром, азотная кислота и др.):
{\displaystyle {\mathsf {R^{1}{\text{-}}NH{\text{-}}NH{\text{-}}R^{2}+[O]\rightarrow R^{1}{\text{-}}N{\text{=}}{\text{-}}N{\text{-}}R^{2}}}}
Функционализированные алифатические азосоединения могут быть получены хлорированием кетазинов с дальнейшим замещением хлора в образующихся при хлорировании α,α′-дихлоразосоединениях различными нуклеофилами:
{\displaystyle {\mathsf {R^{1}R^{2}C{\text{=}}N{\text{-}}N{\text{=}}CR^{3}R^{4}+Cl_{2}\rightarrow R^{1}R^{2}CCl{\text{-}}N{\text{=}}N{\text{-}}CClR^{3}R^{4}}}}
{\displaystyle {\mathsf {R^{1}R^{2}CCl{\text{-}}N{\text{=}}N{\text{-}}CClR^{3}R^{4}+2X^{-}\rightarrow R^{1}R^{2}CX{\text{-}}N{\text{=}}N{\text{-}}CXR^{3}R^{4}}}}{\displaystyle {\mathsf {X=RS^{-},\ CN^{-},\ CH_{3}COO^{-},\ R_{3}Al}}}Первый представитель ароматических азосоединений — азобензол — был впервые получен в 1834 году Э. Мичерлихом восстановлением нитробензола в щелочной среде, этот метод применяется и поныне[4]:
{\displaystyle {\mathsf {2ArNO_{2}+[H]\rightarrow Ar{\text{-}}N{\text{=}}N{\text{-}}Ar+H_{2}O}}}
Симметрично замещённые ароматические азосоединения также могут быть синтезированы окислением соответствующих ариламинов[5]:
{\displaystyle {\mathsf {2ArNH_{2}+[O]\rightarrow Ar{\text{-}}N{\text{=}}N{\text{-}}Ar+H_{2}O}}}а несимметричные могут быть получены конденсацией ароматических аминов с нитрозосоединениями:
{\displaystyle {\mathsf {2ArNH_{2}+Ar'{\text{-}}N{\text{=}}O\rightarrow Ar{\text{-}}N{\text{=}}N{\text{-}}Ar'+H_{2}O}}} Наиболее широко применяемым методом синтеза функционализированных ароматических азосоединений является азосочетание — реакция диазониевых солей с ароматическими соединениями, несущими электрондонорные заместители, этот метод применяется в промышленности в синтезе азокрасителей: