
Ocherki_klinicheskoy_biokhimii
.pdf
151
10.3. Метаболические последствия почечной недостаточности
10.3.1. Гиперкалиемия. В почках функционирует юкста – гломерулярный аппарат, функция которого – регуляция системного давления на основеизменений кровотока почки и электролитного состава вторичной мочи. Механизм, который позволяет почке реализовать столь важную функция, носит название ренин – ангиотензиновой системой. (иногда добавляют слово «альдостероновой»)
(https://biokhimija.ru/gormony/mineralokotikoidy.html)
Относительно альдостерона важно знать следующее. Ангиотензин – 2 стимулирует секрецию альдостерона из клубочковой зоны коры надпочечников, и чем больше снижен кровоток почки, тем более выражена интенсивность действия РАС и тем сильнее выброс альдостерона. Альдостерон действует на эпителиоциты дистальных отделов канальцев нефрона, усиливая там транспорт натрия в кровоток. Взамен, по типуантитранспорта, во вторичную мочууходят ионы калия.
К чему я?
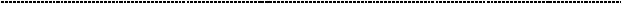
152
Повреждение клеток – мишеней данной системы – почечных канальцев,
приводит к сбою работы данной системы. В результате растёт уровень калия в крови. Однако, при преренальной почечной недостаточности, она, наоборот,
работает в усиленном режиме, тем самым поддерживая объём циркулирующей крови за счёт усиленной реабсорбции натрия. Но следует помнить, что снижение перфузии почек рано или поздно приведёт к ишемическому повреждению почечнойтканииплавномуприсоединениюренальнойпочечной недостаточности.
Главное клинически значимое последствие: ухудшение прохождения возбуждения по проводящей системе сердца; удлинение рефрактерного периода сокращения кардиомиоцитов в результате чего ухудшается сократимость сердца. При выраженной гиперкалиемии существует риск фибрилляции желудочков или остановки сердца.
- метаболический ацидоз (глава 12)
10.4.КФК как маркер поражения мышечной ткани
Всилу такой важной функции, как обеспечение адекватной биоэнергетики,
которую выполняет КФК в мышцах, логично предположить, что данного фермента там много. Как и во всех случаях повреждения клеток, КФК можно также обнаружить в крови в высокой концентрации при поражении мышечной ткани.Но есть нюанс. КФК – это гетерогенная группа ферментов, которая включает в себя КФК – ММ (скелетная мускулатура), КФК – МВ (сердечная мышца) и КФК – ВВ
(ЦНС). Определение этих фракций имеет для диагностики важное значение, в
зависимости от ведущей локации повреждения, мы будем наблюдать подъём в крови разных фракций.
Причины повышения КФК + КФК – ММ:
Прежде всего, это рабдомиолиз при самых разных состояниях.
- ишемия конечностей и краш – синдром, травматическое повреждение мышц
Длительная компрессия магистральных сосудов (чаще всего при сдавлении чем либо тяжёлым для этого) конечностей, вызывает ишемию мягких тканей и рабдомиолиз, связанный как с непосредственным действием повреждающего
153
фактора, так и с таким фактором, как ишемия. Рабдомиолиз опасен накоплением токсических продуктов распада тканей, нарушением проницаемости миоцитов.
При восстановлении кровотока происходит попадание в системную гемодинамику продуктов распада тканей, большого количества миоглобина. Последний фактор приводит к обструктивной нефропатии (ренальный вариант острого почечного повреждения)
- судорожная активность, злокачественная гипертермия
Генерализованные судороги – серьёзная проверка на прочность для скелетной му скулатуры. Это работа, которая осуществляется без учёта потребностей миоцитов в кислороде, по сути являясь истощающей и часто приводящей к повреждению мышечной ткани и рабдомиолизу.
- воспаление иммунопатологического природы - полимиозит, дерматомиозит,
системная склеродермия
Данные заболевания связаны с неадекватным ответом и деструктивным ответом на взаимодействия с аутоантигенами собственных тканей. В случае дерматомиозитаэтотРНК–аминоацилсинтетаза,аименноеёантигеныJo–1,Pl–7,Pl
– 12, EJ и т.д), антигены ядрышка PM – Scl, р56. Почему так происходит, сказать в двух словах сложно. В целом, это связано с нарушением толерантности иммунной системы к конкретнымантигенам,всилулибонедостаточнойселекцииаутореактивныхклонов,либо инактивацииT–reg–популяциилимфоцитов,ивсёэтоврезультатевоздействиятриггеров,
которых может быть, как вирусная инфекция, так и что угодно, причины до конца не выяснены. Антитела к вышеуказанным антигенам составляют так называемый
«миозитный профиль» и используются в серологической диагностике дерматомиозита.
Примечательно,чтодлякаждоговариантасистемныхзаболеванийсоединительнойткани,
свой набор антител. Возвращаясь к нашей реальности, скажу. Что одним из проявлений дерматомиозита служит рост КФК – ММ. Она может служить своеобразным скринингом для данного заболевания.
154
- воспаление инфекционного и паразитарного генеза
К одним из наиболее частых относят трихиннелёз – паразитарное заболевание,
возникающее у любителей поедать сырое, термически необработанное мясо,
приобретённое неизвестно где. Трихинеллы мигрируют из ЖКТ и оседают в мышцах, чаще всего в трапециях имышцах плечевого пояса, но теоретическиэто могут быть любые мышцы, в том числе дыхательная мускулатура. В месте своего пребывания они вызывают инфильтративные изменения, которые к 4 – 5
недели сменяются образованием фиброза, покрытого соединительно тканной капсулой. В неудачных для человека ситуациях, трихинеллы могут не ограничиваться лишь поперечно – полосатой мускулатурой.
- метаболические изменения в виде гипертиреоза, гипертрофии надпочечников; в
виде дефицита фосфорилазы (мышечные гликогенозы, глава 9)
- наследственно обусловленные – миодистрофии различного варианта.
Распространённым вариантом является миодистрофия Дюшена, возникающая из
- за мутации гена дистрофина. Дистрофин – внутриклеточный белок миоцитов,
имеющий важное значение для структуры мышечной ткани. Отсутствие дистрофина приводит к постепенной дегенерации скелетной мускулатуры,
манифестирующим в детстве и постепенно приводящим к генерализованной миопатии. Любопытно, что часто такие дети умирают от пневмонии и ДН,
обусловленной и спровоцированной нарушением внешнего дыхания в результате слабости дыхательной мускулатуры. Во всех случаях рабдомиолиза, будет повышение фракции КФК – ММ. Однако, есть состояния, в которыхповышается уровень другой фракции – КФК – МВ. Об этом мы поговорим позже..
155
Глава 11. Наиболее значимые и редко обсуждаемые
энзимопатии в контексте азотистого обмена
11.1.Нарушения обмена мочевины
Впрошлой главе мы доблестно обсуждали значение процесса обезвреживания аммиака для организма, а также касались процесса образования мочевины.
Пришло время обсудить нарушения орнитинового цикла.
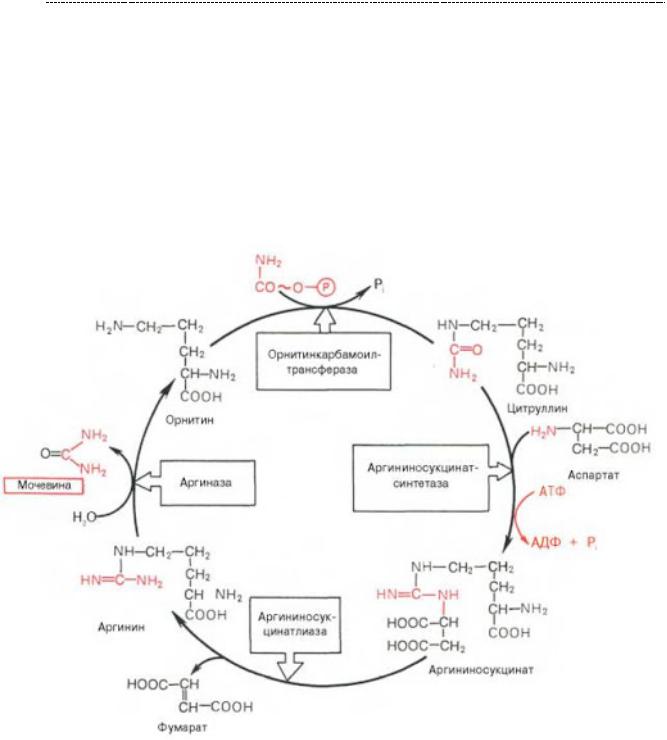
Нарушение образования мочевины является результатом активности следующих ферментов:
-N- ацетилглутаматсинтаза (считается наиболее тяжёлым вариантом)
-карбомоилфосфатсинтетаза I (гипераммониемия I типа, на схеме фермент не указан)
156
-орнитинкарбомоилтрансфераза (гипераммониемия II типа, Х – сцепленная)
-аргининсукцинатсинтетаза (цитруллинемия I и II типов)
-аргининсукцинатлиаза (аргининемия)
Мы не касались (чтобы не добить твой мозг окончательно) определённых моментов в обмене азотистых соединений в печени, но сейчас самое время прояснить ряд моментов.
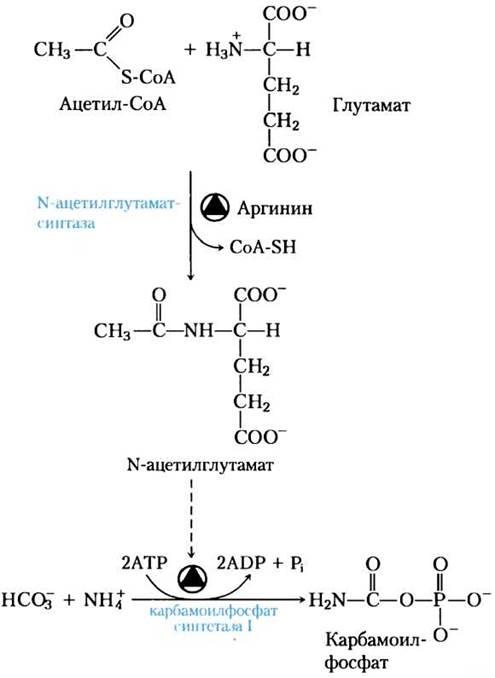
Поступающий в печень, либо образующийся в ходе реакций трансаминирования,
глутамат под действием N –ацетилглутамат – синтазы превращается в N –
ацетилглутамат.
157
Как мы видим, ацетилглутамат является ко – активатором карбомоилфосфат – синтетазы I. Также существуют данные. что N – ацетилглутамат в серии реакций превращается в орнитин – один из компонентов цикла мочевины. Это значит, что при высоком уровне распада белка и повышении азотистой нагрузки, будет образовываться большое количество глутамата и интенсифицироваться процесс образования мочевины, т.е. обезвреживания аммиака.
Считается, что чем «проксимальнее» дефект гена, кодирующего фермент цикла мочевины, тем тяжелее протекает заболевание. Тем не менее, они все ведут к одним и тем же, закономерным в данном случае, биохимическим изменением:
гипераммониемии. Различить формы нарушений орнитинового цикла можно по биохимическому профилю. Чтобы максимально упростить изложение, осветим,
что:
-при гипераммониемии II типа будет наблюдаться оротовая ацидурия (мы коснулись её в главе, посвящённой нарушением обмена пиримидинов), снижение цитруллина и аргинина
-При цитруллинемии будет обнаруживаться высокий уровень цитруллина в крови и моче при сниженном или нормальном уровне орнитина и оротовой кислоты
-при аргининемии – аргинин в крови и моче при сниженном или нормальном уровне цитруллина, орнитина и оротовой кислоты
-при при гипераммониемия I типа будет наблюдаться снижение «вышележащих»
компонентов орнитинового цилка
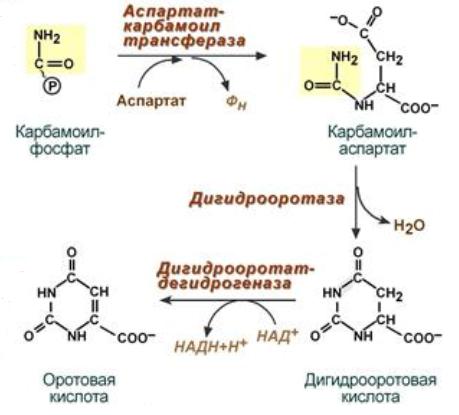
В отношении оротовой ацидурии у неискушённого читателя может возникнуть недоумение, ведь мы рассмотрели её в рамках нарушения обмена пиримидинов.
Поясню. В условиях блока на уровне – орнитинкарбомоил - трансферазы,
карбомоилфосфат диффундирует в цитозоль клетки, где используются для синтеза пиримидинов, в том числе мочевой кислоты.
Это является дифференциальным признаком данной гипераммониемии. Вотличии от ородовой ацидурии, обусловленной блоком оротатфосфорибозил – трансферазы, здесь присутствует гипераммониемия.
158
Заподозрить нарушение обмена мочевины клинически удаётся далеко не всем и не всегда, что связано с редкостью данной патологи. Её не часто заподазривают.
Однако, для всех видов нарушений орнитинового цикла есть ключевые клинические признаки, позволяющие подумать и заподозрить о нарушении обмена мочевины:
•Манифестация в первые месяцы жизни и связь метаболических «кризов» с
началом белкового питания (прикорма – 4 - 6 мес)
•Картина угнетение центральной нервной системы (синдром вялого ребёнка): -
заторможенность, угнетение сознания вплоть до комы
-вялое сосание, иногда отказ от груди/смеси
-судорожный синдром различной вариации
-гипотония и гипорефлексия
-задержка психомоторного развития
•Низкий темп массовых и ростовых прибавок
159
• Расстройства ЖКТ в виде срыгиваний, рвоты, диареи
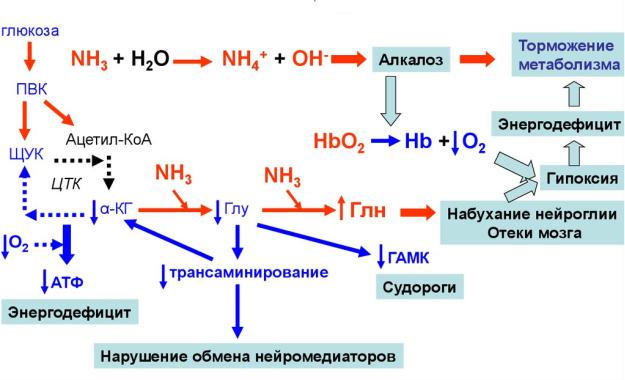
Напомню, что токсичность аммиака связывается с истощением пула глутамата
(который пытается его связать и обезвредить) и а – кето – глутарата (то, во что должен превращаться глутамат) с последующим угнетением ЦТК, что особенно травматично для нервной ткани. Помимо этого, повышение содержания глутамата в клетках ведёт к их набуханию, отёку и нарушению функционирования. Картина усугубляется алкалозом тканей, в силу того, что аммиак связывает протоны с образованием иона аммония. В условиях повышения рН наблюдается повышение сродства гемоглобина к кислороду, и он хуже отдаёт его тканям, тем самым усугубляя энергетический дефицит и все функции нейронов. В этих условиях, о
гармоничном развитии и функционировании ЦНС не может быть и речи.
(слайд с лекции Гаврилова И.В,)
Особого внимания заслуживает гипераммониемия II типа, которая является наиболее частым вариантом и является Х – сцепленной, т.е. передаётся от мамы.
Женщины – гетерозиготы могут не подозревать об имеющимся дефекте в их геноме в силу наличия нормального аллеля гена (одного аллеля вполне достаточно для нормальной работы орнитинового цикла). Единственным проявлением,
зачастую, является замедленный темп роста в детском возрасте. Длямальчиков это заболевание является фатальным, часто не оставляя им шансов в самом раннем
160
возрасте. Существует лечение нарушений орнитиновго цикла. Медикаментозное лечение направлено на обхождение ферментативного блока, а также насвязывание токсичного аммиака. С этой целью применяют бензоат натрия,
фенилацетатнатрия которые связывают аммиак с образованием растворимых и нетоксичных солей и выводятся почками. К сожалению, данные препараты не зарегистрированы в РФ. Наиболее эффективна пересадка печени, но не все дети доживают до возраста, когда возможна пересадка.
Важно помнить, что катаболические ситуации (стресс, инфекции, приём глюкокортикостероидов, травма и прочее) будет способствовать усилению белкового катаболизма и метаболическому кризу. Такая закономерность характерна и для других нарушений азотистого обмена.
11.2. Тирозинемия.
Тирозин является условно заменимой кислотой и характеризуется весьма интересным и сложным метаболизмом. Он даёт начало пигменту меланину;
катехоламинам; тиреоидным гормонам. Катаболизируясь, он проходит ряд этапов,
конечным из которых является образование фумарата и ацетоацетата.
Существует несколько вариантов нарушения его метаболизм. Они характеризуются различными проявлениями и степенями тяжести – от лёгкой, не требующей вмешательства, до тяжелейшей. Разберём наиболее актуальные и опасные для жизни.
11.2.1. Тирозинемия I типа.
Блок на уровне фумарилацетоацетатгидролазы является наиболее тяжёлым вариантом нарушения обмена тирозина. Блок данного фермента ведёт к накоплению токсичных метаболитов: малеилацетоацетата, фумарилацетоацетата,
сукцинилацетоацетата и сукцинилацетона. Токсичность имеет разные векторы,
которые суммируются и выдают просто невообразимый результат на жизнь маленького, ни в чём не повинного, но уже больного ребёнка.
