
Ocherki_klinicheskoy_biokhimii
.pdf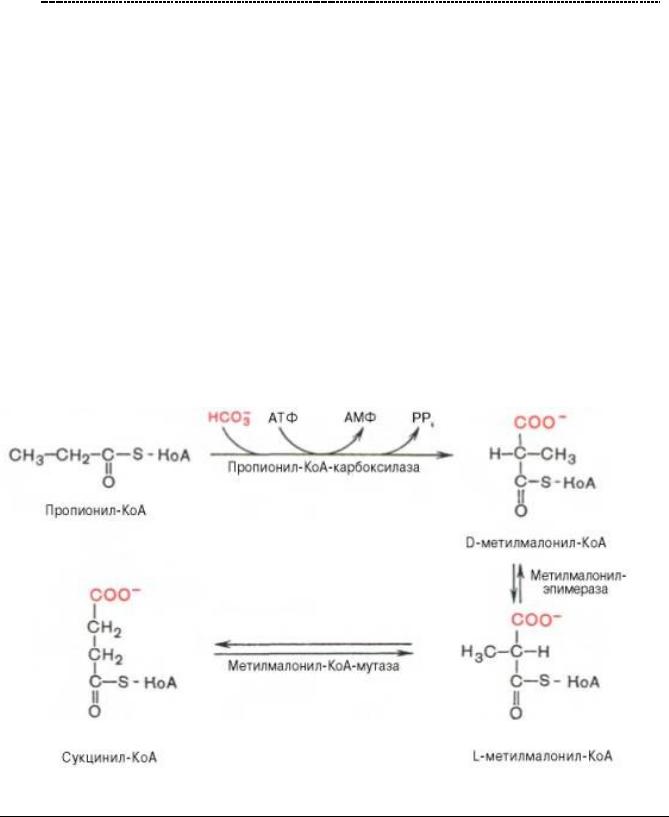
81
-конечный продукт – молекулы Ацетил – КоА– необходимого субстрата для цикла трикарбоновых кислот
-получение энергии обусловлено получением восстановлением ФАД до ФАДН2 и
НАД до НАДН + Н. Данные восстановительные эквиваленты играют роль донаторов электронов в электрон – транспортной цепи, и в конечном счёте, для получения энергии.
-Вцелом, окислением одной жирной кислоты можно получить, в среднем, 90– 130
молекул АТФ. Братан, это очень много, особенно для одной молекулы.
- На последней стадии окисления образуется не ацетил – КоА, а пропионил –КОА.
Путём нехитрых превращений, она останется сукцинилом – КоА – активным участником того же ЦТК
(изображение взято с интернет - портала https://biokhimija.ru/lipidy/beta-okislenie.html )
Метаболизм углеводов и липидов характеризуется наличием ещё и сложных анаболических реакций, которыми я пока не хочу нагромождать и без того огромнейшую главу. Какие - то моменты по анаболизму я поясню чуть позже,
когда коснусь проблемы заболеваний. (часть III)
82
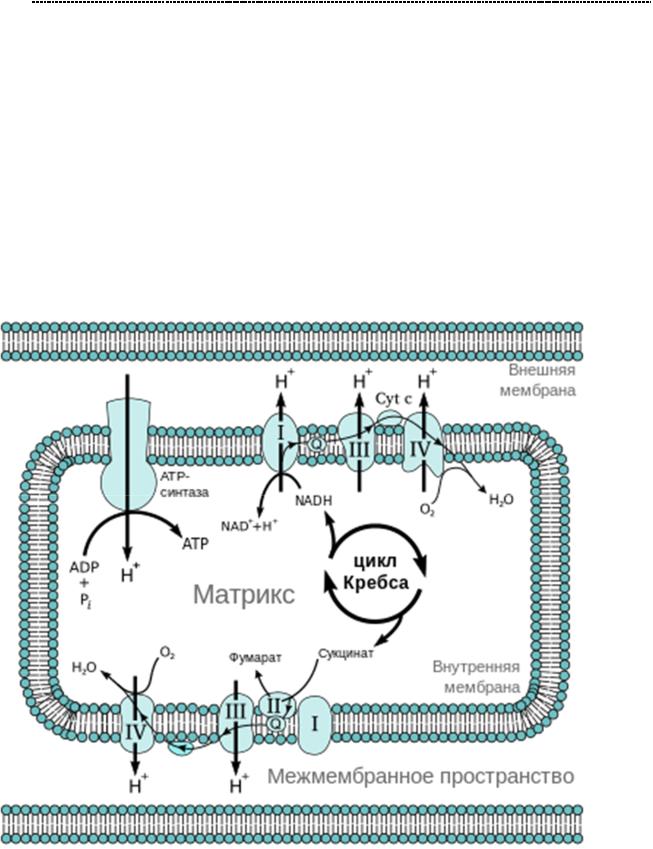
Глава 5. Окислительное фосфорилирование и электрон –
транспортная цепь.
В главных ролях:
Комплекс 1 – НАДН – оксидаза; Комплекс 2 – Сукцинатдегидрогеназа (-
ФАДН2); Комплекс 3 – убихинон – цитохром С – редуктаза; Комплекс
4 – цитохром С – оксидаза;
5 – АТФ - синтаза
(иллюстрация взята с Википедии)
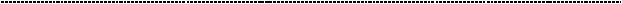
83
Вся эта пьеса заключается в перекидывании электронов от менее отбитого к более отбитому – молекуле кислорода. Перенос электронов осуществляется от более электроотрицательного (больший минус) к менее отрицательному(меньшемуминусуилибольшемуплюсу), посути, здесьдействует стандартная электродинамика. Движение электронов к более положительному участнику сопровождается выбросом энергии. Её не хватит, чтобы накормитьтебя после экзамена по биохимии, зато хватит, чтобы перекинуть протоны против градиента концентрации в межмембранное пространство митохондрий. (см.
рисунок)
В межмембранном пространстве скапливаются протоны. Обратно в матрикс митохондрий им не вернутся. По мере движения электронов, протоны скапливаются в межмембранном пространстве, где нарастает электрический и химический потенциал. Достигая определённой величины, он прорывает АТФ – синтазу (она открывается при определённом потенциале). Протонный градиент становиться источником энергии для синтеза АТФ, переводя энергию,
высвобождающуюся при движении протонов, в энергию магроэргических связей АТФ.
Но где первоисточник электронов и протонов?
Ответ: восстановительные эквиваленты в виде НАДН и ФАДН2.
НАДН,образуясьв6реакциигликолиза, рядереакцийЦТК,В–окислениижирных кислот, передаёт свои электроны на НАДН – оксидазу.
Сукцинатдегидрогеназа забирает электроны от ФАДН2 (В – окисление жирных кислот, ЦТК). И с 1 и с 2 комплексов, электроны передаются на убихинон. Тот, в
свою очередь, как шестёрка, передаёт всё нацитохром С. (Убихинон – Цитохром С
– редуктаза). Но у цитохрома С есть старший брат – «цитохром – С - оксидаза» Но и ему электроны не приносят счастья. Правой рукой он кидает их в кислород,
который, впитывая их и протоны, образует воду.
84
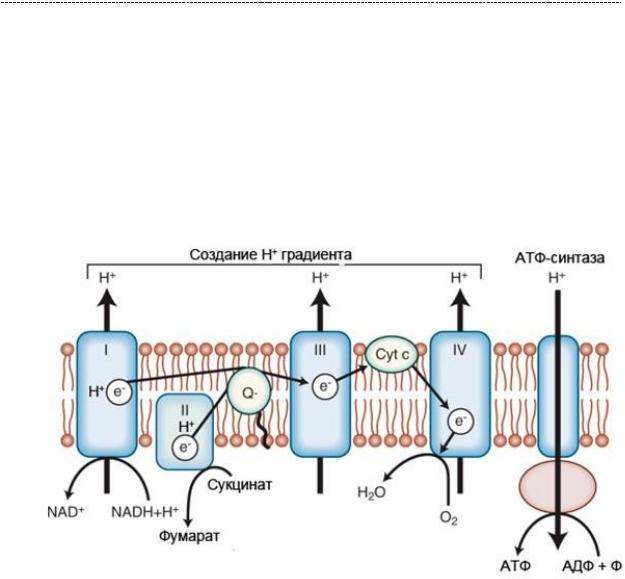
Всё, что ты должен усвоить из этой главы: кислород – конечный акцептор электронов. Если его в клетке нет, ЭТЦ останавливается. Протонный градиент не создаётся, АТФ не синтезируется, клетка страдает от острой нехватки энергии, в результате чего останавливаются в своей работе её ферментативные системы, натрий – калиевая АТФ – аза. Клетка испытывает глубокие повреждения, нарушается её целостность и метаболизм, что является биохимической основой ишемического (по сути гипоксического) некроза.
(иллюстрация взята с интернет – портала https://studopedia.su/20_16709_biologicheskoe-
okislenie-dihatelnaya-tsep.html)
85
Часть Ш. Биохимическая природа распространённых заболеваний
Любое заболевание начинается с тончайших, неуловимых глазом, изменений.
Изменений на молекулярном уровне, начиная с генов и нарушений в протекании метаболических путей. Биохимия – азбука заболеваний. Различные молекулярные нарушения являются буквами, кирпичиками, формирующее заболевание во всех его проявлениях. Они лежат в основе, у истоков «макроскопических» и клинических проявления. Более того: пути полного преодоления заболеваний лежат во вмешательстве в молекулярные механизмы их формирования: именно там нас ждёт множество мишеней для лекарственной терапии, как уже известных, так и тех, что только предстоит открыть. Здесь много потенциала для потенциальных нобелевских лауреатов. Ведь процесс расшифровки наукой биохимической основы заболеваний, по моим впечатлениям, нескончаемый.
В этой, третьей части книги я поделюсь выжимкой того, что известно на сегодняшний день о некоторых распространённых, в той или иной степени,
заболеваниях, природа возникновения которой хорошо объясняется с позиции биохимии. Здесь будет акцентировано внимание на роли метаболических нарушений в развитии заболеваний.
От нашего внимания не ускользнут и вопросы, касающиеся интерпретации результатов биохимического анализа крови. Необходимость этого продиктована тем, что лабораторные показатели в определённой степени адекватности отражают динамику развития многих патологических состояний.
Сказать по правде, это именно то, ради чего я занялся написанием данной книги.
В учебной программе поразительно мало уделяется внимания и времени вопросам молекулярной природе заболеваний. Но мы с вами сделаем первый шаг к исправлению этой досадной ошибки.

86
Глава 6. Нарушение метаболизма пуринов и пиримидинов.
6.1. Подагра и гиперурикемия. В чём отличие подагры от простой гиперурикемии? Гиперурикемия – это лабораторный феномен, суть которого – увеличение содержания в крови мочевой кислоты. Не во всех случаях гиперурикемия приводит к возникновению клинически значимых симптомов.
Подагра – это заболевание, характеризующееся отложением кристаллов мочевой кислотывтканях.Большевсегодостаётсяпочкамисуставом.Подагранеслучается без гиперурикемии. Но как же последняя приводит к такому тяжёлому заболеванию?
Мочевая кислота имеет свой предел растворимости. В чрезмерно кислой среде
(ниже 5,7) она оседает в виде кристаллов уратных солей в мягких тканях. Оседая в суставах, они вызывают чрезвычайно болезненные ощущения. Первым достаётся пальцам ног. Ураты являются по отношению к тканям чужеродным соединением.
В силуэтого, в тканяхреализуется типовой патологический процесс – воспаление,
которое в данном случае имеет скорее разрушающее, нежели защитноедействие.
Но почему так происходит? Бывают случаи, когда мочевой кислоты образуется слишком много.
А) повышенное образование пуринов и их повышенный распад
(логичное следствие).
Здесь причиной – генетически детерминированная чрезмерная
активность фосфорибозилпирофосфат – трансферазы (катализ первой реакции
синтеза пуринов), которая становиться менее чувствительной к отрицательным
регуляторным факторам – ГМФ, АМФ.
(изображение взято с интернет - портала http://scask.ru/k_book_bio2.php?id=231)

87
Б) недостаточная реутилизация
Бывает так, что распадающиеся пурины утилизируются хуже, чем положено (не по плану) в силу дефектов гипоксантин – гуанин – фосфорибозил трансферазы (фермента, переводящего гипоксантин в ИМФ, а гуанин в ГМФ). В
результате мы получаем большое количество мочевой кислоты.
Ситуация может усугубляться, если с пищей поступает большое количество нуклеиновыхкислот,которые,распадаясьнапурины,превращаютсявэнтероцитах в мочевую кислоту и в таком виде всасываются в кровь. Алкоголь нарушает выведение мочевой кислоты (по пока неясным для меня самого причинам). При гиперурикемии противопоказаны диуретики (препараты, усиливающие выведение мочи, в особенности тиазидной группы), так как повышают риск уратной нефропатии. Как видишь, гиперурикемия создаёт сплошные трудности. В
отношении подагры надо сказать, что это инвалидизирующее заболевание,
снижающее качество жизни и увеличивающее риск сердечно – сосудистых заболеваний.
Терапевтический подход. По вышеуказанным причинам, первым вектором лечения подагры будет соблюдение диеты, которая заключается в отказе от потребления тех продуктов, которые в большом количестве содержат пуриновые основания. Исключаются пиво, кофе, чай, шоколад, мясные продукты, печень,
красное вино. Предпочтение отдается вегетарианской диете с количествомчистой воды не менее 2 л в сутки.
Медикаментозный подход заключается в применении аллопуринола – конкурентного ингибитора ксантиноксидазы, той самой, что переводит ксантины в мочевую кислоту. Это терапия первой линии.
(изображение взято с интернет – портала https://biokhimija.ru/obmen-purinov/bolezni-purinovogo-
obmena.html)
88
В силу того, что аллопуринол отнимает всё внимание ксантиноксидазы,
превращаясь в хорошо растворимый аллоксантин, ксантин и гипоксантин, будучи обиженными на сложившуюся ситуацию, покидают организм с мочой.
6.2.Уратная нефропатия создаёт массу проблем. Надо сказать, что сам термин
«уратная нефропатия» сегодня используется реже, чем ранее, кем - то и вовсе считается неправильным. Несмотря на это, именно так мы назовём поражение почек при гиперурикемии. Часто именно ураты формируют мочевые камни,
становясь основой для мочекаменной болезни и вторичного пиелонефрита *.
Около половины людей, страдающих подагрой, страдают ещё и мочекаменной болезнью.
Механизм камнеобразования, в данном случае, провоцируется повышением кислотности (понижением рН) мочи. Это делает возможным переход мочевой кислоты в плохо растворимую форму:
((изображение взято с интернет – портала https://biokhimija.ru/obmen-purinov/bolezni-purinovogo-
obmena.html)
Мочекаменная болезнь опасна наличием риска возникновения острой задержки мочи, которая становится причиной острой постренальной почечной недостаточности, что является угрожающим жизни патологическим состоянием.
-----------------------------------------------------------------------------------------------------------------------------
--------
Вторичный пиелонефрит – воспалительное поражение чашечно – лоханочной системы, возникшее на фоне нарушения уродинамики («движения мочи» по мочевыводящим путям), часто на фоне мочекаменной болезни, но не только. Возникающий стаз мочи делает возможным задержку и размножение бактерий в чашечно – лоханочной системе. Более подробно ищи в учебниках по урологии
89
6. 3. Синдром Леша – Нихана.
Вслучае наличия мутации гена, кодирующего гипоксантин – гуанин – фосфорибозил трансферазу, реализуется синдром Леша - Нихана. Наследуется это Х – сцепленно, а это значит, что достаётся только парням. Но не часто (реже чем могло бы быть, но чаще, чем хотелось бы), это грозит одному человека из380
тысяч.
Особенность этого синдрома в том, что здесь имеется грозная неврологическая и психическая симптоматика с самого раннего возраста: умственная отсталость и снижение темпов психомоторного развития; нарушения двигательныхфункций по типу хореатетоза, аутоагрессивное поведение. (ребёнок пытается нанести себе вред, что в условиях умственной отсталости закономерно. Но по той же причине такие попытки не всегда удачны). К сожалению, патофизиологические механизмы развития поражения ЦНС при болезни Лёша—Нихена не ясны по сей день. «Так,
несмотря на широкий спектр проблем, связанных с гиперпродукцией МК,
причинно-следственнаясвязьмеждунимииневрологическимииповеденческими проявлениями не установлена, и терапия аллопуринолом, проводимая с момента рождения, не влияет на поражение ЦНС»
проявления и варианты течения, анализ собственного опыта» М.С. Елисеев, В.Г. Барсакова,
Журнал «Современная ревматология №3, 10)
Помимо поражения нервной системы, такие дети не лишены и уратной нефропатии, а также подагры. Оба этих патологическихсостояния развиваются по рассмотренным нами выше механизмам.
Последнее, что здесь стоит отметить: спектр клинических проявлений варьирует в зависимости от степени утраты активности фермента. Так, при активности ферментаниже1,5%отнеобходимой, развиваетсяполныйспектрвышеописанных клинических проявлений, в том числе и аутоагрессивное поведение, когнитивную недостаточность. Это является следствием поражения коры головного мозга. При сохранении активности фермента в интервале от 1,5 до 8% от необходимой,
признаки поражения коры, чаще всего, не прослеживаются.
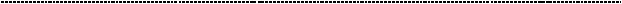
90
Но имеются иные неврологические нарушения, проявляющиеся разной степени выраженности экстрапирамидной и пирамидной моторной дисфункцией, и
связанные с гиперурикемией. Сохранение активности фермента свыше 8 %
проявляется лишь уратной нефропатией, (нефролитиазом – образованием камней
в мочевыводящих путях) п подагрой.
6.4.Синдром лизиса опухоли.
Ряд опухолевых заболеваний (чаще это гемобластозы – лейкозы,
лимфомы, режесолидныеопухоли–ракжелудка, лёгкого, молочнойжелезыит.д.)
может давать картину острой почечной недостаточности в ответ на проводимую химиотерапию. Распадаясь и разрушаясь от действия химиопрепаратов
(флударабин, метотрексат, да и многие другие), опухолевые клетки выбрасывают в кровь большое количество мочевой кислоты, калия и фосфора. Последствия бывают достаточно серьёзные:
- гиперурикемия провоцирует развитие нефролитиаза почечных канальцев и развитие ренальной почечной недостаточности.
- гиперкалиемия провоцирует развитие тяжёлых сердечных аритмий,
вплоть до остановки сердца (усугубляется вторичной гипокальциемией) в связи с угнетением атриовентрикулярной проводимости в сердце
- гиперлактатемия (связана с высокой активностью в опухолевых клетках анаэробного гликолиза и обусловливающее высокое содержание в них лактата), с риском развития метаболического ацидоза
К метаболическим изменениям при синдроме лизиса опухоли также относят повышение уровня остаточного азота в крови (в частности мочевины, что выступает как проявление повышенного катаболизма белков клеток), вторичную гипокальциемию на фоне гиперфосфатемии, изменение кислотности крови – ацидоз.
Гиперурикемия при несоответствии возможностям почек, провоцирует мочекислый нефролитиаз с развитием мочекислой нефропатии (по указанному в
1.6.2 механизму) и острой ренальной почечной недостаточности.
