
Ocherki_klinicheskoy_biokhimii
.pdf
51
(источник иллюстрации: интернет – портал http://toxicology.narod.ru/book28.html)
Различные рецепторы к факторам роста (эпидермальному, фибробластитческому,
тромбоцитарному, инсулиноподобным) при взаимодействии со своим лигандом индуцируют активацию каскада внутриклеточных биохимических реакций,
приводящих к изменению транскрипции различных циклин – зависимых киназ и других участников, обусловливающих продвижение клеточного цикла по фазам.
Реакции, запускающие смены фаз клеточного цикла, сложны и многогранны, но их суть сводится к активации определённых транскрипционных факторов, которые, в
свою очередь, обеспечивают считывание генов, ответственных за экспрессию
«белков – участников» клеточного цикла. В нижележащей схеме факторы роста обозначены как «факторы выживания»:

52
(источник иллюстрации: ФЛАВОНОИДЫ: БИОХИМИЯ, БИОФИЗИКА, МЕДИЦИНА - ТараховскийЮ.
С. – 2013)
Представляяэтусхему, немогунеотметить,чтодлямногихклетоквзаимодействие с ихмикроокружением (в частности, с внеклеточным матриксом) является важным условием (необходимым) для пролиферации. К таким клеткам можно отнести клетки эпителиальной гистологической структуры. Они требуют для своей пролиферации контакта с внеклеточным матриксом соединительной ткани,
который реализуется путём взаимодействия белков этого матрикса с интегринами Как показано на схеме, они участвуют в активации белков Ras – центральных внутриклеточных протеинкиназ сигнальныхпутей путей МАРК (МАРК – mitogen activated protein kinase - митоген – активируемые протеин киназы – киназы,
активируемые митогенными факторами и приводящие к митозу клеток). По последним данным, гормоны щитовидной железы, в частности тетрайодтиронин,
служит лигандом интегриновых ICAM – белков (белков межклеточной адгезии),
тем самым способствуя пролиферации клеток.

53
Это, вомногом,определяетважную рольгормоновщитовиднойжелезыв развитии нервной системы у эмбриона/плода и у детей и объясняет задержку психомоторного развития при врождённом гипотиреозе – врождённой недостаточности щитовидной железы. С другой стороны, это объясняет повышенныйрисквозникновенияипрогрессированиязлокачественнойопухоли на фоне гипертиреоза. *
Бывает так, что в генах, кодирующих участников этой передачи ростового сигнала,
происходит мутация, т.е. стойкое и необратимое изменение структуры того или иного гена. Это происходит при воздействии самых разных причин физической
(радиация в виде ионизирующего излучения), химической (нитриты, карцерогены в примесях сигарет, различные фенолы и пр.), и биологических факторов (вирус Эпштейн – Бар, онкогенные типы вируса папилломы человека (16,18,31 и пр.), Helicobacter pylori, в сочетании с дефектом систем репарации («починки имеющихся дефектов путём вырезания «сломанных»фрагментов и синтезом на их месте новых или же другими путями), или системы апоптоза (генетически детерминированнойгибели клетки). Результат– функциональная аномалия клетки.
Она живёт и растёт теперь только по своим законам. Если точнее происходит гиперпродукциия и/или чрезмерная спонтанная активность определённого участника МАРК – путей (начиная от рецепторов к факторам роста, белков Ras, PKC и прочие) и полной автономии, независимости от каких – либо митогенных сигналов и отрицательной обратной связи. Такие гены называются протоонкогенами. В нормальных условиях они обеспечиваю выживание клетки тогда, когда это необходимо в рамках гистогенеза и строго при воздействии митогенных сигналов извне. К наиболее известным протоонкогенам относят.
Гипертиреоз – повышение функциональной активности щитовидной железы, повышенная
продукция тиреоидных гормонов (Т3,Т4), формирующее своеобразную клиническую
симптоматику
54
- рецепторы к факторам роста (rEGFR,r FGFR,r IGF и проч), в результате которого происходит его спонтанная активация и реализация внутриклеточного каскада,
приводящего к неконтролируемой пролиферации клеток:
- мутации в «нижележащих точках», приводящие к гиперэкспрессии внутриклеточных участников трансдукции сигнала (допустим, белков RAS, BRAF,
протеин – киназа В, Bcl- 2)
Но,нарядусэтим,происходититак,чтомутациязадеваетгены,кодирующиебелки онкосупрессоры. Это белки, способные заблокировать клеточный цикл в случае наличия неисправимых повреждений ДНК и включить программу апоптоза. Она необходима тогда, когда клетка имеет необратимые повреждения ДНК. Хотя,надо сказать, что апоптоз – естественный и важный процесс эмбриогенеза и ряда физиологических процессов.
К наиболее известным белкам – онкосупрессорам относят p53, pRb, PTEN. И их функция различна. Так, р53 запускает программу апоптоза путём активации каспазы – 3, 8, 9 и других молекул – участников апоптоза. рRb или белок ретинобластомы, останавливает движение клеточного цикла в фазе G1, не давая клетке пройти дальше. Происходит это инактивацией соответствующих факторов репликации, в частности eF-2 (эукариотический фактор элонгации – 2). PTEN
является инактиватором различных участников МАРК – путей. Инактивация этих факторов в результате мутации их гена – важный элемент формирования большинства опухолей у человека.
Как результат мутаций в протоонкогенах и генах - онкосупрессорах, мы получаем клетку, неадекватно реагирующие на ростовые сигналы. Способные к автономному росту, инвазии (внедрению) в окружающие ткани, а в исходе – к
метастазированию в отдалённые уголки организма.
55
2.6.Биохимические аспекты цитостатической терапии, направленной на угнетение метаболизма ДНК.
2.6.1. Химиотерапия злокачественныхновообразований различной природы
на примере ингибиторов топоизомераз
Насегодняшнийденьдостигнутызначительныеуспехивлечениизлокачественных новообразований. Разработаны схемы и режимы химиотерапии для новообразований различной локализации и морфологической природы. Несмотря на различие этих схем, принцип действия химиотерапевтических препаратов, в
глобальном и общем смысле, является универсальным для данных лекарственных средств. Он заключается в остановке клеточного цикла и угнетениипролиферации опухолевых клеток, и каждая группа препаратов делает это по - своему. Главным недостатком «традиционной» химиотерапии является низкая селективность препаратов: они угнетают пролиферацию всех пролиферирующих клеток организма. Наиболее интенсивно в организме пролиферируют опухолевыеклетки.
Ингибиторы топоизомераз. В опухолевых клетках, в силу высокой пролиферативной активности, прослеживается высокая активность топоизомераз,
преимущественно I и II типов. Теканы (топотекан, иринотекан) ингибируют топоизомеразу I типа. Антрациклины (доксорубицин, идарубицин эпирубицин),
эпиподофиллотоксины (этопозид, тенопозид) являются ингибиторами топоизомераз II типа. В силу высокой важности топоизомераз для поддержания
«считываемой» пространственной ориентации нитей ДНК при репликации, их ингибирование является фатальным для опухолевой клетки. Указанные выше группы препаратов нашли широкое применение в онкологии. Так, антрациклины входят в схемы лечения солидных опухолей (в частности рак лёгкого, желудка),
гематологических опухолевых заболеваний.
К сожалению, данные типы топоизомераз присутствуют и в здоровых тканях организма. Это лежит в основе развития побочных эффектов, часто специфический именно для ингибиторов топоизомераз. Так, в последние годы
56
появляется всё больше сообщений о развитии антрациклиновой кардиотоксичности. Антрациклин – индуцированная кардиотоксичность – феномен, характеризующийся постоянно прогрессирующим снижением фракции выброса левого желудочка миокарда, т.е. так называемую кардиомиопатию.
Опасность заключается и в том, что зачастую очень сложно проследить развитие сердечной недостаточности в силу их поздней манифестации. С целью снижения кардиотоксичности химиотерапии антрациклинами, разработаны новые препараты – эпирубицин и идарубицин.
2.6.2. Химиотерапия аутоиммунных заболеваний на примере
антиметаболитов в контексте лекарственного влияния на синтез ДНК
Механизмы аутоиммунных заболеваний сложны. Но достаточно часто они включают в себя пролиферацию аутореактивных лимфоцитов. Это обусловлено угнетением негативной селекции аутореактивных (опасных в отношении тканей собственного организма) лимфоцитов, избеганием ими апоптоза. Лимфоциты относятся к группе быстро пролиферирующих клеток, поэтому в лечении множества аутоиммунных (иммунопатологических) заболеваний нашли цитостатики. Одними из наиболее известных являются антиметаболиты фолиевой кислоты, в частности метотрексат.
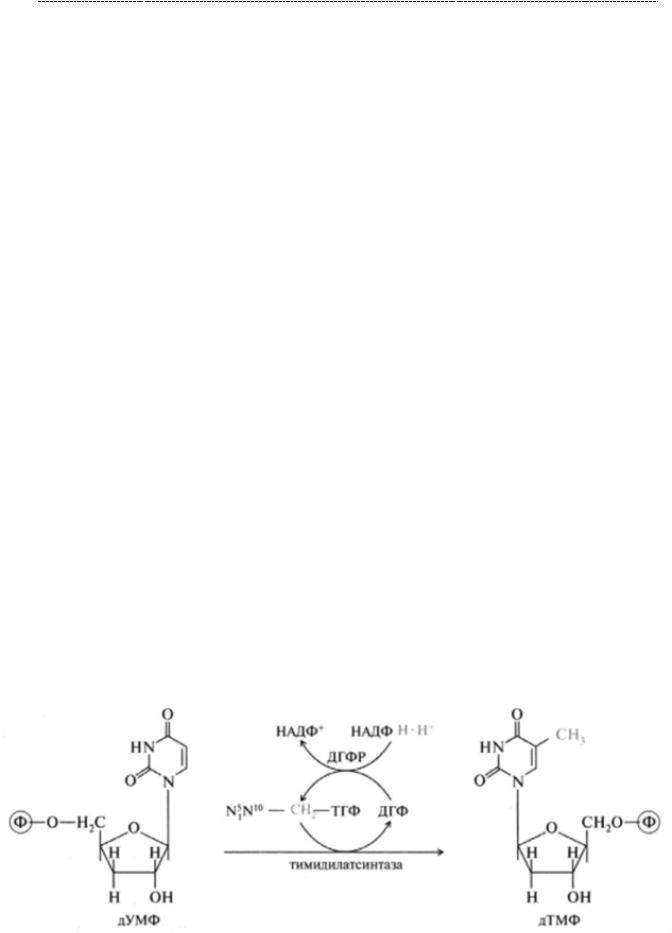
Метотрексат является ингибитором дигидрофолатредуктазы и тимидилатсинтетазы.

57
Конкурентное ингибирование данных ферментов приводит к снижению синтеза одного из субстратов, необходимых для репликации ДНК – дезокситимидинтрифосфата. Данный механизм действия обусловливает применение метотрекстата как в лечении опухолевых заболеваний
(преимущественно гемобластозов), так и аутоиммунных, в частности ревматоидного артрита, болезни Крона и неспецифического язвенного колита
(один из препаратов резерва), диффузные болезни соединительной ткани и пр.
Хотя, справедливости ради стоит отметить, что сейчас применяются более безопасные и эффективные препараты. Но метотрексат и по сей день не потерял своего значения. Особое место он занимает в лечении ревматоидного артрита – аутоиммунного поражения суставов и периартикулярных тканей, которое без лечения заканчивается контрактурой суставов, ограничением подвижности,
инвалидностью, амилоидозом внутренних органов и множеством других проблем.

58
Часть II. Биоэнергетика клетки
3.Катаболизм и биоэнергетика
Речь пойдёт о распаде макромолекул – преимущественно липидов и сахаров– до мономеров и воды с пеплом. А также обо всём, что с этими путями связано (а
связано очень много). Тема важная. Тема интересная. Порою, её понимание даёт ответы на ряд вопросов и вскрывает происхождение ряда ужасных картин,
которые ты можешь наблюдать в стационаре и в жизни, даёт адекватное понимание диететики и в целом делает тебя адекватнее. В этот раз ты узнаешь,
как и почему вафельки со сгущёнкой и шоколадкой не сделаю тебя сладкой конфеткой, а приведут к отложению ненужного жира в боках. Как выживает мозг, когда у тебя5 пар. Аесли серьёзно,то ещёя расскажу, почемубессмысленна безуглеводная диета,почемуразвиваетсяацидозикакиеизэтогопоследствия.Мы коснёмся базы, необходимой для понимания множества клинических проблем.
Места, объясняющие процессы распада углеводов и липидов местами могут показаться нудными, если знаешьих, пропусти (только попробуй).
3.1. Судьба углеводов в суровом организме. В главных ролях – глюкоза.
Взгляни на эту красоту. На это настоящее чудо биохимии, на одну из самых активных молекул нашего организма. По количеству реакций, вкоторыхона фигурирует, можнопо - началуподумать, что наша жизнь – способ существования глюкозы.
Мы имеем дело с 6 – атомный гидроксиальдегидом, имеющим 5
гидроксильных групп. Это делает её чрезвычайно водолюбивой и открывает

59
просторы для биохимического синтеза. В нашем организме функционирует L –
форма глюкозы, только такая форма способна участвовать в ферментативных
реакциях. |
(здесь она слева) |
3.1.1. Внешний обмен углеводов.
Об её источниках с пищей тебе хорошо известно. Это различные овощи и фрукты, оциллококцинум, сладости пряности и прочее. Гораздо интереснее, что с ней происходит при приёме per os.
Глюкоза попадает в виде полимеров – крахмала, целлюлозы, гликогена. Не извсех их можно с одинаковой эффективностью вылущить глюкозу. Крахмал и гликоген начинается расщепляться ещё в ротовой полости, благодаря а- амилазе изслюнных желёз. Происходит разрушение а – 1,4 гликозидных связей (связь между первым атомом углерода одной молекулы и 4 атомом соседней молекулы углевода). К
слову, в организме расщепляются только такие связи.
Процесспродолжается вкишечнике (просвете12 –перстнойкишки), где под действием а – амилазы поджелудочной железы происходит образование углеводных мономеров и димеров. В качестве мономеров не обязательно получается только глюкоза. Это может быть и фруктоза, и галактоза, но, как мы увидим дальше, все они имеют одинаковую судьбу. Далее начинается их абсорбция.
В абсорбции молекул моносахаров в кишечнике важную роль играет вторичный активный транспорт.

60
(изображение взято с интернет – портала https://biokhimija.ru/uglevody/trasnport-monosaharov.html)
Здесь всё максимально просто. Глюкоза (как и другие мономеры) нагло использует натрий. Увидев в нём внутренний потенциал в виде электрохимического градиента, она заманивает его на специальный белковый переносчик в мембране энтероцита. Тут то она и берёт его в оборот, заставляя оборачиваться вокруг своей оси ещё и белок – переносчик. Это происходит в результате изменения его конформации – пространственной взаимной ориентации компонентов его большой молекулы. Как результат, и глюкоза, и натрий оказывается внутри клетки. Поскольку натрий двигается по своему градиенту,
высвобождаясь от белка – переносчика, он высвобождает малое количество энергии. Этого количество достаточно, чтобы глюкоза расплатилась с переносчиком за такси через клеточную мембрану и спокойно ушла вглубь энтероцита. Увидев большой город в виде цитоплазмы энтероцита, глюкоза имеет два пути: остаться здесь (потом расскажу, что произойдёт) или двигаться дальшек своей мечте, для чего она прыгает в кровь. И тут начинаются высокие материи.
3.1.2. Путешествия глюкозы
Существует гомеостатический механизм, обеспечивающий поддержание физиологического уровня глюкозы в крови, и он сложнее, чем кажется на первый взгляд. Главным её компонентом и сигналом, её хэдлайнером, является глюкоза. А
