
- •Микробиология производства хлеба, кондитерских и макаронных изделий
- •Федеральное агентство по образованию
- •Микробиология производства хлеба, кондитерских и макаронных изделий
- •Введение
- •1. Микроорганизмы, используемые в хлебопекарном производстве
- •1.1. Дрожжи
- •1.1.1. Строение дрожжевой клетки
- •1.1.2. Классификация дрожжей
- •1.1.3. Размножение дрожжей
- •1.1.4. Характеристика дрожжей, используемых в хлебопекарном производстве
- •Оценка дрожжей по показателю мальтазной активности
- •1.1.5. Штаммы (расы) хлебопекарных дрожжей
- •Хлебопекарные свойства некоторых рас и штаммов дрожжей
- •1.1.6. Спиртовое брожение, осуществляемое дрожжами
- •1.2. Молочнокислые бактерии
- •1.2.1. Характеристика молочнокислых бактерий, используемых в хлебопекарном производстве
- •1.2.2. Гомоферментативное молочнокислое брожение
- •1.2.3. Гетероферментативное молочнокислое брожение
- •1.3. Пропионовокислые бактерии
- •1.4. Бифидобактерии
- •2 Глюкоза
- •Контрольные вопросы
- •2. Дрожжи – биологические агенты брожения теста
- •2.1. Разновидности хлебопекарных дрожжей
- •2.1.1. Прессованные дрожжи
- •2.1.2. Сушеные дрожжи
- •Показатели качества сушеных дрожжей
- •2.1.3. Дрожжевое молоко
- •2.1.4. Осмотолерантные дрожжи
- •2.1.5. Дрожжи полусушеные замороженные
- •2.1.6. Дрожжи, чувствительные к холоду
- •2.1.7. Дрожжи, устойчивые к пропионату кальция
- •2.1.8. Дрожжи для готовых смесей (премиксов)
- •2.1.9. Жидкие дрожжи
- •Биохимические и технологические свойства новых селекционированных штаммов дрожжей
- •2.2. Посторонняя микрофлора дрожжей
- •2.2.1. Дикие дрожжи
- •2.2.2. Бактерии
- •Контрольные вопросы
- •3. Закваски, применяемые для приготовления хлебобулочных изделий из пшеничного и ржаного теста
- •3.1. Пшеничная мезофильная и дрожжевая закваски
- •3.2. Пропионовокислая закваска
- •3.3. Комплексная закваска
- •3.4. Ацидофильная закваска
- •3.5. Витаминная закваска
- •3.6. Эргостериновая закваска
- •3.7. Закваски для ржаного теста
- •Видовой и штаммовый состав сухого лактобактерина
- •Контрольные вопросы
- •4. Микробиологические и биохимические процессы, происходящие в тесте
- •Подготовка сырья þ замес теста þ брожение þ разделка и расстойка теста þ выпечка изделий þ охлаждение и хранение изделий.
- •Контрольные вопросы
- •5. Микрофлора зерна и муки
- •5.1. Микрофлора зерна
- •5.2. Микрофлора муки
- •6. Микробная порча хлебобулочных изделий
- •6.1. «Картофельная болезнь» хлеба
- •6.1.1. Причины заболевания хлеба
- •6.1.2. Методы диагностики «картофельной» болезни хлеба
- •6.1.3. Меры предупреждения «картофельной» болезни хлеба
- •Ампула с культурой l. Fermentum пробирка с 10–15 см3 солодового сусла колба с 250 см 3 солодового сусла колба с 1000 см3 солодового сусла.
- •6.2. Плесневение хлеба
- •6.3. «Меловая» болезнь хлеба
- •6.4. «Красная» болезнь хлеба
- •Контрольные вопросы
- •7. Микробиологический и санитарный контроль хлебопекарного производства
- •7.1. Контроль сырья и полуфабрикатов
- •Зависимость степени поражения хлеба «картофельной» болезнью от протеолитической активности спорообразующих бактерий
- •7.2. Контроль прессованных дрожжей
- •7.3. Контроль теста
- •7.4. Контроль готовой продукции
- •Степень контаминации хлеба картофельной палочкой
- •8. Микробиология кондитерского производства
- •8.1. Микрофлора сырья и полуфабрикатов
- •8.2. Микрофлора готовых кондитерских изделий
- •8.3. Санитарно-микробиологический контроль производства кондитерских изделий
- •Микробиологические показатели качества кондитерских изделий
- •Контрольные вопросы
- •9. Микробиология макаронного производства
- •Подготовка сырья þ приготовление макаронного теста þ þ прессование теста þ разделка сырых изделий þ сушка изделий þ þ охлаждение высушенных изделий þ упаковка готовых изделий.
- •9.1. Микробиологическая порча макаронных изделий
- •9.2. Микробиологический контроль макаронного производства
- •Контрольные вопросы
- •10. Способы предотвращения микробной порчи хлебобулочных, кондитерских и макаронных изделий
- •10.1. Изменение содержания свободной воды в мучных изделиях
- •Содержание и активность воды в пищевых продуктах
- •Активность воды и рост микроорганизмов в пищевых продуктах
- •10.2. Применение консервантов
- •Контрольные вопросы
- •Заключение
- •Список Рекомендуемой литературы
- •Содержание
- •Микробиологические процессы при производстве хлеба, кондитерских и макаронных изделий
Хлебопекарные свойства некоторых рас и штаммов дрожжей
|
Показатель, мин |
Т-7 |
К-21 |
О-14 |
Л-1 |
616 |
ЛВ-7 |
5 |
|
Зимазная активность |
55 |
60 |
45 |
45 |
55 |
45 |
85 |
|
Мальтазная активность |
160 |
100 |
95 |
110 |
67 |
120 |
95 |
|
Осмочувстви- тельность |
12 |
10 |
10 |
18 |
5–10 |
6–10 |
15 |
Среди дрожжей вида Saccharomyces minor в хлебопечении используют штаммы 12/17, 7 и «Чернореченский».
Штамм 12/17. Клетки овальной формы размером (2,9–3,0) (4,0–4,2) мкм. Штамм имеет подъемную силу (по шарику) 19–21 мин, выдерживает кислотность до 14 град.
Штамм 7. Клетки мелкие круглые или слегка овальные размером 2,62,2 мкм. Подъемная сила – 17–19 мин, может размножаться при кислотности до 16 град.
Штамм «Чернореченский». Клетки овально-округлой формы размером 3,8–3,2 мкм. Подъемная сила 19–20 мин. Штамм способен размножаться при кислотности среды 16–18 град.
1.1.6. Спиртовое брожение, осуществляемое дрожжами
Размножение дрожжей в тесте происходит в анаэробных условиях, в результате чего они получают энергию за счет спиртового брожения. Образующийся при этом брожении диоксид углерода разрыхляет тесто.
Процесс спиртового брожения суммарно можно выразить следующим уравнением:
С6Н12О6 + 2 Фн + 2 АДФ → 2 СО2 + 2 С2Н5ОН +2 АТФ + 2 Н2О
глюкоза диоксид этанол
углерода
Спиртовое брожение протекает по фруктозодифосфатному пути (гликолитический путь Эмбдена–Мейергофа–Парнаса) (рис. 1.5).
Первая реакция процесса брожения – фосфорилирование глюкозы при участии АТФ с образованием глюкозо-6-фосфата. Затем молекула глюкозо-6-фосфата изомеризуется в молекулу фруктозо-6-фосфата, которая, в свою очередь, фосфорилируется в положении 1. Образовавшийся при этом фруктозо-1,6-дифосфат расщепляется под действием фермента альдолазы (ключевого фермента гликолитического пути) на две триозы – диоксиацетонфосфат и 3-фосфоглицери-новый альдегид (3-ФГА). Диоксиацетонфосфат превращается в 3-ФГА в результате реакции, катализируемой триозофосфатизомеразой. На этом заканчивается первая стадия гликолитического пути, характеризующаяся активированием одной молекулы глюкозы с затратой энергии в виде двух молекул АТФ. На второй стадии брожения происходит окисление 3-ФГА до 1,3-дифосфоглицериновой кислоты при участии НАД-зависимой 3-фосфоглицеральдегиддегидрогеназы. Далее 1,3-дифосфоглицериновая кислота взаимодействует с АДФ, отдавая фосфатную группу, что приводит к синтезу АТФ. На этом этапе имеет место первое субстратное фосфорилирование, т. е. высвобождение энергии и запасание ее в виде АТФ. В следующей реакции гликолиза фосфатная группа 3-фосфоглицериновой кислоты переносится из третьего положения во второе.
Затем происходит реакция дегидратации 2-фосфоглицериновой кислоты, катализируемая ферментом енолазой, приводящая к образованию фосфоенолпирувата. От молекулы фосфоенолпирувата фосфатная группа переносится на АДФ с помощью фермента пируваткиназы, что приводит к образованию АТФ и пирувата. Это вторая реакция субстратного фосфорилирования.
Таким образом, в результате гликолиза из одного моля глюкозы образуются два моля пирувата, от которого с помощью фермента пируватдекарбоксилазы – ключевого фермента спиртового брожения – отщепляется диоксид углерода. Образовавшийся при этом ацетальдегид становится акцептором водорода окисляемого субстрата и восстанавливается до этанола с участием НАД+-зависимой алкогольдегидрогеназы. Биологическое значение последней реакции заключается в окислении восстановленного НАДН+Н+, образовавшегося ранее в ходе реакции превращения 3-фосфоглицеринового альдегида в 1,3-ди-фосфоглицериновую кислоту. Данный путь включает как использование АТФ, так и образование АТФ, давая чистый выход 2 моля АТФ на каждый моль сбраживаемой глюкозы.
К. Нойберг обнаружил, что в зависимости от условий при спиртовом брожении могут образовываться нехарактерные для этого процесса продукты. Так, если к дрожжам, сбраживающим глюкозу, добавить бисульфит (NaHSO3), то последний образует комплекс с ацетальдегидом, в связи с чем он больше не может выполнять роль акцептора электронов. Вследствие этого электроны от восстановленного НАДН передаются на диоксиацетонфосфат. Он восстанавливается до глицерол-3-фосфата и дефосфорилируется с образованием глицерина, как это показано на схеме (см. рис. 1.5). Это модифицированное брожение называют глицериновой формой спиртового брожения.
ГЛЮКОЗА
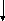 АТФ
АТФ
1 АДФ
Глюкозо-6-фосфат
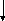 2
2
Фруктозо-6-фосфат
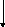 АТФ
АТФ
3 АДФ
Фруктозо-1,6-дифосфат
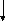
4
 Диоксиацетонфосфат
Глицеральдегид-3-фосфат
Диоксиацетонфосфат
Глицеральдегид-3-фосфат

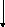
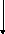 5
6
5
6
13 НАДН+Н+ НАД+
НАД+ + Фн НАДН+Н+
Глицерол-3-фосфат 1,3-дифосфоглицериновая
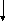 14
кислота
14
кислота
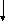 7
АДФ
7
АДФ
ГЛИЦЕРИН + Фн АТФ
3-фосфоглицериновая кислота
 8
8
2- фосфоглицериновая кислота
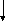 9
– Н2О
9
– Н2О
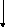 Фосфоенолпируват
Фосфоенолпируват
АДФ
10 АТФ
Пируват
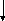
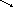
11 СО2
Ацетальдегид
 12
НАДН+Н+
12
НАДН+Н+
НАД+
ЭТАНОЛ
Рис. 1.5. Ферменты, участвующие в осуществлении спиртового брожения (Шлегель, 1987):
1 – гексокиназа; 2 – глюкозофосфатизомераза; 3 – фосфофруктокиназа; 4 – фрукто-
зо-1,6-дифосфат-альдолаза; 5 – триозофосфатизомераза; 6 – 3-фосфоглицеральдегид-дегидрогеназа; 7 – фосфоглицераткиназа; 8 – фосфоглицеромутаза; 9 – енолаза; 10 – пируваткиназа; 11 – пируватдекарбоксилаза; 12 – алкогольдегидрогеназа; 13 – глицерол-3-фосфатдегидрогеназа; 14 – глицеролфосфатаза
Сбраживание глюкозы до этанола и СО2 обычно происходит в слабокислой среде (рН 3–6). Если спиртовое брожение проводить в щелочной среде (например, в присутствии NaHCO3), то также происходит накопление глицерина. Это объясняется тем, что ацетальдегид в щелочных условиях не может являться акцептором водорода окисляемого субстрата, поскольку участвует в реакции дисмутации с образованием этанола и уксусной кислоты. Поэтому акцептором электронов, как и в предыдущем случае, служит диоксиацетонфосфат. Процесс брожения в щелочной среде называют смешанной формой спиртового брожения, которую можно представить в виде уравнения
2 С6Н12О6 → 2 С3Н8О3 + С2Н5ОН + СН3СООН + 2 СО2
глюкоза глицерин этанол уксусная диоксид
кислота углерода
На интенсивность спиртового брожения влияет ряд факторов: температура и влажность теста; наличие витаминов и минеральных веществ, необходимых для нормальной жизнедеятельности дрожжей; бродильная активность дрожжей; состав рецептуры; интенсивность замеса теста; присутствие в тесте улучшителей (ферментных препаратов).
При изучении спиртового брожения Л. Пастер открыл, что в условиях свободного доступа кислорода воздуха брожение подавляется и активируется дыхание. Это явление получило название эффекта Пастера. Эффект Пастера объясняется взаимодействием различных энергетических путей, существующих у дрожжей, а именно, конкуренцией за АДФ между процессами субстратного фосфорилирования гликолитического пути и окислительного фосфорилирования в дыхательной цепи.
