
Травматология и ортопедия. В трёх томах. Шапошников Ю.Г. / Травматология и ортопедия. Руководство для врачей. Том 1. Шапошников Ю.Г
..pdf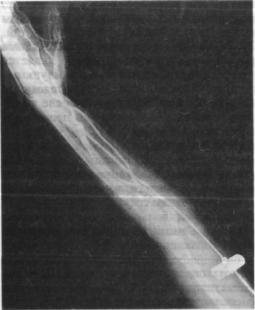
Рис. 5.1. Чрескожная пун кция правой плечевой ар терии. Игла установлена в антеградном направлении.
няют тепло на периферические отделы конечности, используют иглы
икатетеры небольшого диаметра, щадящие способы ангиографии периферических сосудов, по возможности без применения металли ческих проводников. Обязательно наблюдение за состоянием боль ного и кровообращением в сосудах конечности в момент исследования
ив течение 3—4 сут после него. После удаления иглы или катетера из сосуда обязательно рукой прижимают артерию в течение 15— 30 мин до прекращения артериального кровотечения. На место пун кции артерии накладывают стерильный ватно-марлевый давящий валик, больному назначают строгий постельный режим на 24 ч. После бинтования валика проверяют пульс на дистальной части конечности: он должен быть отчетливым.
Для предупреждения тромбоза артерии после открытой пункции или катетеризации на образовавшуюся рану периферического сосуда накладывают новый сосудистый шов. Он отличается от традицион ного шва через три слоя стенки тем, что его накладывают с про шиванием двух слоев: наружного и среднего, внутренний — инти му — не прошивают. При затягивании шва края внутреннего слоя сближают до соприкосновения и восстанавливают естественную скользящую поверхность интимы. Шовный материал не проникает в просвет сосуда. В послеоперационном периоде явлений сосудистой недостаточности в исследованной конечности не наблюдается. При повторной ангиографии этой области обнаруживают хорошую про ходимость и отсутствие деформации периферической артерии в месте наложения сосудистого шва. Важным моментом в профилактике
124
осложнений является строгое соблюдение асептики в кабинете ан гиографии. Проведение постоянной профилактики позволяет избе жать тяжелых осложнений и значительно снизить частоту легких (до 1,87%), в связи с чем'ангиография является вполне безопасным исследованием.
Ангиография при травме. Такое исследование проводили в ос новном у пострадавших с тяжелой травмой. Выявленные у обсле дованных больных повреждения отнесены, согласно классификации, предложенной А. В. Каштаном и О. Н. Марковой (1975), к открытым переломам III—IV, реже ИБ и ИВ степени тяжести. Возраст паци ентов — от 2 до 70 лет. Исследование проводили в разные сроки: в 1—2-е сутки, в течение 5 лет и более с момента травмы, пре имущественно при осложненном течении переломов.
Симптомы острой недостаточности кровообращения в конечности выявлены у 4,3% больных с переломами, у 9,3% с повреждениями мягких тканей. У остальных обследованных проявления острой со судистой недостаточности в момент травмы не определялись или маскировались тяжелым течением перелома.
При ангиографии окклюзия магистральных артерий обнаружена у 81,26% обследованных, стеноз — у 2,64%, окклюзия глубоких вен без повреждения артерий — у 14,6%. Таким образом, магист ральные сосуды в травмированном сегменте были повреждены у 98,5% пострадавших.
Клинико-ангиографические сопоставления показали, что основ ной причиной повреждения магистральных артерий и вен была тяжелая травма (у 65,3% обследованных), на втором месте — спицы фиксирующих аппаратов (у 12,5%), причем на голени, при пере ломах которой спицевые аппараты применяли чаще, чем при по вреждениях других областей, спицевые повреждения артерий диаг ностированы у 18,05% обследованных. Третье место среди причин повреждений занимал тромбоз артерий (рис. 5.2) (9,6%), затем следовали вскрытие гнойников (5,7%), перевязка артерий при кро вотечении (3,8%), спицы скелетного вытяжения (1,9%), гипсовая повязка (0,9%).
Тромбозы магистральных артерий поврежденного сегмента ха рактеризовались множественностью и большой протяженностью. Так, тромбоз одной артерии выявлен у 49,8%, двух — у 38,9%, всех артерий — у 7,8%, ветвей первого порядка — у 3,5% больных (рис. 5.3). У 2/з больных протяженность артериальных окклюзии составляла 7 см и более. При повреждении всех артерий сегмента конечность сохраняли лишь в тех случаях, когда протяженность артериальных окклюзии равнялась 1—2, редко — 3 см (рис. 5.4) при условии развития наиболее экономичных внутриартериальных коллатералей (6,9%). У большинства (84,7%) больных функцио нировали менее экономичные межартериальные коллатерали, что приводило к развитию симптома заместительного кровотока — сим птома «обкрадывания» (рис. 5.5). Клинико-ангиографические сопо ставления показали их функциональную недостаточность. Матема тическая обработка полученных данных статистически достоверно
125

Рис 5.2. Лнгиограмма правой голени, артериальная фаза. Окклюзия передней и задней большеберцовых артерий. Громбоз передней большеберцовой артерии при полной окклюзии сопровождающих ее глубоких вен.'
Рис. 5.3. Ангиограмма правой голени, артермальная фаза. Окклюзия передней большеберцовой и малоберцовой артерий. Большая протяженность окклюзии, мало коллатералей.
показала, что частота окклюзии при травме зависела от тяжести повреждений и не коррелировала с их характером (мягкотканные, костные, открытые, закрытые). Частота артериальных окклюзии и функция коллатералей также зависели от области повреждения (плечо, предплечье, кисть, бедро, голень, стопа).
Обширные тромбозы артерий в поврежденном сегменте, как пра вило, сопровождались «содружественной» окклюзией одноименных глубоких вен на том же или большем протяжении. Глубокие вены часто тромбировались выше уровня травмы, поверхностные вены — на уров не повреждения и Рубцовых изменений кожи. Емкость артериального и венозного русла уменьшалась в общей сложности на 36—48,2%, т. е. развивалась хроническая посттравматическая артериовенозная недостаточность кровоснабжения поврежденного сегмента.
У 14,6% больных были обнаружены окклюзии только глубоких вен на уровне травмы и проксимально от нее, а также поверхностных вен; артериальные окклюзии у них не выявлены. У этих больных
126

Рис 5.4. Ангиограмма ле вой стопы. Окклюзия всех артерий голени. Дефект наполнения размером око ло 3 см в задней большеберцовой артерии в нижней трети голени с развитием внутриартериальных коллатералей, через которые стопа и снабжается кровью.
Рис 5.5. Ангиограмма пра вой кисти, артериальная фаза. Окклюзия лучевой артерии. Кровоснабжение кисти через одну локтевую артерию с «обкрадывани ем» кровотока в ее естест венном регионе (III—IV пальцы).

Ри. 5.6. Ангиограмма лево го плеча,артериальная фа за. Сохранена проходи мость плечевой артерии. Тромбоз глубокой плечевой вены.
возникла хроническая посттравматическая венозная недостаточность (рис. 5.6). При сопоставлении частоты окклюзии в артериальной и венозной сети при артериовенозной и венозной недостаточности статистически достоверно установлено, что венозные окклюзии пре обладали. Следовательно, даже при артериовенозной посттравмати ческой недостаточности артериальный приток был больше, чем ве нозный отток, т. е. редуцированное кровообращение в поврежденном сегменте не развивалось. Известно, что редуцированное кровообра щение создает наилучшие условия для кровотока в поврежденных тканях [Кунцевич В. В., 1979], но для его развития необходимо равновесие между притоком и оттоком крови. Такое равновесие отсутствует у больных с хронической посттравматической артерио венозной и венозной недостаточностью, вследствие чего у них воз никает венозная гипертензия, образуются артериовенозные шунты, развивается венозный застой, замедляется артериальный кровоток, слабо функционируют коллатерали. Все эти нарушения отчетливо видны на ангиограммах.
Помимо обширных окклюзии в венозной сети, нарушение оттока крови от дистальных отделов конечности после травмы вызывают образовавшиеся посттравматические рубцовые ткани и повреждения
128
периферических нервов. Установлено, что трофические функции периферических нервов осуществляются через кровеносную систему. При их повреждении резко замедляется венозный отток в зоне иннервации, ухудшается функция коллатералей, не контрастируются мышечные артериальные ветви, замедляется осевой кровоток по магистральной артерии. В связи с этим своевременное наложение шва на поврежденный периферический нерв будет способствовать улучшению венозного оттока и кровоснабжения конечности (вос становление трофической функции).
Нами совместно с Н. П. Ивановой, Л. А. Болховитиновой и С. В. Седовой (1984, 1986, 1989) было установлено влияние несво бодной кожной пластики и стебля Филатова на кровоснабжение конечности. Ангиографиюпроводили до и после операции. После удаления обширных рубцов с подлежащими измененными тканями и замещения их полнослойным несвободным лоскутом кожи улуч шался венозный отток, скорость артериального кровотока увеличи валась в 2—2,5 раза, начинали функционировать новые коллатерали. Часто без дополнительных операций восстанавливалась функция пальцев у больных с электроожогом, срастались несросшиеся пере ломы, ликвидировались лимфостаз и трофические язвы.
Наблюдение за динамикой сосудистых изменений в процессе сращения переломов показало, что в острый период травмы (до 1 мес) преобладали изменения в венозной сети. В течение 1-го года по сравнению с острым периодом травмы увеличивалось количество окклюзии магистральных артерий и сопровождающих их глубоких вен. К 2 годам отмечалось ухудшение микроциркуляции в зоне несросшегося перелома, увеличивалось количество изолированных окклюзии глубоких вен. Через 3—4 года статистически достоверного увеличения частоты ангиографических симптомов не выявлено. Спу стя 5 лет и более вновь увеличилось количество окклюзии глубоких вен. Аналогичная динамика сосудистых изменений выявлена при проведении повторных операций: каждая новая операция ухудшала сосудистый статус. Таким образом, установлено, что скрытые, не распознанные и нелеченые сосудистые повреждения, сопровождаю щие открытые переломы III, ПБ и ИВ степени тяжести, прогрес сируют. Лечение их необходимо проводить одновременно с восста новлением целости кости и функции конечности.
i Следствием ишемии верхней конечности и электроожогов явля ются выраженные изменения сосудов: окклюзии артерий и вен на большом протяжении со слабым развитием коллатерального крово тока, обширными участками плохо снабжаемых кровью тканей, артериовенозным сбросом крови проксимально от Рубцовых тканей (рис. 5.7). Результаты исследований показали, что лечение данной группы больных необходимо начинать с выполнения операций, улуч шающих кровообращение, — иссечения рубцов и тканей, плохо снабжаемых кровью (клинически — рубцы и участки индурации кожи, подкожной жировой клетчатки), с пластикой дефекта несво бодным кожным лоскутом или свободным кожно-мышечным транс плантатом на сосудистой ножке.
П92 |
129 |

Рис. 5.7. Ангиограмма правой кисти предплечья, артериальная фаза. Последствия электроожога. Окклюзия лучевой и локтевой артерии на большом протяжении со слабым развитием коллатералей.
Повреждения мягких тканей предплечья часто приводят к тя желым неврогенным деформациям кисти. На ангиограммах окклюзия сосудов предплечья выявляется у 92,5%, рубцовая деформация — у 7,5% обследованных. Повреждение локтевого нерва на предплечье сопровождается окклюзией одноименной или двух артерий в 90% случаев, а срединного — в 60%. В зоне поврежденного нерва на обширных участках снижено кровоснабжение, что является одной из причин его замедленного восстановления после наложения шва (рис. 5.8). В связи с этим срединный нерв восстанавливается лучше, чем локтевой. Одновременное восстановление целости артерий, нер вов и сухожилий предплечья в остром периоде травмы приводит к полному восстановлению функции кисти в короткие сроки. Эта операция патогенетически обоснована, и ее нужно проводить в
130

Рис. 5.8. Лнгиограмма правого предплечья. Окклюзия локтевой артерии на всем протяжении после ранения мягких тканей предплечья и повреждения локтевого нерва.
полном объеме сразу после травмы с использованием микрохирур гической техники.
При тяжелой травме кисти повреждаются ладонные дуги, общие и собственные артерии пальцев, сосуды предплечья и соответству ющие вены. Основной симптом этих повреждений — окклюзия. На основании данных, полученных при ангиографии, разработан способ оценки кровоснабжения каждого пальца и кисти по состоянию кро вотока в двух областях: собственно пальцев и пясти-предплечье. Клинико-ангиографические сопоставления показали, что от состоя ния кровоснабжения зависят не только жизнеспособность кисти и пальцев в момент травмы, но и восстановление их функций в процессе лечения. На основании этих данных разработаны показания к перемещению пальца при операции полицизации, способ прогно зирования восстановления подвижности пальцев и определения оче редности выполнения восстановительных операций.
Перед микрохирургическими операциями ангиографию проводят с целью оценки состояния сосудов реципиентной и донорской об ластей. В случае отсутствия у больного общих клинических проти вопоказаний результаты ангиографии являются основанием для при-
5* |
131 |

Рис. 5.9. Исследование донорской и реципиентной зон перед микрохирургическими операциями.
а — ангиограмма левого плеча (реципиентная область); б — ангиограмма правой голени (донорская область).
нятия решения о пересадке аутотрансплантата на сосудистой ножке с разработкой конкретного плана операции — «свободы выбора» реципиентных сосудов, места наложения анастомоза, способа обра зования новой сосудистой связи, необходимости использования аутовенозной вставки и др. Данные, полученные при ангиографии, в основном подтверждались на операции [Гришин И. Г., 1985]. Пра вильная предоперационная оценка состояния сосудов реципиентной и донорской областей — непременное условие снижения частоты осложнений в момент операции и в послеоперационном периоде (рис. 5.9).
Ятрогенные повреждения сосудов — не редкость. На ангиограммах их обнаруживают после оперативных вмешательств — форми рования трансплантата из малоберцовой кости, алкоголизации ро стковых зон, введения лекарств в пупочную артерию у новорож денных, длительной внутрисосудистой катетерной терапии инфек ционных осложнений, ангиографии, удаления опухолей. Анализ клинико-ангиографической картины позволяет расценивать указан ные тромбозы как следствие длительного спазма артерии. Спазм артерий легко возникает вследствие неадекватного растяжения со судистого пучка во время его выделения или смещения крючками во время операции, спицами фиксирующих аппаратов, при нару шении техники выполнения внутриартериальных исследований и
вмешательств, неадекватных действий в случаях внутриартериального введения лекарств.
Для предотвращения сосудистого спазма, а следовательно, и сосудистых тромбозов рекомендуются проведение паравазальной бло кады магистральных сосудов выше того уровня, на котором произ водят вмешательство, внутриартериальное введение растворов но вокаина, тримекаина, папаверина, но-шпы при обнаружении спазма магистральной артерии во время операции. Необходимо проводить периартериальную анестезию магистрального сосуда перед его пе ревязкой для предупреждения стеноза и тромбоза конца перевязан ного сосуда. При исследовании сосудов ампутационной культи ко нечности, на которой имеются трофические язвы, обнаруживают тромбоз или стеноз конца перевязанного сосуда на протяжении 10—15 см с уменьшением кровоснабжения тканей культи и слабой компенсацией кровотока за счет редких артериальных ветвей от расположенной выше проходимости части магистральной артерии. Аналогичные изменения на том же уровне происходят и в соответ ствующих магистральных венах.
Новорожденным перед введением лекарств в артерию и по окон чании его, помимо выполнения периартериальной анестезии, необ ходимо вводить раствор новокаина или тримекаина внутриартериально в соответствующих дозах. Все растворы подогревают до 37°С и вводят медленно. Те же правила необходимо соблюдать при ис пользовании катетера для длительных внутриартериальных влива ний. Перечисленные мероприятия позволяют предотвратить возник новение длительного сегментарного спазма магистральных артерий, вен, а в последующем их тромбоза.
Сосудистые изменения при патологической функциональной перестройке костной ткани. При болезни Пертеса и асептическом некрозе головки бедренной кости у детей измерение диаметра пяти артерий, снабжающих кровью тазобедренный сустав на поврежден ной и неповрежденной сторонах, позволило установить статистиче ски достоверное уменьшение диаметра каждой из них и суммарного сосудистого бассейна на стороне поражения тазобедренного сустава по сравнению с показателями, полученными при исследовании не поврежденной стороны, т. е. наличие гипоплазии артериального рус ла. В отличие от болезни Пертеса при асептическом некрозе гипо плазия усугублялась нарушением формирования сосудистого русла в виде развития редких анатомических вариантов. Атипичные со судистые варианты наблюдались лишь на стороне поражения. Ги поплазия артерий, как правило, сочетается с гипоплазией сопро вождающих их глубоких вен, в результате чего формируется врож денная артериовенозная недостаточность кровоснабжения данного региона. При асептическом некрозе головки бедренной кости еще один фактор вызывает нарушение кровоснабжения тазобедренного сустава — это положение Лоренца I при вправлении головки, когда она сдавливает бедренные сосуды. Таким образом, результаты ан гиографии подтвердили наличие гипоплазии региональной сосуди стой сети тазобедренного сустава на стороне поражения. Признаки
