
- •Стереохимия аминокислот.
- •Биосинтез жирных кислот
- •3.Ферменты
- •Образование аммиака, роль глутамина и аспарагина
- •Рацематы
- •Бэта-окисление жирных кислот
- •Общ хар. Сахаров, тригалозный сахар
- •Мажорные-минорные осн, пуриновые-пиримидиновые
- •Оксидоредуктазы
- •Таутомерные превращения азотистых оснований
- •Гликозиды. Написать формулу метил-альфа-d-глюкозогликозид
- •Кардиолипин; хар-ка
- •Кинетика ферментативных процессов;уравнение михаэлис-Мэнтен
- •Цикл глюкоза в лактат и сколько нужно и затратить атф
- •МРнк, строение и роль
- •Арахидоновая к-та и ее производные
- •Изомеразы; общая хар-ка,примеры реакций
- •Как влияет концентрац... Уравнение Михаэлиса–Ментен
- •Дыхательная цепь
- •Сахароза, как влияет её строение на хим св-ва; может ли она восстонавливать аммиачный р-р Ag
- •Высшие Жирные кислоты ; числа омыления,йодное число и кислотное тное число.
- •Важнейшие коферменты над и надф.
- •Биосинтез белка
- •Мутаротация
- •Желчные кислоты
- •Трансферазы
- •Коферменты фмн и фад
- •Цикл трикарбоновых кислот (Цикл Кребса)
- •Коферменты
- •Биосинтез рнк
- •Жирные кислоты: структура и свойства, связи
- •Гликоген,целлюлоза, амилопектин.
- •Пируват, аспартат- фермент
- •ТРнк, биороль
- •Механизм действия стероидных гормонов.
- •Изоферменты
- •Цикл пировиноградной кислоты.
- •Основные свойства генетического кода
- •Таутомерия глюкозы и что такоемутаротация
- •3.Специфические ферменты
- •5.Гликолиз
- •6. Рилизинг-факторы (либерины)
- •Факторы, влияющие на скорость ферм.Реакции
- •Биосинтез триглицерина и глицеролфосфолипидов
- •3.Нуклеотиды.
- •4. Горм.Гипофиза
- •1. Отличия и сходста днк и рнк
- •3 Роль тиреоидных гормонов
- •Цикл мочевины.
- •Гормоны поджелудочной железы
- •Гетерогликаны
- •4) Классы ферментов
- •5) Аллостерическая активность ферментов
- •Гормоны гипоталамуса
- •Кортикотропин-рилизинг-гормон
- •Специфичность ферментов
- •5.Жирные кислоты (алифатические кислоты)
- •Фолдинг белка
- •1.Стерины и стериды
- •2. Нуклеозиды и нуклеотиды
- •Метаболизим белков, липидов и углеводов.
- •Адреналин и норадреналин
- •1. Днк: типы, характеристика
- •2. Воски
- •3.Распад гликогена. Гликоген
- •Роль в организме
- •2.Аминосахара и их значение
- •5)Трансаминирование аминокислот
- •6.Отличие спиртового от молочно-кислого брожения
- •1.Методы очисткии разделения белков и пептидов,
- •2) Сахароза и её инверсия.
- •3) Глицерофосфолипиды.
- •4)Первичная структура нуклеиновых кислот
- •Пуриновые основания
- •2)Цереброзиды
- •3.Первичная и вторичная структура белков (связи)
- •4. Гомогликаны (строение, функции)
- •5) Пиридоксин, его роль в регуляции белкового обмена, переаминирование(механизм р-ии и роль в метаболизме)
- •1.Пиримидиновые азотистые основания
- •2.Плазмалогены.
- •3. Способы образования аминокислот
- •4. Пути метаболизма
- •1)Строение матричной рнк.
- •2. Гормоны,как производныеАмк,гормональный цикл
- •3.Кислотно-основные свойства Аминокислот.
- •5) Регуляция активности ферментов
- •6.Пентозофосфатный путь окисления
- •1.Моносахариды.
- •2) Пептиды
- •3)Сфинголипиды.
- •4.Гликолиз и гликогенолиз.
- •1. Общие пути обмена аминокислот.
- •2. Транскри́пция
- •3.Альфа – Аминокислоты.
- •Связь между окислением жиров и циклом Кребса.
- •1. Структурная организация фермента
- •2. Регуляторные центры
- •Гормоны пептидной природы
- •Гликогенез и его рольСинтез гликогена (гликогенез)
- •Жирные кислоты
- •1.Гликофосфолипиды.
- •Гликозиды,кислоты, аминосахара как производные монасахаридов.
- •Мембранно-опосредованное взаимодействие гормонов.
- •Катаболизм аминокислот.
- •Распад стеариновой кислоты.
- •138 Молекул атф
- •Стеролы и стероиды.
- •Биосинтез пуриновых нуклеотидов.
- •ЦАмф, свойства.
- •Гидролазы.
- •Типы ингибирования. Константа Михаэлиса.
- •Свободное окисление.
- •Качественные реакции на гомо- и гетероциклические аминокислоты.
- •3) Физические и химические свойства крахмала, целлюлозы,гликогена
Биосинтез белка
Биосинтез белка — сложный многостадийный процесс синтеза полипептидной цепи из аминокислотных остатков, происходящий на рибосомах клеток живых организмов с участием молекул мРНК и тРНК. Биосинтез белка можно разделить на стадии транскрипции, процессинга и трансляции.
Транскрипция: происходит считывание генетической информации, зашифрованной в молекулах ДНК, и запись этой информации в молекулы мРНК.
Процессинг: между транскрипцией и трансляцией молекула мРНК претерпевает ряд последовательных изменений, которые обеспечивают созревание функционирующей матрицы для синтеза полипептидной цепочки. К 5΄-концу присоединяется кэп, а к 3΄-концу поли-А хвост, который увеличивает длительность жизни мРНК; в ходе ряда стадий процессинга из мРНК удаляются некоторые фрагменты, ненужные в последующих стадиях, и происходит редактирование нуклеотидных последовательностей.
Трансляция: заключается в синтезе полипептидной цепи в соответствии с информацией, закодированной в матричной РНК. Аминокислотная последовательность выстраивается при помощи тРНК, которые образуют с аминокислотами комплексы — аминоацил-тРНК. Каждой аминокислоте соответствует своя тРНК, имеющая соответствующий антикодон, «подходящий» к кодону мРНК. Во время трансляции рибосома движется вдоль мРНК, по мере этого наращивается полипептидная цепь.
Готовая белковая молекула затем отщепляется от рибосомы и транспортируется в нужное место клетки. Энергией биосинтез белка обеспечивается за счёт АТФ.
Билет 7
Мутаротация
МУТАРОТАЦИЯ - самопроизвольное изменение величины оптич. вращения свежеприготовленных р-ров оптически активных соединений. Характерна для моносахаридов, восстанавливающих олигосахаридов, лактонов и др. Катализируется к-тами и основаниями.
В случае глюкозы мутаротация объясняется установлением равновесия:
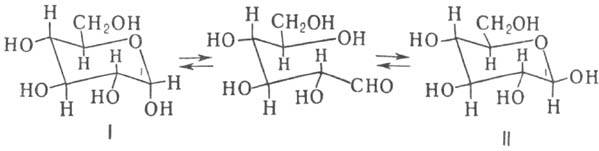
В равновесном состоянии присутствует 38 % aльфа-формы и 62 % бета-формы. Промежуточная альдегидная форма содержится в ничтожно малой концентрации.
Желчные кислоты
ЖК-монокарбоновые гидроксикислоты из класса стероидов; производные холановой кислоты, отличающиеся тем, что к её кольцевой структуре присоединены гидроксильные группы.
 Наиб.
распространены ее моно-, ди- и
тригидроксизамещенные, содержащие 24
атома
С; известны также ди-, три- и
тетрагидроксизамещенные желчные к-ты,
содержащие 27 и 28 атомов
С. Положение заместителей, расположенных
под или над плоскостью мол-лы,
обозначают соотв. буквами a
и b.
Желчные к-ты
- кристаллы;
плохо раств. в воде.
Образование желчных к-т
происходит в печени
нек-рых птиц, млекопитающих и человека
из холестерина.
Биосинтез
желчных к-т
из холестерина
включает след.р-ции: гидроксилирование
по атомамуглерода
колец В и С, инверсию
3b-
в 3a-гидроксигруппу,
восстановлениедвойной
связи
при атоме
С-5 с получением цис-сочленения колец А
и В, окислит. отщепление изопропильной
группы в боковой цепи с обр-нием
карбоксильной при атоме
С-24.
Желчные к-ты
содержатся в желчи
в виде щелочных солей
т. наз. конъюгатов - соединений желчных
к-т
с таурином или глицином.
Так, для холевой к-ты конъюгаты -
гликохолевая к-та и таурохолевая к-та.
Натриевые соли
желчных к-т
- хорошие эмульгаторы;
эмульгируя жиры,
они способствуют их всасыванию и
перевариванию. Важную роль при этом
играют растворимыеримые комплексы
дезоксихолевой к-ты с жирами
и жирными к-тами (холеиновые к-ты). Желчные
к-ты
получают щелочным гидролизом
твердого в-ва желчи.
На основе прир. желчных к-т
осуществлен синтез разл. гидрокси- и
оксопроизводных холановой к-ты. Так,
дегидратация
холевой к-ты при нагр. в вакууме
или при действии ZnCl2
в ацетоне
приводит к апохолевой к-те, из к-рой м.
б. получены холеиновые к-ты. Желчные
к-ты
применяют для синтеза кортикостероидов
и в медицине в качестве лек. препаратов,
растворяющих и предотвращающих обр-ние
желчных камней .
Наиб.
распространены ее моно-, ди- и
тригидроксизамещенные, содержащие 24
атома
С; известны также ди-, три- и
тетрагидроксизамещенные желчные к-ты,
содержащие 27 и 28 атомов
С. Положение заместителей, расположенных
под или над плоскостью мол-лы,
обозначают соотв. буквами a
и b.
Желчные к-ты
- кристаллы;
плохо раств. в воде.
Образование желчных к-т
происходит в печени
нек-рых птиц, млекопитающих и человека
из холестерина.
Биосинтез
желчных к-т
из холестерина
включает след.р-ции: гидроксилирование
по атомамуглерода
колец В и С, инверсию
3b-
в 3a-гидроксигруппу,
восстановлениедвойной
связи
при атоме
С-5 с получением цис-сочленения колец А
и В, окислит. отщепление изопропильной
группы в боковой цепи с обр-нием
карбоксильной при атоме
С-24.
Желчные к-ты
содержатся в желчи
в виде щелочных солей
т. наз. конъюгатов - соединений желчных
к-т
с таурином или глицином.
Так, для холевой к-ты конъюгаты -
гликохолевая к-та и таурохолевая к-та.
Натриевые соли
желчных к-т
- хорошие эмульгаторы;
эмульгируя жиры,
они способствуют их всасыванию и
перевариванию. Важную роль при этом
играют растворимыеримые комплексы
дезоксихолевой к-ты с жирами
и жирными к-тами (холеиновые к-ты). Желчные
к-ты
получают щелочным гидролизом
твердого в-ва желчи.
На основе прир. желчных к-т
осуществлен синтез разл. гидрокси- и
оксопроизводных холановой к-ты. Так,
дегидратация
холевой к-ты при нагр. в вакууме
или при действии ZnCl2
в ацетоне
приводит к апохолевой к-те, из к-рой м.
б. получены холеиновые к-ты. Желчные
к-ты
применяют для синтеза кортикостероидов
и в медицине в качестве лек. препаратов,
растворяющих и предотвращающих обр-ние
желчных камней .
