
- •Стереохимия аминокислот.
- •Биосинтез жирных кислот
- •3.Ферменты
- •Образование аммиака, роль глутамина и аспарагина
- •Рацематы
- •Бэта-окисление жирных кислот
- •Общ хар. Сахаров, тригалозный сахар
- •Мажорные-минорные осн, пуриновые-пиримидиновые
- •Оксидоредуктазы
- •Таутомерные превращения азотистых оснований
- •Гликозиды. Написать формулу метил-альфа-d-глюкозогликозид
- •Кардиолипин; хар-ка
- •Кинетика ферментативных процессов;уравнение михаэлис-Мэнтен
- •Цикл глюкоза в лактат и сколько нужно и затратить атф
- •МРнк, строение и роль
- •Арахидоновая к-та и ее производные
- •Изомеразы; общая хар-ка,примеры реакций
- •Как влияет концентрац... Уравнение Михаэлиса–Ментен
- •Дыхательная цепь
- •Сахароза, как влияет её строение на хим св-ва; может ли она восстонавливать аммиачный р-р Ag
- •Высшие Жирные кислоты ; числа омыления,йодное число и кислотное тное число.
- •Важнейшие коферменты над и надф.
- •Биосинтез белка
- •Мутаротация
- •Желчные кислоты
- •Трансферазы
- •Коферменты фмн и фад
- •Цикл трикарбоновых кислот (Цикл Кребса)
- •Коферменты
- •Биосинтез рнк
- •Жирные кислоты: структура и свойства, связи
- •Гликоген,целлюлоза, амилопектин.
- •Пируват, аспартат- фермент
- •ТРнк, биороль
- •Механизм действия стероидных гормонов.
- •Изоферменты
- •Цикл пировиноградной кислоты.
- •Основные свойства генетического кода
- •Таутомерия глюкозы и что такоемутаротация
- •3.Специфические ферменты
- •5.Гликолиз
- •6. Рилизинг-факторы (либерины)
- •Факторы, влияющие на скорость ферм.Реакции
- •Биосинтез триглицерина и глицеролфосфолипидов
- •3.Нуклеотиды.
- •4. Горм.Гипофиза
- •1. Отличия и сходста днк и рнк
- •3 Роль тиреоидных гормонов
- •Цикл мочевины.
- •Гормоны поджелудочной железы
- •Гетерогликаны
- •4) Классы ферментов
- •5) Аллостерическая активность ферментов
- •Гормоны гипоталамуса
- •Кортикотропин-рилизинг-гормон
- •Специфичность ферментов
- •5.Жирные кислоты (алифатические кислоты)
- •Фолдинг белка
- •1.Стерины и стериды
- •2. Нуклеозиды и нуклеотиды
- •Метаболизим белков, липидов и углеводов.
- •Адреналин и норадреналин
- •1. Днк: типы, характеристика
- •2. Воски
- •3.Распад гликогена. Гликоген
- •Роль в организме
- •2.Аминосахара и их значение
- •5)Трансаминирование аминокислот
- •6.Отличие спиртового от молочно-кислого брожения
- •1.Методы очисткии разделения белков и пептидов,
- •2) Сахароза и её инверсия.
- •3) Глицерофосфолипиды.
- •4)Первичная структура нуклеиновых кислот
- •Пуриновые основания
- •2)Цереброзиды
- •3.Первичная и вторичная структура белков (связи)
- •4. Гомогликаны (строение, функции)
- •5) Пиридоксин, его роль в регуляции белкового обмена, переаминирование(механизм р-ии и роль в метаболизме)
- •1.Пиримидиновые азотистые основания
- •2.Плазмалогены.
- •3. Способы образования аминокислот
- •4. Пути метаболизма
- •1)Строение матричной рнк.
- •2. Гормоны,как производныеАмк,гормональный цикл
- •3.Кислотно-основные свойства Аминокислот.
- •5) Регуляция активности ферментов
- •6.Пентозофосфатный путь окисления
- •1.Моносахариды.
- •2) Пептиды
- •3)Сфинголипиды.
- •4.Гликолиз и гликогенолиз.
- •1. Общие пути обмена аминокислот.
- •2. Транскри́пция
- •3.Альфа – Аминокислоты.
- •Связь между окислением жиров и циклом Кребса.
- •1. Структурная организация фермента
- •2. Регуляторные центры
- •Гормоны пептидной природы
- •Гликогенез и его рольСинтез гликогена (гликогенез)
- •Жирные кислоты
- •1.Гликофосфолипиды.
- •Гликозиды,кислоты, аминосахара как производные монасахаридов.
- •Мембранно-опосредованное взаимодействие гормонов.
- •Катаболизм аминокислот.
- •Распад стеариновой кислоты.
- •138 Молекул атф
- •Стеролы и стероиды.
- •Биосинтез пуриновых нуклеотидов.
- •ЦАмф, свойства.
- •Гидролазы.
- •Типы ингибирования. Константа Михаэлиса.
- •Свободное окисление.
- •Качественные реакции на гомо- и гетероциклические аминокислоты.
- •3) Физические и химические свойства крахмала, целлюлозы,гликогена
1.Пиримидиновые азотистые основания
Азо́тистые основа́ния — гетероциклические органические соединения, производные пиримидина и пурина, входящие в состав нуклеиновых кислот. Для сокращенного обозначения пользуются большими латинскими буквами. К азотистым основаниям относят аденин (A), гуанин (G), цитозин (C), которые входят в состав как ДНК, так и РНК. Тимин (T) входит в состав только ДНК, а урацил (U) встречается только в РНК.
Пиримидиновые основания – производные пиримидина, входящие в состав нуклеиновых кислот: урацил, тимин, цитозин. Для оснований, содержащих группу –ОН, характерно подвижное равновесие структурных изомеров, обусловленное переносом протона от кислорода к азоту и наоборот:
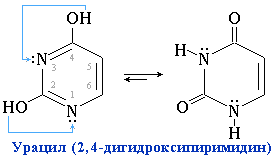
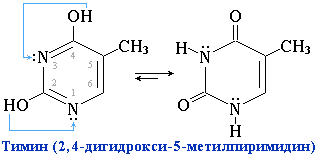

Подобное динамическое равновесие структурных изомеров называют "таутомерией".
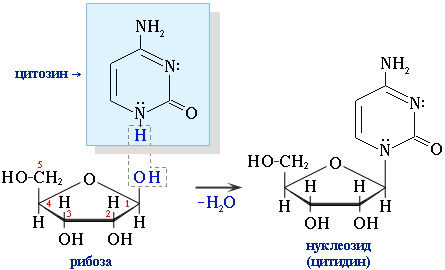
Пиримидиновые основания входят в состав нуклеозидов — структурных компонентов нуклеиновых кислот. Нуклеозиды образуются за счет отщепления водорода от N–H-связи в молекуле азотистого основания и гидроксила при С1 в молекуле углевода рибозы (или 2-дезоксирибозы).Здесь проявляются нуклеофильные свойства амина (группа :N–H в азотистом гетероцикле) и способность к нуклеофильному замещению полуацетальногогидрокисила (при С1) в молекуле углевода.
2.Плазмалогены.
ПЛАЗМАЛОГЕНЫ (альдегидогенные липиды), фосфолипиды общей ф-лы цис-RCH=CHOCH2CH (OR') CH2 —OP(O)(OH)OX, где R-обычно алкил или алкенил, содержащий 14 или 16 атомов С; R'-ацил насыщенной или ненасыщенной к-ты с 16-24 атомами С в цепи; X = H (фосфатидалевая к-та), (фосфатидаль-холин), X = CH2CH2NH3 (фосфатидальэтаноламин), X = CH2CH(COOH)NH3 (фосфатидальсерин) и др.
Плазмалогены широко распространены в природе; встречаются во всех клетках животных и в отдельных видах растений. В больших кол-вах плазмалогены содержатся в спинном и головном мозге, сердечной мышце и плазме крови. Могут накапливаться в тканях при нек-рых патологич. состояниях, напр. при ишемии сердечной мышцы.
В условиях кислотного катализа плазмалогены гидролизуются с образованием RCH2CHO. При щелочном гидролизе плазмалогенов образуются жирные к-ты и соответствующие лизоплазма-логены (в общей ф-ле R' = H). Плазмалогены расщепляются фосфолипазами A2, С и D, как правило, с меньшей скоростью, чем диацилфосфолипиды (в сердечной мышце идентифицирована специфич. фосфолипаза A2, гидролизующая плазмалогены с большей скоростью, чем диацилфосфолипиды). Алкенильно-эфирная связь плазмалогенов расщепляется плазмалогеназами с образованием RCH2CHO и лизоплазмалогена (ОН при C-1 остатка глицерина).Обнаружено, что генетич. дефект в синтезе плазмалогенов приводит к церебральным нарушениям (синдром Целлвегера). Плазмалогены участвуют в клеточном обмене полиненасыщ. жирных к-т, в первую очередь арахидоновой, выполняя ф-ции промежут. депо, через к-рые к-ты транспортируются к мембранным диацилфосфолипидам. Поведение плазмалогенов в модельных мембранах сходно с поведением диацилфосфолипидов, хотя и обнаружены нек-рые различия в структурной организации, формировании фаз, динамич. поведении.
Осн. путь биосинтеза плазмалогенов-дегидрирование алкилацилфос-фолипидов.
