
- •В.Н. Захарченко Курс физической химии Москва
- •Часть 2. Электрохимические системы и электрохимические процессы
- •Глава 1. Термодинамика гальванического элемента
- •1.1.Гальванический элемент
- •1.2.Термодинамика гальванического элемента
- •1.3.Электродный потенциал. Электродные реакции
- •Глава 2.Основные типы электродов
- •2.1.Классификация электродов
- •2.2.Электроды 1-го рода
- •2.3.Электроды 2-го рода
- •2.4.Окислительно-восстановительные электроды
- •2.5.Газовые электроды
- •2.6.Ионоселективные электроды
- •Глава 3.Ионы в растворах электролитов
- •3.1.Классическая теория электролитической диссоциации
- •3.2.Взаимодействие растворяемого вещества с растворителем
- •3.3.Межионное взаимодействие в растворах
- •Глава 4.Термодинамика растворов электролитов
- •4.1.Формальные представления об активности ионов в растворах электролитов
- •4.2.Экспериментальные данные по коэффициентам активности
- •Глава 5.Явления переноса в растворах электролитов
- •5.1.Диффузия в растворах электролитов
- •5.2.Диффузионный потенциал
- •5.3.Электрическая проводимость растворов электролитов
- •Глава 6.Электрохимическая поляризация
- •6.1.Эдс поляризации и электродная поляризация
- •6.2.Теории электродной поляризации
- •Аллотропические цепи
- •Концентрационные цепи
- •7.3.Химические электрохимические цепи
- •Простые химические цепи
- •Сложные химические цепи
- •Глава 8.Химические источники тока
- •8.1.Эталонные гальванические элементы
- •8.2.Первичные гальванические элементы
- •Элемент Лекланше
- •Ртутнооксидный элемент
- •Индийсодержащие элементы
- •Элементы с твердыми электролитами
- •Резервные элементы
- •8.3.Вторичные гальванические элементы
- •Свинцовый аккумулятор
- •Щелочной аккумулятор
- •Серебряный аккумулятор
- •Часть 3. Химическая кинетика и катализ
- •Глава 9.Формальная кинетика
- •9.1.Основные понятия
- •9.2.Классификация химических реакций по их кинетике
- •9.3.Необратимая реакция первого порядка
- •9.4.Необратимая реакция второго порядка
- •9.5.Два случая бимолекулярной реакции
- •2A Продукты реакции,
- •9.6.Необратимая реакция n-ого порядка
- •9.7.Методы определения порядка реакции
- •Дифференцирование кинетической кривой
- •Глава 10.Кинетика сложных реакций
- •10.1.Параллельные реакции
- •10.2.Обратимая реакция
- •Последовательные реакции
- •Глава 11.Влияние температуры на скорость химических реакций
- •11.1.Эмпирические закономерности влияния температуры на скорость реакций
- •11.2.Уравнение Аррениуса
- •Глава 12.Элементарные акты химических превращений
- •12.1.Теория активных столкновений
- •12.2.Механизм мономолекулярных реакций по теории активных столкновений (схема Линдемана)
- •12.3.Теория переходного состояния (теория активного комплекса)
- •Глава 13.Химическая индукция
- •Глава 14.Фотохимические процессы
- •14.1.Основные законы фотохимии
- •14.2.Механизм фотохимических реакций
- •Глава 15.Цепные реакции
- •15.1.Общие сведения о цепных реакциях
- •15.2.Зарождение цепи и методы обнаружения свободных радикалов
- •15.3.Развитие и обрыв цепи
- •Глава 16.Катализ
- •16.1.Общие сведения
- •16.2.Гомогенный катализ
- •16.3.Кислотно-основной катализ
- •16.4.Ферментативный катализ
- •16.5.Гетерогенный катализ
- •Предметный указатель
- •Оглавление
- •Часть 3. Химическая кинетика и катализ 78
- •Глава 9. Формальная кинетика 79
Глава 2.Основные типы электродов
2.1.Классификация электродов
Различают три основных класса электродов:
электроды с активным электродным материалом, то есть непосредственно входящим в суммарное уравнение электродной реакции,
электроды с инертным электродным материалом, на поверхности которых протекает электродная реакция и которые не входят в уравнение этой реакции,
ионоселективные электроды, представляющие собой мембраны, на поверхности которых происходит скачок потенциала.
К электродам с активным электродным материалом относятся электроды 1-го и 2-го рода, а к электродам с инертным электродным материалом относятся простые и сложные окислительно-восстановительные электроды, или редокс-электроды, и газовые электроды.
Из ионоселективных электродов важнейшим является стеклянный электрод.
2.2.Электроды 1-го рода
Электрод первого рода состоит из активного металла, погруженного в ненасыщенный раствор соли этого металла.
Обозначим металл M, а катионы, образующиеся при растворении его соли, - Mz+.
С учетом этих обозначений электродную реакцию можно записать следующим образом:
Mz+ + ze = M.
Условная запись электрода принимает следующий вид:
Mz+M.
Уравнение для электродного потенциала записывается так:
![]() (2
- 1)
(2
- 1)
К электродам 1-го рода относятся медный электрод Cu2+Cu, цинковый электрод Zn2+Zn, серебряный электрод Ag+Ag и др.
Эту группу электродов объединяет то, что их потенциал зависит от активности катиона. Название этой группы - электроды, обратимые по катиону.
Однако к числу электродов 1-го рода относится немногочисленная группа электродов, потенциал которых определяется активностью аниона (их называют электродами, обратимыми по аниону). Наиболее изученными из них являются селеновый электрод и теллуровый электрод, который характеризуется следующим:
2Te
+ 2e
=
![]() −,
−,
Te,
![]() .
.
2.3.Электроды 2-го рода
Электроды 2-го рода содержат металл и труднорастворимое соединение этого металла, контактирующие с раствором, содержащим анионы, входящие в состав труднорастворимого соединения.
В зависимости от типа труднорастворимого соединения металла различают металлогалогенидные электроды, содержащие труднорастворимые галогениды металлов, металлосульфатные, содержащие труднорастворимые сульфаты металлов, и др.
Общая запись электродной реакции для электродов 2-го рода такова:
MxAz +xze = xM + zAx. (а)
Приведенная выше запись результирующей электродной реакции соответствует двум ее основным стадиям:
растворению труднорастворимой соли
MxAz = xMz+ + zAx,
восстановлению ионов металла на катоде
xMz+ + xze = M.
Таким образом, по механизму катодного процесса электроды 2-го рода принципиально не отличаются от электродов 1-го рода.
Отвечающая суммарной реакции (а) условная запись электрода 2-го рода имеет следующий вид:
Ax−Mz+ , M .
Этой же реакции соответствует выражение для электродного потенциала:
![]() (2
- 2)
(2
- 2)
Потенциал электродов 2-го рода зависит от активности анионов. Поэтому их часто называют электродами, обратимыми по анионам.
Электроды
2-го рода широко применяются при проведении
электрохимических измерений. Кроме
того, данные по их стандартным электродным
потенциалам используются для расчета
произведения растворимости PS
труднорастворимых солей. С этой целью
сравнивают стандартный потенциал
электрода 2-го рода
![]() со стандартным потенциалом электрода
1-го рода с соответствующим металлом
со стандартным потенциалом электрода
1-го рода с соответствующим металлом
![]() .
Так как в системе, содержащей
труднорастворимую соль MxAz,
устанавливается равновесие
.
Так как в системе, содержащей
труднорастворимую соль MxAz,
устанавливается равновесие
MxAz = xMz+ + zAx,
характеризуемое константой равновесия
![]() ,
,
то
стандартным условиям для электрода
2-го рода (![]() )
отвечает активность ионов металла,
равная
)
отвечает активность ионов металла,
равная
![]() .
Таким образом, выполняется условие:
.
Таким образом, выполняется условие:
![]() ,
,
из которого следует:
![]() .
(2 - 3)
.
(2 - 3)
Изучение наиболее известных электродов 2-го рода начнем с класса металлогалогенидных, из которых наиболее распространена группа металлохлоридных электродов.
Каломельный электрод. Его название дано по труднорастворимому хлориду ртути (I) - каломели Hg2Cl2.
Каломельный электрод характеризуют:
электродная реакция:
Hg2Cl2 + 2e = 2Hg + 2Cl,
условная запись:
ClHg2Cl2, Hg,
выражение для электродного потенциала:
![]()
Для изготовления каломельного электрода каломель перетирают с раствором хлорида калия и несколькими каплями ртути до получения однородной пасты, которую наслаивают на поверхность ртути, помещаемой в стеклянную емкость. Сверху на пасту наслаивают раствор хлорида калия. Металлический контакт осуществляют платиновой проволокой, которую впаивают в стекло (платина и лабораторное стекло имеют близкие значения термического коэффициента расширения).
Каломельный электрод отличается прекрасной воспроизводимостью электродного потенциала и очень высокой устойчивостью. Известно, что при хранении свыше 25 лет каломельного электрода не было замечено никакого изменения его электродного потенциала. В связи с этим он широко применялся в качестве практического электрода сравнения. Было предложено использовать следующие типы каломельного электрода:
децинормальный каломельный электрод, заполняемый 0,1 н. раствором KCl (электродный потенциал такого электрода по отношению к стандартному электроду сравнения при 25С равен 0,3365 В),
нормальный каломельный электрод, заполняемый 1 н. раствором KCl (его электродный потенциал по отношению к стандартному электроду сравнения при 25С равен 0,2828 В),
насыщенный каломельный электрод, заполняемый насыщенным раствором KCl (потенциал при 25С равен 0,2438 В).
Наиболее употребительным является насыщенный каломельный электрод. Однако по сравнению с другими типами каломельных электродов у него наибольшая зависимость электродного потенциала от температуры.
Трудности миниатюризации каломельного электрода и работа с ртутью привели к тому, что он повсеместно заменялся серебряногалогенидными электродами.
Серебрянохлоридный электрод является наиболее распространенным представителем группы серебряногалогенидных электродов.
Приводим электродную реакцию, условную запись и выражение для электродного потенциала серебрянохлоридного электрода:
AgCl + e = Ag + Cl,
Cl−AgCl, Ag,
![]()
Серебрянохлоридный электрод подобно каломельному электроду имеет хорошую воспроизводимость и устойчивость электродного потенциала. Он широко применяется в качестве практического электрода сравнения (иногда такие электроды называют вспомогательными) не только в водных средах, но и в водных растворах спиртов, кетонов и эфиров.
Для получения серебрянохлоридного электрода тонкую серебряную проволоку покрывают слоем хлорида серебра. С этой целью ее погружают в водный раствор, содержащий хлорид-ионы, и пропускают электрический ток, используя серебряную проволоку в качестве анода. Погруженная в раствор KCl серебряная проволока с электролитическим покрытием AgCl представляет собой готовый электрод сравнения.
Миниатюрные серебрянохлоридные электроды используются в физиологических и биохимических исследованиях.
Ртутносульфатный электрод является представителем группы металлосульфатных электродов с наиболее устойчивым электродным потенциалом и наиболее высокой воспроизводимостью.
Характеристики этого электрода приводятся ниже:
Hg2SO4 + 2e = 2Hg + SO42,
SO42Hg2SO4, Hg,
![]()
Металлооксидные электроды. В этих электродах анионом, содержащимся в водной среде, служит гидроксид-ион. Частную реакцию на этих электродах можно представить как двухстадийный процесс:
M2Oz + zH2O + 2ze = [2M(OH)z + 2ze]= 2M + 2zOH.
Электродной реакции соответствует следующая форма условной записи электрода:
OHM2Oz, M.
Выражение для электродного потенциала металлооксидного электрода имеет следующий вид:
![]() .
(2 - 4)
.
(2 - 4)
Оно может быть преобразовано с использованием ионного произведения воды
![]()
следующим образом:
![]()
Обозначив
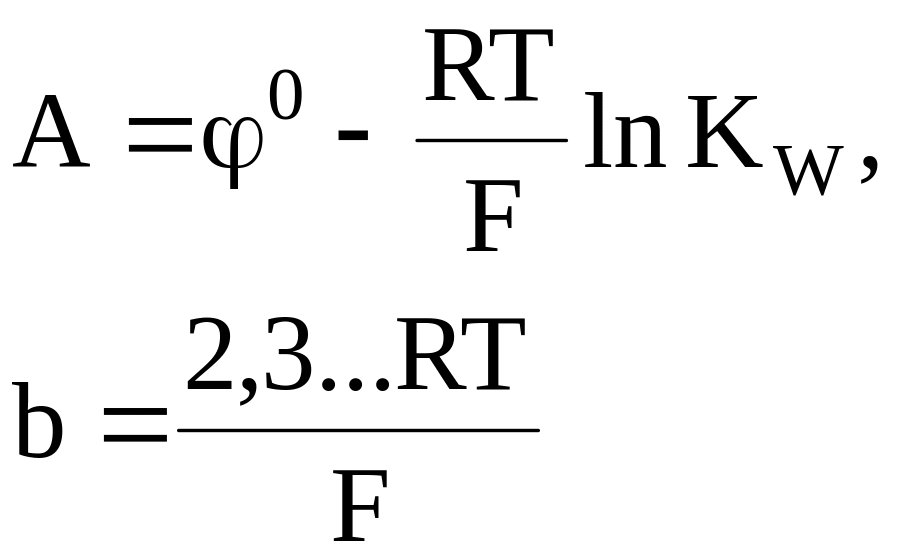
и принимая во внимание, что десятичный логарифм активности водородных ионов представляет собой водородный показатель среды pH, получим
= A - bpH.
Входящий в уравнение коэффициент b называется электрохимическим коэффициентом. При 25С он равен 0,059157 В.
Линейная зависимость между водородным показателем среды и потенциалом металлооксидного электрода предполагает его применение для измерений рН. Такая возможность действительно существует. Однако в кислой среде происходит растворение оксидов и электрод перестает функционировать как рН-метрический.
Примерами металлооксидных электродов могут служить ртутнооксидный и сурьмянооксидный электроды.
Ртутнооксидный электрод характеризуется следующим:
HgO + H2O + 2e = Hg + 2OH,
OH HgO, Hg,
а сурьмянооксидный электрод может быть описан электродной реакцией и условной записью в таком виде:
Sb2O3 + 3H2O + 6e = 2Sb + 6OH,
OH Sb2O3, Sb.
Для изготовления сурьмянооксидного электрода достаточно заполнить стеклянную трубку расплавленной сурьмой и окислить выступающую поверхность сурьмы нагреванием на воздухе.
Электроды на основе металлических сплавов и растворов. Они представляют собой разновидность электродов 1-го и 2-го рода, в которых вместо чистого металла в кристаллической форме используются металлические сплавы или растворы. Многие металлы хорошо растворяются в ртути с образованием амальгамы. В качестве примера амальгамного электрода можно привести кадмиевый амальгамный электрод:
Cd2+ + 2e = Cd (Hg),
Cd2+ Cd (Hg),
![]()
Обращаем внимание на то, что потенциал металла входит в выражение для электродного потенциала, так как в отличие от обычных электродов 1-го и 2-го рода металл не находится в стандартном состоянии.
