
- •В.Н. Захарченко Курс физической химии Москва
- •Часть 2. Электрохимические системы и электрохимические процессы
- •Глава 1. Термодинамика гальванического элемента
- •1.1.Гальванический элемент
- •1.2.Термодинамика гальванического элемента
- •1.3.Электродный потенциал. Электродные реакции
- •Глава 2.Основные типы электродов
- •2.1.Классификация электродов
- •2.2.Электроды 1-го рода
- •2.3.Электроды 2-го рода
- •2.4.Окислительно-восстановительные электроды
- •2.5.Газовые электроды
- •2.6.Ионоселективные электроды
- •Глава 3.Ионы в растворах электролитов
- •3.1.Классическая теория электролитической диссоциации
- •3.2.Взаимодействие растворяемого вещества с растворителем
- •3.3.Межионное взаимодействие в растворах
- •Глава 4.Термодинамика растворов электролитов
- •4.1.Формальные представления об активности ионов в растворах электролитов
- •4.2.Экспериментальные данные по коэффициентам активности
- •Глава 5.Явления переноса в растворах электролитов
- •5.1.Диффузия в растворах электролитов
- •5.2.Диффузионный потенциал
- •5.3.Электрическая проводимость растворов электролитов
- •Глава 6.Электрохимическая поляризация
- •6.1.Эдс поляризации и электродная поляризация
- •6.2.Теории электродной поляризации
- •Аллотропические цепи
- •Концентрационные цепи
- •7.3.Химические электрохимические цепи
- •Простые химические цепи
- •Сложные химические цепи
- •Глава 8.Химические источники тока
- •8.1.Эталонные гальванические элементы
- •8.2.Первичные гальванические элементы
- •Элемент Лекланше
- •Ртутнооксидный элемент
- •Индийсодержащие элементы
- •Элементы с твердыми электролитами
- •Резервные элементы
- •8.3.Вторичные гальванические элементы
- •Свинцовый аккумулятор
- •Щелочной аккумулятор
- •Серебряный аккумулятор
- •Часть 3. Химическая кинетика и катализ
- •Глава 9.Формальная кинетика
- •9.1.Основные понятия
- •9.2.Классификация химических реакций по их кинетике
- •9.3.Необратимая реакция первого порядка
- •9.4.Необратимая реакция второго порядка
- •9.5.Два случая бимолекулярной реакции
- •2A Продукты реакции,
- •9.6.Необратимая реакция n-ого порядка
- •9.7.Методы определения порядка реакции
- •Дифференцирование кинетической кривой
- •Глава 10.Кинетика сложных реакций
- •10.1.Параллельные реакции
- •10.2.Обратимая реакция
- •Последовательные реакции
- •Глава 11.Влияние температуры на скорость химических реакций
- •11.1.Эмпирические закономерности влияния температуры на скорость реакций
- •11.2.Уравнение Аррениуса
- •Глава 12.Элементарные акты химических превращений
- •12.1.Теория активных столкновений
- •12.2.Механизм мономолекулярных реакций по теории активных столкновений (схема Линдемана)
- •12.3.Теория переходного состояния (теория активного комплекса)
- •Глава 13.Химическая индукция
- •Глава 14.Фотохимические процессы
- •14.1.Основные законы фотохимии
- •14.2.Механизм фотохимических реакций
- •Глава 15.Цепные реакции
- •15.1.Общие сведения о цепных реакциях
- •15.2.Зарождение цепи и методы обнаружения свободных радикалов
- •15.3.Развитие и обрыв цепи
- •Глава 16.Катализ
- •16.1.Общие сведения
- •16.2.Гомогенный катализ
- •16.3.Кислотно-основной катализ
- •16.4.Ферментативный катализ
- •16.5.Гетерогенный катализ
- •Предметный указатель
- •Оглавление
- •Часть 3. Химическая кинетика и катализ 78
- •Глава 9. Формальная кинетика 79
10.2.Обратимая реакция
Рассмотрим систему реакций:
k1
A B. (a)
k−1
Частная реакция
A B (b)
называется прямой реакцией, а частная реакция
A B (с)
называется обратной реакцией.
Скорость исчезновения вещества А по реакции (b) описывается уравнением:
![]() ,
(10 - 10)
,
(10 - 10)
а его накопление по реакции (с) - уравнением:
![]() .
(10 - 11)
.
(10 - 11)
Изменение концентрации вещества А по обеим реакциям в соответствии с принципом независимого протекания реакций составит:
![]() .
(10 - 12)
.
(10 - 12)
Для решения уравнения (10 - 12) введем следующие граничные условия: к началу реакции ( = 0) концентрации веществ А и В соответственно равны a и b. Если к моменту времени концентрация вещества А изменится на –х, то концентрация вещества В в соответствии с условием материального баланса изменится на х. Следовательно,
CA = a – x,
CB = b – x,
и уравнение (10 - 12) принимает следующий вид:
![]() .
(10 - 13)
.
(10 - 13)
После преобразования уравнения (10 - 13) получим:
![]()
и
![]() .
(10 - 14)
.
(10 - 14)
Обозначив
![]() ,
,
с учетом граничных условий (х = 0 при = 0) интегрированием уравнения (13 - 14) получим:
![]() .
(10 - 15)
.
(10 - 15)
Из уравнения (10 - 15) следует, что предельное значение х, соответствующее = , равно константе А, то есть
А = х.
При очень длительном протекании обратимой реакции в системе наступает равновесие. Равновесные концентрации СА, и СВ, зависят от исходных концентраций веществ и констант скоростей:
![]() ;
;
![]() ;
;
![]() ;
(10 - 16)
;
(10 - 16)
![]() .
(10 - 17)
.
(10 - 17)
Рис.
10 - 2.
Кинетические кривые для исходного
вещества и продукта.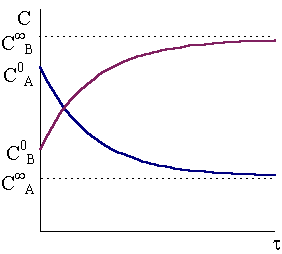
![]() .
(10 - 18)
.
(10 - 18)
Выражение (10 - 18) показывает, что полученные результаты полностью согласуются с представлениями о динамическом характере химического равновесия.
Типичный ход кинетических кривых для исходных веществ и продуктов обратимой реакции первого порядка показан на рис. 10 - 2.
Последовательные реакции
Последовательными реакциями называют реакции, протекающие в несколько стадий. Вещества, образующиеся на каждой стадии и принимающие участие в дальнейшем превращении, называются промежуточными соединениями.
Рассмотрим простейшую схему последовательных реакций:
k1 k2
A B C.
В данной схеме А является исходным веществом, В - промежуточное соединение, С - продукт реакции.
Кинетика расходования исходного вещества описывается обычным уравнением необратимой реакции первого порядка:
. (а)
Кинетика накопления вещества В описывается тем же уравнением (а), которое перепишем в иной форме:
![]() .
(b)
.
(b)
Кинетика расходования вещества В на образование продукта реакции описывается также уравнением необратимой реакции первого порядка:
![]() .
(с)
.
(с)
Общая скорость изменения концентрации промежуточного продукта в соответствии с принципом независимого протекания реакций определяется как алгебраическая разность скоростей реакций (b) и (с):
![]() .
(10 - 19)
.
(10 - 19)
В уравнениях (a), (b) и (с) в качестве переменных используются концентрации веществ А и В. Кроме того, переменной является концентрация продукта реакции. Для удобства записи обозначим концентрации веществ А, В и С соответственно X, Y и Z. Если до начала реакции в системе содержится только вещество А, концентрация которого равна а, то концентрации всех веществ должны быть связаны между собой в соответствии с условием материального баланса:
X + Y + Z = a.
Для еще большего упрощения записи последующих уравнений используем нормированные концентрации:
![]() ,
то есть СА
= ах, СВ
= ay,
CC
= az.
,
то есть СА
= ах, СВ
= ay,
CC
= az.
Нормированная концентрация вещества А изменяется по времени в соответствии с уравнением (9 - 14), которое в данной форме записи принимает вид:
![]() .
(10 - 20)
.
(10 - 20)
Дифференциальное уравнение (10 - 19), описывающее изменение по времени концентрации промежуточного соединения, можно записать так:
![]() .
(10 - 21)
.
(10 - 21)
Уравнение (10 - 21) является неоднородным дифференциальным уравнением первой степени. Первым этапом его решения является решение соответствующего однородного уравнения. В данном случае таким однородным уравнением является:
![]() .
(10 - 22)
.
(10 - 22)
Его решение таково:
![]() .
(10 - 23)
.
(10 - 23)
Возникающая при интегрировании уравнения (10 - 22) величина не является константой, а представляет собой функцию времени , так как это уравнение послужит заменой неоднородного уравнения.
Уравнению (10 - 23) можно придать иную форму:
![]()
или,
обозначив
![]() ,
получим
,
получим
![]() .
(10 - 24)
.
(10 - 24)
Величина А, входящая в уравнение (10 - 24), также зависит от времени . В связи с этим дифференцирование уравнения (10 ‑ 24) дает:
![]() .
(10 - 25)
.
(10 - 25)
Вычитая из уравнения (10 - 25) уравнение (10 - 21) и учитывая, что левый член правой части уравнения (10 - 25) равен −k2y, получим:
![]()
или
![]() .
(10 - 26)
.
(10 - 26)
После интегрирования уравнения (10 - 26) находим зависящую от времени величину А:
![]() .
(10 - 27)
.
(10 - 27)
Ее подстановка в уравнение (10 - 24) приводит к новому уравнению, выражающему зависимость концентрации промежуточного соединения от времени:
![]() .
(10 - 28)
.
(10 - 28)
Для того, чтобы найти постоянную интегрирования, входящую в уравнение (10 - 28), воспользуемся исходными условиями: в начальный момент промежуточное соединение отсутствует ( = 0, y = 0), т.е.
![]() .
.
Окончательный вид уравнения для концентрации промежуточного соединения таков:
![]() .
(10 - 29)
.
(10 - 29)
Концентрацию продукта реакции можно сравнительно легко установить из условия:
z = 1 - (x + y).
Следовательно,
![]()
или
![]() .
(10 - 30)
.
(10 - 30)
Уравнения (10 - 20), (10 - 24) и (10 - 30) позволяют описать кинетические кривые всех трех веществ А, В и С. Однако прежде, чем анализировать ход кинетических кривых, убедимся в правильности полученного результата. С этой целью для проверки воспользуемся уравнением (10 - 30), для которого возьмем два крайних случая:
скорость первой реакции АВ во много раз меньше скорости второй реакции ВС;
скорость второй реакции ВС во много раз меньше скорости первой реакции АВ.
Первому случаю отвечает соотношение констант скоростей k1 << k2, а второму - k2 << k1.
В первом случае выполняются приближения:
![]() ,
,
а во втором случае - приближения:
![]() .
.
С учетом этих приближений уравнение (10 - 30) трансформируется в два однотипных уравнения:
![]() при
k1<<
k2,
при
k1<<
k2,
![]() при
k2<<
k1.
при
k2<<
k1.
Таким образом, получены варианты уравнения (10 - 15), определяющего кинетику необратимой реакции первого порядка по накоплению продукта реакции.
Данный результат находится в полном согласии с постулатом о том, что кинетика реакции в целом определяется самой медленной стадией и показывает правильность полученных уравнений.
Окончательную форму уравнений, описывающих ход кинетических кривых для каждого вещества, получим, перейдя от нормированных концентраций к обычным, то есть с учетом, что СA =ax, CB = ay, CC = az:
![]() ,
(10 - 31)
,
(10 - 31)
![]() ,
(10 - 32)
,
(10 - 32)
Рис.
10 - 3.
Кинетические кривые для реакций
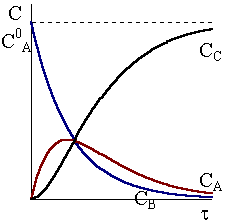
![]() в случае k1k2.
в случае k1k2.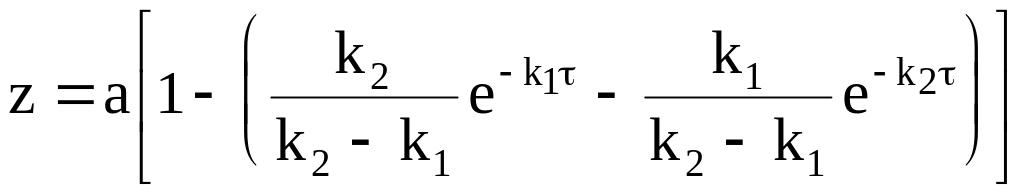 .
(10 - 33)
.
(10 - 33)
Кинетические кривые для последовательных реакций с различным соотношением констант скоростей показаны на рис. 10 ‑ 3, 10 ‑ 4 и 10 - 5.
Максимум
на кинетической кривой CB
= CB()
наступает при условии![]() и в соответствии с уравнением (10 - 21)
в точке максимума выполняется соотношение:
и в соответствии с уравнением (10 - 21)
в точке максимума выполняется соотношение:
Рис.
10 - 5.
Кинетические кривые для реакций
Рис.
10 - 4.
Кинетические кривые для реакций
в случае k1k2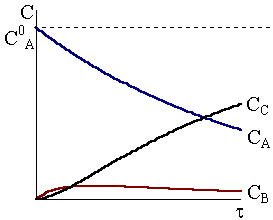
![]() в случае k1<<k2.
в случае k1<<k2.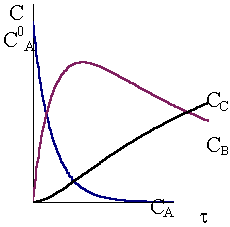
![]() .
(10 - 34)
.
(10 - 34)
Положение максимума на кинетической кривой найдем дифференцированием уравнения (10 - 32):
![]() .
.
После преобразований получим:
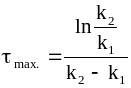 .
(10 -35)
.
(10 -35)
Из формулы (10 - 35) следует, что положение максимума промежуточного соединения не зависит от концентрации исходного вещества, а определяется лишь соотношением между константами скорости.
Соотношение между константами скорости также влияет на форму кинетической кривой промежуточного соединения. При большом отношении k1/k2 концентрация промежуточного соединения очень быстро возрастает, а затем после максимума начинает медленно уменьшаться. Для больших отношений k2/k1 характерен медленный подъем концентрации промежуточного соединения и более размытый максимум.
Если константа реакции превращения промежуточного соединения меньше константы превращения исходного вещества, то всегда можно дождаться такого времени реакции, чтобы выполнялось условие:
![]()
или
![]() .
.
Поэтому разделив уравнение (10 - 32) на уравнение (10 - 31), получим:
![]() .
(10 - 36)
.
(10 - 36)
Наступающее через достаточно длительное время соотношение между концентрациями называется переходным отношением (или переходным равновесием).
Если выполняется более жесткое условие k2>>k1, то соотношение между концентрациями принимает вид:
![]() (10
- 37)
(10
- 37)
или
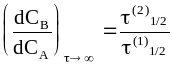 ,
(10 - 38)
,
(10 - 38)
где (1)1/2 и (2)1/2 - соответственно время полупревращения исходного вещества и промежуточного соединения.
Формулы (10 - 37) и (10 - 38) отражают вековое соотношение между концентрациями (или вековое равновесие). Они представляют значительный интерес для выяснения времени полураспада радиоактивных элементов по содержанию в образцах руды элементов, составляющих радиоактивное семейство. Кроме того, аналитическое определение концентраций промежуточных веществ дает возможность оценивать константы скорости отдельных этапов многостадийных реакций.
