
- •В.Н. Захарченко Курс физической химии Москва
- •Часть 2. Электрохимические системы и электрохимические процессы
- •Глава 1. Термодинамика гальванического элемента
- •1.1.Гальванический элемент
- •1.2.Термодинамика гальванического элемента
- •1.3.Электродный потенциал. Электродные реакции
- •Глава 2.Основные типы электродов
- •2.1.Классификация электродов
- •2.2.Электроды 1-го рода
- •2.3.Электроды 2-го рода
- •2.4.Окислительно-восстановительные электроды
- •2.5.Газовые электроды
- •2.6.Ионоселективные электроды
- •Глава 3.Ионы в растворах электролитов
- •3.1.Классическая теория электролитической диссоциации
- •3.2.Взаимодействие растворяемого вещества с растворителем
- •3.3.Межионное взаимодействие в растворах
- •Глава 4.Термодинамика растворов электролитов
- •4.1.Формальные представления об активности ионов в растворах электролитов
- •4.2.Экспериментальные данные по коэффициентам активности
- •Глава 5.Явления переноса в растворах электролитов
- •5.1.Диффузия в растворах электролитов
- •5.2.Диффузионный потенциал
- •5.3.Электрическая проводимость растворов электролитов
- •Глава 6.Электрохимическая поляризация
- •6.1.Эдс поляризации и электродная поляризация
- •6.2.Теории электродной поляризации
- •Аллотропические цепи
- •Концентрационные цепи
- •7.3.Химические электрохимические цепи
- •Простые химические цепи
- •Сложные химические цепи
- •Глава 8.Химические источники тока
- •8.1.Эталонные гальванические элементы
- •8.2.Первичные гальванические элементы
- •Элемент Лекланше
- •Ртутнооксидный элемент
- •Индийсодержащие элементы
- •Элементы с твердыми электролитами
- •Резервные элементы
- •8.3.Вторичные гальванические элементы
- •Свинцовый аккумулятор
- •Щелочной аккумулятор
- •Серебряный аккумулятор
- •Часть 3. Химическая кинетика и катализ
- •Глава 9.Формальная кинетика
- •9.1.Основные понятия
- •9.2.Классификация химических реакций по их кинетике
- •9.3.Необратимая реакция первого порядка
- •9.4.Необратимая реакция второго порядка
- •9.5.Два случая бимолекулярной реакции
- •2A Продукты реакции,
- •9.6.Необратимая реакция n-ого порядка
- •9.7.Методы определения порядка реакции
- •Дифференцирование кинетической кривой
- •Глава 10.Кинетика сложных реакций
- •10.1.Параллельные реакции
- •10.2.Обратимая реакция
- •Последовательные реакции
- •Глава 11.Влияние температуры на скорость химических реакций
- •11.1.Эмпирические закономерности влияния температуры на скорость реакций
- •11.2.Уравнение Аррениуса
- •Глава 12.Элементарные акты химических превращений
- •12.1.Теория активных столкновений
- •12.2.Механизм мономолекулярных реакций по теории активных столкновений (схема Линдемана)
- •12.3.Теория переходного состояния (теория активного комплекса)
- •Глава 13.Химическая индукция
- •Глава 14.Фотохимические процессы
- •14.1.Основные законы фотохимии
- •14.2.Механизм фотохимических реакций
- •Глава 15.Цепные реакции
- •15.1.Общие сведения о цепных реакциях
- •15.2.Зарождение цепи и методы обнаружения свободных радикалов
- •15.3.Развитие и обрыв цепи
- •Глава 16.Катализ
- •16.1.Общие сведения
- •16.2.Гомогенный катализ
- •16.3.Кислотно-основной катализ
- •16.4.Ферментативный катализ
- •16.5.Гетерогенный катализ
- •Предметный указатель
- •Оглавление
- •Часть 3. Химическая кинетика и катализ 78
- •Глава 9. Формальная кинетика 79
Аллотропические цепи
В цепях этого типа источником работы является переход из одной кристаллической формы металла в другую.
Аллотропическую цепь можно записать в следующей форме:
MMz+, Ax−M,
где M и M - кристаллические формы металла.
По данным ЭДС аллотропической цепи можно экспериментально определить термодинамические характеристики перехода
M M.
Так как электрическая работа цепи равна убыли энергии Гиббса - G, то
G = −zFE.
К.В. Захарченко использовал аллотропическую цепь для определения термодинамической активности аморфного кобальта (аморфные металлы образуются при чрезвычайно быстром охлаждении расплавленного металла). Цепь, содержащая один электрод из аморфного кобальта, а другой из кристаллического металла, позволила по данным ЭДС найти термодинамическую активность аморфного кобальта, которая оказалась в зависимости от скорости охлаждения равной от 15 до 27. По температурной зависимости ЭДС, используя уравнение Гиббса - Гельмгольца, были вычислены изменения энтальпии и энтропии при переходе кобальта из кристаллического в аморфное состояние.
Концентрационные цепи
Существует несколько типов концентрационных цепей.
Например, используя в качестве электродов амальгаму кадмия разной концентрации, можно получить цепь
Cd(Hg)Cd2+Cd(Hg),
aCd’ aCd’’
ЭДС которой равна
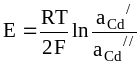 .
.
К подобного рода цепям можно отнести электрохимическую систему, содержащую два водородных электрода с разными давлениями водорода и общим электролитом.
Второго рода цепи представляют одинаковые электродные материалы, погружаемые в растворы одинаковых электролитов, но имеющих разную термодинамическую активность. Эти цепи используются для определения чисел переноса ионов.
7.3.Химические электрохимические цепи
Принято различать простые и сложные химические цепи.
Простые химические цепи
К ним относятся цепи, в которых имеется общий электролит для двух разных электродов.
ЭДС простой химической цепи определяется произведением активностей ионов или давлений газов.
Приведем примеры простых химических цепей.
Цепь, содержащая электрод 1-го рода и электрод 2‑го рода
Такой цепью является элемент, содержащий амальгамный кадмиевый электрод и ртутносульфатный электрод:
Cd(Hg)CdSO4 (насыщенный раствор)Hg2SO4, Hg.
ЭДС этого элемента, называемого элементом Вестона и используемого как эталон ЭДС, выражается следующим уравнением:
![]() .
(7 - 1)
.
(7 - 1)
В последнюю часть уравнения входит средняя активность электролита.
Цепь, содержащая электрод 2-го рода и газовый электрод
В качестве такой цепи рассмотрим элемент, содержащий серебрянохлоридный электрод и водородный электрод:
Ag,AgClHClH2,Pt.
При постоянном давлении водорода ЭДС этой цепи можно выразить уравнением:
![]() .
.
Цепь, содержащая два газовых электрода
Примером такой цепи служит следующая цепь:
Pt, H2 HClCl2, Pt.
Сложные химические цепи
В сложных химических цепях существует граница между двумя растворами электролитов и ЭДС таких цепей определяется отношением активностей ионов.
Классическим примером сложной химической цепи является медно-цинковый элемент, называемый также элементом Якоби - Даниэля:
ZnZn2+Cu2+Cu.
ЭДС этого элемента выражается уравнением:
![]() .
.
