
- •Лекція № 9 оксигеновмісні органічні сполуки
- •Класифікація оксигеновмісних органічних сполук
- •Коротка характеристика групи оксигеновмісних органічних сполук
- •1. Алканоли або спирти, або алкоголі
- •Класифікаця спиртів залежно від числа гідроксильних груп
- •За характером карбонового ланцюга
- •Залежно від положення гідроксильних груп
- •1.1. Одноатомні насичені спирти
- •Міжнародна номенклатура спиртів
- •Ізомерія одноатомних насичених спиртів
- •Властивості одноатомних насичених спиртів Фізичні властивості
- •Хімічні властивості
- •8. Якісні реакції на одноатомні спирти.
- •Добування одноатомних насичених спиртів
- •Застосування одноатомних насичених спиртів
- •1.2. Багатоатомні спирти
- •Фізичні властивості
- •Хімічні властивості
- •Добування багатоатомних спиртів
- •Застосування багатоатомних спиртів
- •2. Феноли
- •Фізичні властивості фенолу.
- •Хімічні властивості фенолу
- •Добування фенолу
- •Застосування фенолу
- •3. Альдегіди
- •Гомологічний ряд альдегідів
- •Міжнародна номенклатура альдегідів
- •Властивості альдегідів Фізичні властивості
- •Хімічні властивості
- •Добування альдегідів
- •Застосування альдегідів і кетонів
- •4. Карбонові кислоти
- •Гомологічний ряд одноосновних насичених карбонових кислот
- •Міжнародна номенклатура карбонових кислот
- •Властивості карбонових кислот Фізичні властивості
- •Хімічні властивості
- •Добування карбонових кислот
- •Застосування карбонових кислот
- •Етери або прості ефіри
- •Застосування етерів
- •6. Естери або складні ефіри
- •Застосування естерів
- •7. Жири. Мило. Смз
- •Склад і будова молекул жирів.
- •Фізичні властивості.
- •Значення жирів
- •Хімічні властивості жирів.
- •Мило. Смз
- •Застосування жирів й їхнього значення.
- •8. Вуглеводи
- •8.1. Моносахариди глюкоза
- •Властивості глюкози Фізичні властивості
- •Хімічні властивості
- •Властивості сахарози Фізичні властивості
- •Хімічні властивості
- •Виробництво цукру та застосування сахарози
- •8.3. Полісахариди
- •Властивості крохмалю та целюлози Фізичні властивості
- •Хімічні властивості крохмалю
- •Хімічні властивості целюлози
- •Добування крохмалю та целюлози
- •Застосування крохмалю та целюлози
- •Порівняльна характеристика оксигенвмісних органічних сполук
Добування карбонових кислот
Карбонові кислоти добувають реакціями окиснення алканів, ацетилену, спиртів, альдегідів.
Застосування карбонових кислот
Мурашину кислоту застосовують як розчинник, у медицині (мурашиний спирт) як відновник. Мурашина кислота застосовується як протрава для фарбування шерсті, консервант фруктових соків і силосу, використовується для дезінфекції місткостей у харчовій промисловості, у хімічних синтезах.
Оцтову кислоту у вигляді 6 – 9 % розчину, як оцет – приправа до їжі, для консервації овочів.
Оцтова кислота застосовується для добування пластмас, кіноплівки; в хімічних синтезах; як розчинник; для виробництва ацетатного волокна, синтезу барвників, ліків (аспірин), виробництва пестицидів.
Естери карбонових кислот, як пахучі речовини в косметиці та кондитерській галузі (запахи квітів, овочів, фруктів, прянощів тощо). Солі оцтової кислоти використовують для фарбування тканин, а також для боротьби зі шкідниками сільського господарства.
Етери або прості ефіри
Етерами називаються органічні сполуки, молекули яких складаються з двох вуглеводневих радикалів, пов’язаних з атомом Оксигену R1–О–R2. Етери або прості ефіри – це продукт взаємодії двох спиртів. Загальна формула етерів або простих ефірів
R1–О–R2 , функціональна група –О–
Реакція одержання етерів називається реакцією етерифікації:
R1 – OH + НО – R2 R1 – O – R2+ H2O
Спирт 1 Спирт2 Етер або простий ефір
C2H5 – OH + НО – CH3 C2H5 – O – CH3+ H2O
Етанол Метанол Етилметиловий етер
Міжнародна номенклатура етерів або простих ефірів
Назви етерів утворюються за назвами радикалів з додаванням слова ~ етер або слів ~ простий ефір. Прикладом може служити діетиловий етер С2Н5 – О – С2Н5.
ВЛАСТИВОСТІ ЕТЕРІВ
Фізичні властивості
Більшість всіх етерів – рідини, майже нерозчинні у воді.
Низькомолекулярні етери – леткі речовини нейтрального характеру з характерним запахом. Високомолекулярні ефіри – тверді кристалічні речовини. Етери погано розчинні у воді, мають меншу густину, ніж вода, добре розчинні в органічних розчинниках і самі розчиняють багато органічних сполук.
15
Хімічні властивості
Етери стійкі до дії лугів і лужних металів. Ця властивість дозволяє використовувати їх в якості розчинників. Прості ефіри легко окислюються навіть киснем повітря, утворюючи вибухонебезпечні пероксиди і гідропероксиди. Це слід враховувати при одержанні, зберіганні і застосуванні етерів.
Основною хімічною властивістю етерів є реакція гідролізу (обернена до реакції етерифікації):
R1
– O – R2+
H2O
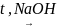 R1
– OH
+ R2
– ОН
R1
– OH
+ R2
– ОН
Етер або простий ефір Спирт 1 Спирт2
C2H5 – O – CH3 + H2O C2H5 – OH + CH3 – ОН
Етилметиловий етер Етанол Метанол
