
- •Лекція № 9 оксигеновмісні органічні сполуки
- •Класифікація оксигеновмісних органічних сполук
- •Коротка характеристика групи оксигеновмісних органічних сполук
- •1. Алканоли або спирти, або алкоголі
- •Класифікаця спиртів залежно від числа гідроксильних груп
- •За характером карбонового ланцюга
- •Залежно від положення гідроксильних груп
- •1.1. Одноатомні насичені спирти
- •Міжнародна номенклатура спиртів
- •Ізомерія одноатомних насичених спиртів
- •Властивості одноатомних насичених спиртів Фізичні властивості
- •Хімічні властивості
- •8. Якісні реакції на одноатомні спирти.
- •Добування одноатомних насичених спиртів
- •Застосування одноатомних насичених спиртів
- •1.2. Багатоатомні спирти
- •Фізичні властивості
- •Хімічні властивості
- •Добування багатоатомних спиртів
- •Застосування багатоатомних спиртів
- •2. Феноли
- •Фізичні властивості фенолу.
- •Хімічні властивості фенолу
- •Добування фенолу
- •Застосування фенолу
- •3. Альдегіди
- •Гомологічний ряд альдегідів
- •Міжнародна номенклатура альдегідів
- •Властивості альдегідів Фізичні властивості
- •Хімічні властивості
- •Добування альдегідів
- •Застосування альдегідів і кетонів
- •4. Карбонові кислоти
- •Гомологічний ряд одноосновних насичених карбонових кислот
- •Міжнародна номенклатура карбонових кислот
- •Властивості карбонових кислот Фізичні властивості
- •Хімічні властивості
- •Добування карбонових кислот
- •Застосування карбонових кислот
- •Етери або прості ефіри
- •Застосування етерів
- •6. Естери або складні ефіри
- •Застосування естерів
- •7. Жири. Мило. Смз
- •Склад і будова молекул жирів.
- •Фізичні властивості.
- •Значення жирів
- •Хімічні властивості жирів.
- •Мило. Смз
- •Застосування жирів й їхнього значення.
- •8. Вуглеводи
- •8.1. Моносахариди глюкоза
- •Властивості глюкози Фізичні властивості
- •Хімічні властивості
- •Властивості сахарози Фізичні властивості
- •Хімічні властивості
- •Виробництво цукру та застосування сахарози
- •8.3. Полісахариди
- •Властивості крохмалю та целюлози Фізичні властивості
- •Хімічні властивості крохмалю
- •Хімічні властивості целюлози
- •Добування крохмалю та целюлози
- •Застосування крохмалю та целюлози
- •Порівняльна характеристика оксигенвмісних органічних сполук
8. Вуглеводи
Вуглеводи — це органічні сполуки, що мають загальну формулу:
Cn (H2О)m
Вуглеводи поділяються на моносахариди, дисахариди, полісахариди. Ди- і полісахариди гідролізуються з утворенням моносахаридів. Моносахариди не можуть гідролізуватися з утворенням найпростіших вуглеводів. За числом атомів Карбону моносахариди поділяють на тетрози , пентози і гексози . За будовою вуглеводи мають по дві функціональні групи. Усі вуглеводи є багатоатомними спиртами з одного боку та альдегідами чи кетонами з іншого боку, тому за хімічними властивостями вуглеводи можуть бути альдегідо – спиртами (глюкоза, рибоза) або кетоно – спиртами (фруктоза). Для вуглеводів характерна циклічна та розгалужена будова. Полімеризація циклічної будови є основою для утворення полісахаридів. Наприклад, крохмаль утворений молекулами α – глюкози, целюлоза утворена молекулами β – глюкози.
21
8.1. Моносахариди глюкоза
Глюкоза має молекулярну формулу — С6Н12О6 . Молекули глюкози можуть мати або лінійну
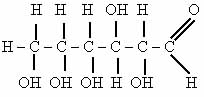 ,
скорчена форма СН2ОН
– (СНОН)4
– СОН, або
,
скорчена форма СН2ОН
– (СНОН)4
– СОН, або
циклічну форму:

α – глюкоза Альдегідна β – глюкоза
форма
У кристалах молекули глюкоза знаходиться в одній із двох циклічних форм: α – або β –. У водному розчині між цими формами існує динамічна рівновага:
Властивості глюкози Фізичні властивості
Глюкоза – біла кристалічна речовина, солодка на смак, добре розчинна у воді. У природі глюкоза утворюється в хлоропластах зелених рослин у процесі фотосинтезу:
6СО2
+ 6Н2О
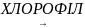 С6Н12О6
+ 6О2
+ Q
С6Н12О6
+ 6О2
+ Q
У мітохондріях живих організмів відбувається окиснення глюкози киснем повітря. При цьому виділяється енергія, яка використовується для процесів життєдіяльності.
Глюкоза міститься в рослинних і тваринних організмах, особливо багато її у винограді, меді, а також стиглих фруктах і ягодах, у корінні, листі та квітах рослин, у крові людини і тварин (близько 0,1 %).Глюкоза — цінна поживна речовина. Їжа людини складається приблизно на 70 % з вуглеводів.
Хімічні властивості
Хімічні властивості глюкози зумовлені наявністю в її молекулі альдегідної групи (у лінійній формі) і п’яти гідроксильних груп. Відповідно вона виявляє властивості альдегідів і багатоатомних спиртів.
І. Реакції за участю альдегідної групи.
1. Реакція, яка доводить, що глюкоза має альдегідну групу – це реакція «СРІБНОГО ДЗЕРКАЛА» – з амоніачним розчином аргентум оксиду:
AgNO3 + NaOH → AgOH ↓ + NaNO3
2AgOH → Ag2O + H2O
Ag2O + 4NH4OH → 2 [Ag(NH3)2]OH + 3H2O
22
CH2OH – (CHOH)4 – COH + Ag2O → CH2OH – (CHOH)4 – COOH + 2Ag↓
глюкоза глюконова кислота
2. Відновлення альдегідної групи:
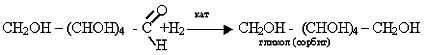
ІІ. Реакції за участю гідроксильних груп.
3. Із купрум(II) гідроксидом без нагрівання. Реакця, яка доводить, що глюкоза – це багатоатомний спирт. До розчину глюкози додають свіжовиготовлений осад купрум(ІІ)гідроксиду. З’являється яксраво – синє забрвлення – розчин купрум(ІІ)глюконат:
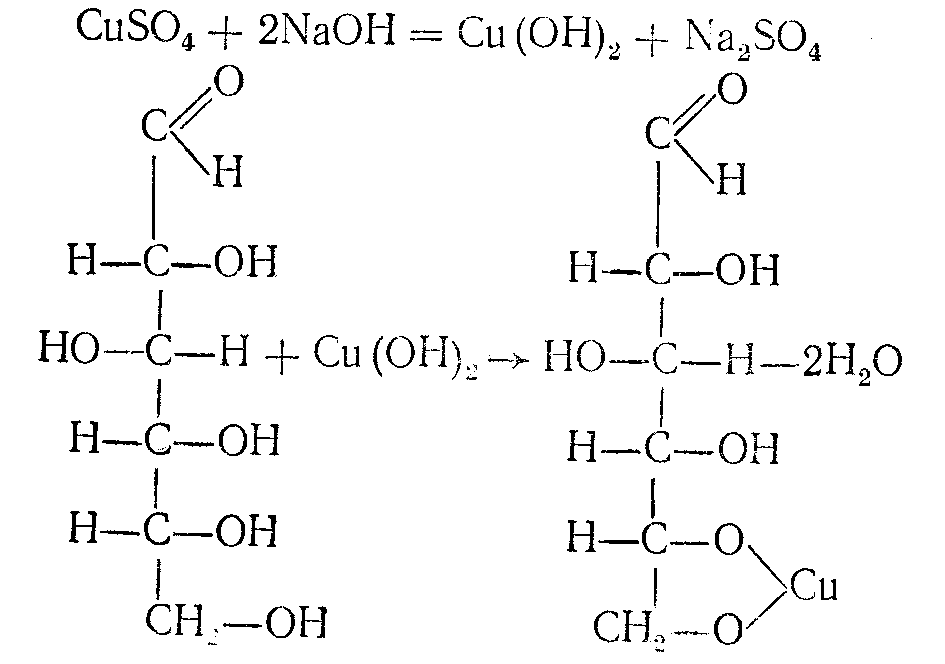
ІІІ. Реакції бродіння (проходять за участю мікроорганізмів).
4. Спиртове бродіння:
С6Н12О6
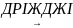 2С2Н5ОН
+ 2СО2↑
2С2Н5ОН
+ 2СО2↑
Етанол
5. Молочнокисле бродіння. Ця реакція проходить при скисанні молока, квашенні капусти, силосу, у процесі роботи м’язів у результаті енергетичного обміну:
С6Н12О6
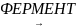 2СН3
– СНОН – СООН (без
повітря)
2СН3
– СНОН – СООН (без
повітря)
Молочна кислота
6. Маслянокисле бродіння. Масляна кислота, що утворюється, надає неприємного смаку і запаху згірклому вершковому маслу:
С6Н12О6 2С3Н7СООН + 2Н2↑ + 2СО2↑ (без повітря)
Масляна кислота
7. Поступове окиснення в організмах з повільним виділенням енергії:
С6Н12О6 + 6О2 → 6СО2 + 6Н2О + Q
ДОБУВАННЯ ГЛЮКОЗИ
Глюкозу добувають в основному гідролізом крохмалю або целюлози.
![]()
23
ЗАСТОСУВАННЯ ГЛЮКОЗИ
Глюкоза застосовується в медицині для приготування лікувальних препаратів, у кондитерському виробництві, у виробництві дзеркал та іграшок (сріблення), у хімічній промисловості.
8.2. ДИСАХАРИДИ
САХАРОЗА
Дисахариди – це вуглеводи, молекули яких складаються з двох залишків моносахаридів, які сполучені за рахунок взаємодії гідроксильних груп. До найважливіших дисахаридів належать сахароза, мальтоза, лактоза. Їх загальна формула С12Н22О11. Будова молекули сахарози має вигляд:

залишок залишок
α – глюкози β - глюкози
Сахароза у вигляді тростинного цукру була відома з давніх-давен, її використовували як лікувальний засіб. У Європі цукор з’явився у XVI столітті; а з цукрового буряку вперше був виділений у середині XVIII столітті. Доведено, що середньорічна потреба людини в цукрі становить близько 30 кг. Оскільки сахароза – цінний харчовий продукт, її добувають у великій кількості. Світове виробництво цукру перевищує 50 млн. тонн на рік. Україна виробляє кілька мільйонів тонн цукру на рік із цукрового буряку.
