- •Isbn 5-861852-282-0 © Мурманский государственный технический университет, 2006
- •© Николай Георгиевич Воронько оглавление Предисловие
- •Лабораторная работа 1 Рефрактометрия и строение молекул
- •Краткие теоретические сведения
- •Экспериментальная часть
- •Измерение и обработка результатов измерения
- •Контрольные вопросы
- •Литература
- •Лабораторная работа 2 Калориметрия. Определение интегральной теплоты растворения хорошо растворимой соли
- •Краткие теоретические сведения
- •Зависимость энтальпии реакции от температуры. Закон Киргофа
- •Значения теплоты растворения (Нраст) некоторых веществ в воде [1], [2]
- •Энтальпия гидратации ионов и солей в кДжмоль-1[1], [4]; радиусы ионов в пм
- •§5. Структурная температура и растворимость солей
- •Время ядерной спин-решеточной релаксации воды т1 при 21 с
- •§ 6. Растворимость в воде неполярных газов
- •Экспериментальная часть
- •Порядок выполнения работы
- •Контрольные вопросы
- •Литература
- •Примеры решения задач
- •Контрольные задачи
- •Cтандартные мольные энтальпии образования при 25 с (в кДж/моль)
- •Cтандартные мольные энтальпия образования и сгорания веществ при 25 с (в кДж/моль)
- •Энтальпия фазовых переходов Нm (в кДж/моль)
- •Значения энергии разрушения кристаллической решетки (Екр), энергии гидратации (Нгидр) и теплоты растворения (Нраст) некоторых солей в воде
- •Энтальпия кристаллической решетки (н) при 25 с [1], энергия гидратации (Нгидр) и теплоты растворения (Нраст) некоторых солей в воде
- •Лабораторная работа 3 Определение молярной массы растворенного вещества методом криометрии
- •Краткие теоретические сведения
- •Значения эвтектических температур водных растворов различных солей
- •Экспериментальная часть
- •Порядок выполнения работы
- •Выводы: Контрольные вопросы
- •Примеры решения задач
- •Контрольные задачи
- •Лабораторная работа 4 изучение электрической проводимости растворов электролитов
- •Краткие теоретические сведения
- •Экспериментальная часть Измерение электропроводности растворов электролитов методом компенсации
- •Измеритель rcl р5030
- •Порядок измерения сопротивления растворов электролитов на измерителе rcl р5030
- •Калибровка кондуктометрической ячейки
- •Опыт 1. Определение электрической проводимости растворов слабого электролита различной концентрации Порядок выполнения
- •Опыт 2. Определение электрической проводимости растворов сильного электролита различной концентрации Порядок выполнения
- •Контрольные вопросы
- •Контрольные задачи
- •Рекомендуемая литература
- •Использованная литература
- •Лабораторная работа 5 фотометрическое изучение кинетики разложения комплексного иона триоксалата марганца
- •Краткие теоретические сведения
- •Основные понятия и определения формальной кинетики
- •Средняя и истинная скорость реакции
- •Закон действующих масс
- •Принцип независимости протекания реакций
- •Вычисление констант скорости реакций различных порядков
- •Способы определения порядка реакции
- •Экспериментальная часть
- •1. Фотометрический метод.
- •Аппаратура и техника измерений
- •Порядок измерения оптической плотности на колориметре кфк-2
- •Порядок измерения оптической плотности на фотометре кфк-3
- •Фотометрическое изучение кинетики разложения комплексного иона триоксалата марганца
- •Порядок выполнения работы
- •Контрольные вопросы
- •Контрольные задачи
- •Рекомендуемая литература
- •Использованная литература
- •Литература
Измерение и обработка результатов измерения
1. Установите рефрактометр в удобное для измерений положение.
2. Перед началом работы проверьте установку нуль-пункта рефрактометра (устанавливается инженером кафедры).
3. Откройте верхнюю камеру и промойте дистиллированной водой или спиртом поверхности измерительной и осветительной призм и насухо вытрите их чистой льняной салфеткой. Пипеткой нанесите на поверхность измерительной призмы 2-3 капли дистиллированной воды, так чтобы поверхность призмы была покрыта водой и закройте верхнюю камеру.
4. Смещая осветитель, направьте луч света в окно верхней камеры. Источником света может служить электролампа или дневной свет. Рефрактометр и источник света установите так, чтобы свет падал на входное окно осветительной призмы.
5. Перемещением рукоятки с окуляром введите в поле зрения границу светотени. Резкость границы светотени, штрихов шкалы и перекрестия сетки установите вращением гайки окуляра.
6. Вращением рукоятки дисперсионного компенсатора устраните окрашенную границу светотени.
7. Поворотом рычага осветителя и вращением осветителя добейтесь максимальной контрастности границы светотени.
8. Перемещением рукоятки границу светотени подведите к центру перекрестия сетки и снимите показание прибора с учетом цены деления и точности отсчета (для дистиллированной воды опыт проведите три раза).
9. По окончании измерений откройте рефрактометрический блок и чистой салфеткой или листком фильтровальной бумаги удалите основное количество жидкости с рабочих поверхностей призм и оправ. Полированную грань измерительной призмы вытирайте очень осторожно, без нажима, чтобы не повредить полировку. После этого протирайте призмы мягкой салфеткой, смоченной спиртом, эфиром или смесью спирта и эфира, пока поверхность не станет блестящей. Рефрактометрический блок подержите некоторое время открытым для просушки.
10. Измерьте показатель преломления исследуемого вещества. Измерения проводите семь раз.
11. С помощью весов определите массу пустого и сухого пикнометра (gп. п) (рис. 5).
12. С помощью весов определите массу пикнометра с дистиллированной водой при данной температуре помещения (gп. в). Пикнометр заполните дистиллированной водой так, чтобы нижний мениск жидкости совпал с меткой. Если при заполнении пикнометра жидкости окажется больше, чем это необходимо, ее избыток удалите фильтровальной бумагой. Из справочной литературы найдите плотность дистиллированной воды (д. в) при данной температуре.
13. Из соотношения Vп = (gп. в gп. п) / д. в определите объем пикнометра.
Рис. 5. Пикнометр
14. Таким же образом заполните сухой пикнометр исследуемой жидкостью, взвесьте пикнометр с раствором. Найдите массу (gр-р) и плотность раствора по формуле р-р gр-р gп. пVп.
15. Рассчитайте семь значений молярной рефракции растворенного вещества RМ. Для этого в формулу (12) подставьте среднее арифметическое значение показателя преломления воды (< n.1 >) и значения n.2.
16. Найдите среднее
арифметическое значение молярной
рефракции <RМ>
растворенного вещества; абсолютные
погрешности RМ i
<RМ>
RМ i,
среднеквадратичное отклонение
![]() .
Для вероятности Р = 0.95 определите
ширину доверительного интервала Х(RМ)
= tP n
.
Для вероятности Р = 0.95 определите
ширину доверительного интервала Х(RМ)
= tP n![]() ,
где
,
где
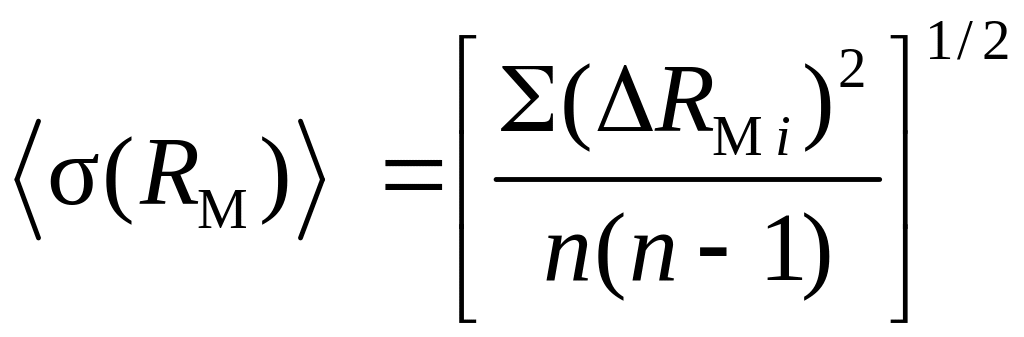 .
Величина коэффициента Стьюдента tP n
для вероятности Р = 0.95 и числа
измерений n = 3
составляет 4.3; для n
= 7 и Р = 0.95 величина tP n
равна 2.4. Если значение RМ i
выходит за пределы [<RМ>
– tP n
<RМ>
+ tP n
],
то данное значение является "промахом"
и при обработке результатов измерений
не учитывается.
.
Величина коэффициента Стьюдента tP n
для вероятности Р = 0.95 и числа
измерений n = 3
составляет 4.3; для n
= 7 и Р = 0.95 величина tP n
равна 2.4. Если значение RМ i
выходит за пределы [<RМ>
– tP n
<RМ>
+ tP n
],
то данное значение является "промахом"
и при обработке результатов измерений
не учитывается.
17. Запишите результат расчета в виде RМ.экс = <RМ> Х.
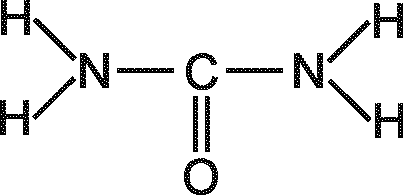
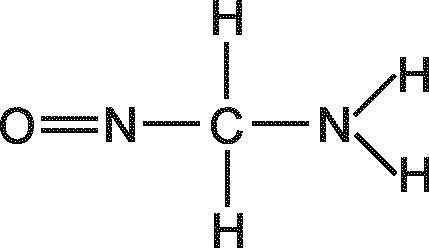
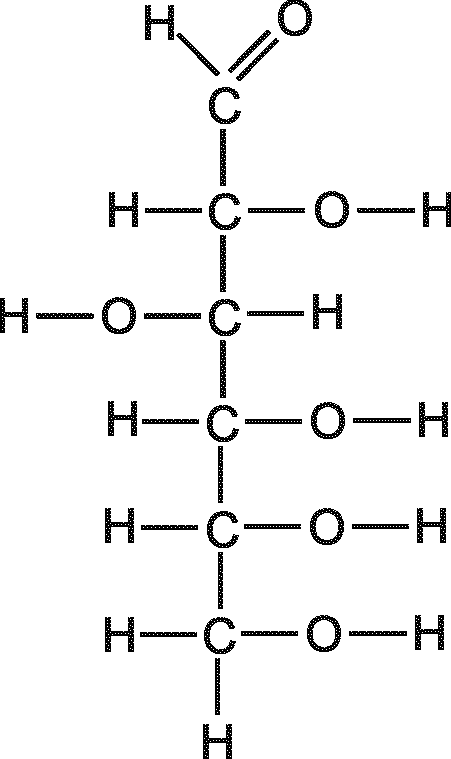
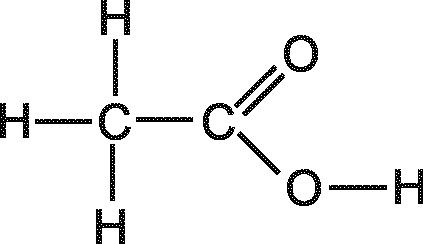
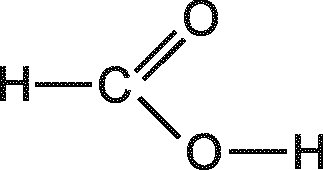
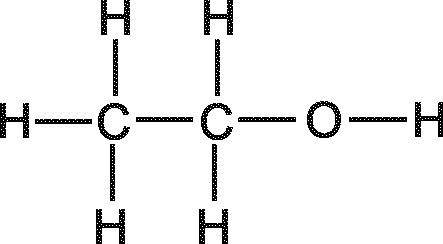
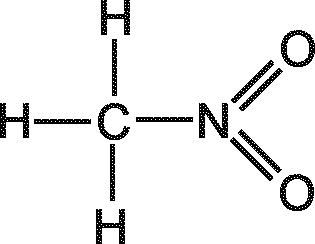
18. Рассчитайте теоретическое значение молярной рефракции по аддитивному методу RМ.теор=RМ.св=RМ.ат для нескольких структурных формул молекулы исследуемых веществ (рис.6). Данные для расчета возьмите из справочной литературы.
1.
|
или |
|
2.
|
или |
|
3.
а |
|
б |
|
в |
|
г |
|
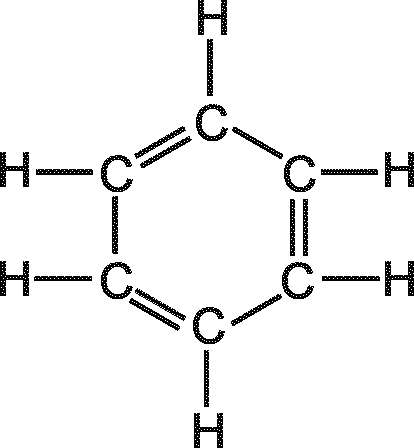
Рис. 6. Предполагаемые структуры молекулы некоторых веществ
19. Сравните значения RМ. теор с RМ. экс = <RМ> Х и сделайте выбор в пользу одной из структур молекулы растворенного вещества.
20. Сделайте выводы.