- •Isbn 5-861852-282-0 © Мурманский государственный технический университет, 2006
- •© Николай Георгиевич Воронько оглавление Предисловие
- •Лабораторная работа 1 Рефрактометрия и строение молекул
- •Краткие теоретические сведения
- •Экспериментальная часть
- •Измерение и обработка результатов измерения
- •Контрольные вопросы
- •Литература
- •Лабораторная работа 2 Калориметрия. Определение интегральной теплоты растворения хорошо растворимой соли
- •Краткие теоретические сведения
- •Зависимость энтальпии реакции от температуры. Закон Киргофа
- •Значения теплоты растворения (Нраст) некоторых веществ в воде [1], [2]
- •Энтальпия гидратации ионов и солей в кДжмоль-1[1], [4]; радиусы ионов в пм
- •§5. Структурная температура и растворимость солей
- •Время ядерной спин-решеточной релаксации воды т1 при 21 с
- •§ 6. Растворимость в воде неполярных газов
- •Экспериментальная часть
- •Порядок выполнения работы
- •Контрольные вопросы
- •Литература
- •Примеры решения задач
- •Контрольные задачи
- •Cтандартные мольные энтальпии образования при 25 с (в кДж/моль)
- •Cтандартные мольные энтальпия образования и сгорания веществ при 25 с (в кДж/моль)
- •Энтальпия фазовых переходов Нm (в кДж/моль)
- •Значения энергии разрушения кристаллической решетки (Екр), энергии гидратации (Нгидр) и теплоты растворения (Нраст) некоторых солей в воде
- •Энтальпия кристаллической решетки (н) при 25 с [1], энергия гидратации (Нгидр) и теплоты растворения (Нраст) некоторых солей в воде
- •Лабораторная работа 3 Определение молярной массы растворенного вещества методом криометрии
- •Краткие теоретические сведения
- •Значения эвтектических температур водных растворов различных солей
- •Экспериментальная часть
- •Порядок выполнения работы
- •Выводы: Контрольные вопросы
- •Примеры решения задач
- •Контрольные задачи
- •Лабораторная работа 4 изучение электрической проводимости растворов электролитов
- •Краткие теоретические сведения
- •Экспериментальная часть Измерение электропроводности растворов электролитов методом компенсации
- •Измеритель rcl р5030
- •Порядок измерения сопротивления растворов электролитов на измерителе rcl р5030
- •Калибровка кондуктометрической ячейки
- •Опыт 1. Определение электрической проводимости растворов слабого электролита различной концентрации Порядок выполнения
- •Опыт 2. Определение электрической проводимости растворов сильного электролита различной концентрации Порядок выполнения
- •Контрольные вопросы
- •Контрольные задачи
- •Рекомендуемая литература
- •Использованная литература
- •Лабораторная работа 5 фотометрическое изучение кинетики разложения комплексного иона триоксалата марганца
- •Краткие теоретические сведения
- •Основные понятия и определения формальной кинетики
- •Средняя и истинная скорость реакции
- •Закон действующих масс
- •Принцип независимости протекания реакций
- •Вычисление констант скорости реакций различных порядков
- •Способы определения порядка реакции
- •Экспериментальная часть
- •1. Фотометрический метод.
- •Аппаратура и техника измерений
- •Порядок измерения оптической плотности на колориметре кфк-2
- •Порядок измерения оптической плотности на фотометре кфк-3
- •Фотометрическое изучение кинетики разложения комплексного иона триоксалата марганца
- •Порядок выполнения работы
- •Контрольные вопросы
- •Контрольные задачи
- •Рекомендуемая литература
- •Использованная литература
- •Литература
Измеритель rcl р5030
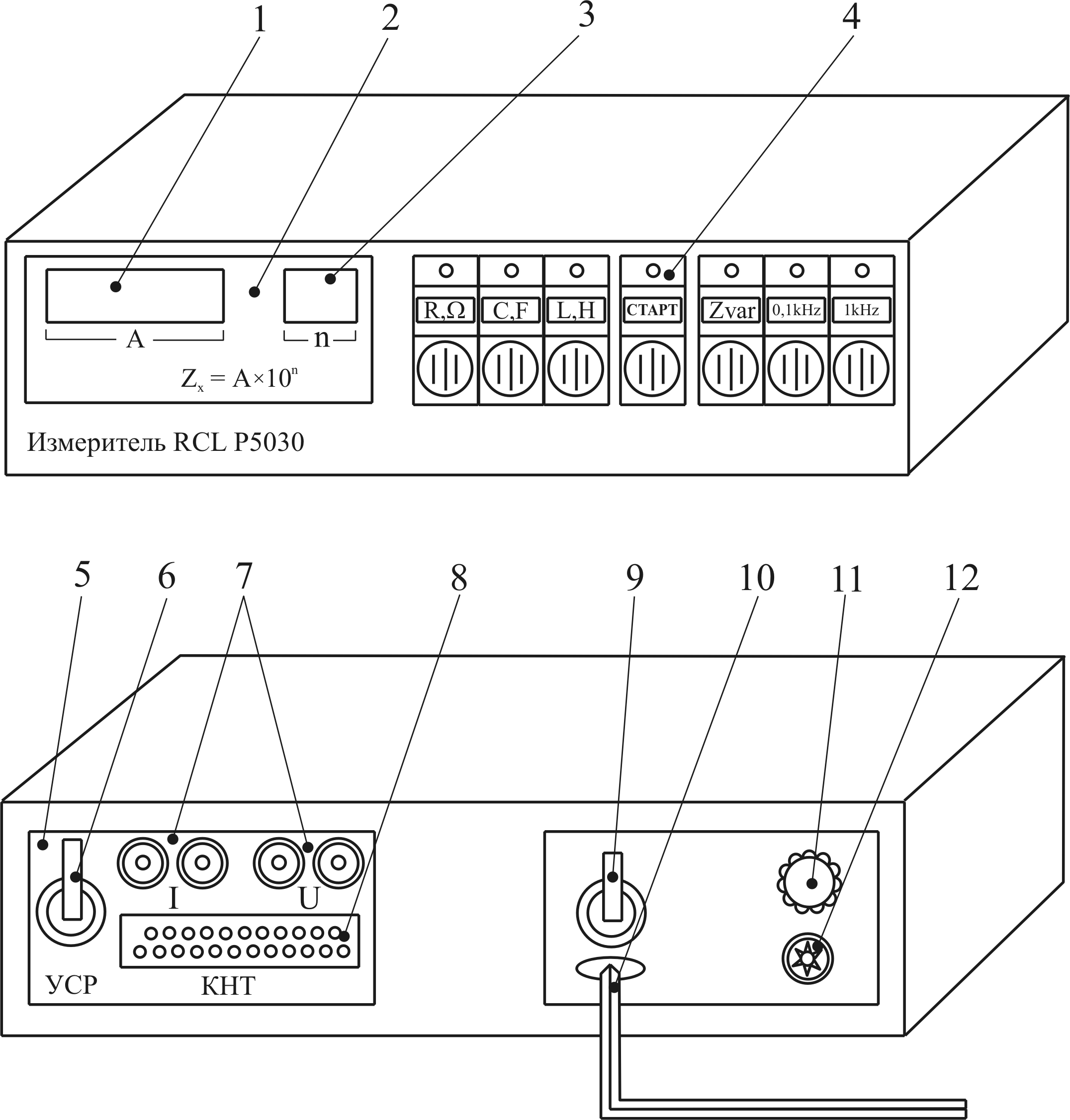
Для измерения сопротивления растворов электролитов, емкости и индуктивности используется измеритель RCL Р5030 (в дальнейшем – измеритель). Передняя и задняя панели измерителя изображены на рис. 7.
а
б
|
|
Рис. 7. Измеритель RCL Р5030: а – вид спереди; б – вид сзади; 1 – индикаторное табло 1; 2 – блок цифровой индикации; 3 – индикаторное табло 24; 4 – ячейки сенсорного переключателя; 5 – блок питания; 6 – тумблер включения режима "Усреднение"; 7 – соединители для подключения измерителя к объекту измерения; 8 – розетка для контроля за работой измерителя; 9 – тумблер включения питания; 10 – кабель подсоединения к сети питания; 11 – предохранитель; 12 – зажим для заземления корпуса
Порядок измерения сопротивления растворов электролитов на измерителе rcl р5030
1. Подключите зажим 12 к общей шине заземления.
2. Подключите измеритель к сети питания, предварительно убедившись, что тумблер 9 выключен.
3. Закрепите кондуктометрическую ячейку в лапке штатива. Подключите ячейку с помощью кабелей к соединителям 7. Налейте в стакан 50 мл исследуемого раствора электролита и поместите в него кондуктометрическую ячейку так, чтобы уровень жидкости был выше верхнего края электродов на 30 – 40 мм.
4. Включите тумблер 9 и прогрейте измеритель в течение 30 мин.
5. Установите измеряемую величину R и частоту измерения 1 кГц прикосновением касанием руки к ячейкам сенсорного переключателя 4 "R, " и "1 kHz".
5. Включите тумблер режима "Усреднение" 6. При работе в этом режиме на индикаторном табло 1 указывается среднее арифметическое результатов десяти измерительных циклов.
6. После измерения сопротивления выключите тумблер 9, отключите измеритель от сети питания, отсоедините кондуктометрическую ячейку и промойте электроды сначала водопроводной, потом дистиллированной водой.
Калибровка кондуктометрической ячейки
Если бы расстояние между электродами кондуктометрической ячейки было равно 1 м, площадь каждого электрода была бы равна 1 м2, а в проведении тока участвовал бы только объем раствора, заключённый между электродами, то измеренное в таких условиях электрическое сопротивление являлось бы удельным сопротивлением раствора электролита . Зная , легко можно было бы определить удельную электропроводность (см. формулу (3)). В действительности электропроводность зависит не только от размеров электродов и расстояния между ними, но и от их формы и взаимного расположения в объеме раствора, так как ток проходит не только через поверхность участков электродов, обращенных друг к другу, но и через окружающий электроды раствор. Для учета геометрических особенностей кондуктометрической ячейки в формулу (3) вводится коэффициент :
 . (34)
. (34)
Так как в процессе измерений , l и S остаются постоянными, то формулу (34) можно записать в виде
 , (35)
, (35)
где К
– постоянная (константа)
кондуктометрической ячейки, м1
(![]() ).
).
Таким образом, для измерения электропроводности растворов элект-ролитов необходимо произвести калибровку кондуктометрической ячейки, т. е. определить К. Для определения К измеряют сопротивление стандартных растворов электролитов (обычно KCl или NaCl) с известной удельной электропроводностью. Например, для определения К можно использовать 0,02 н раствор KCl, удельная электропроводность которого при Т = 298 К равна: 298 = 0,2765 См/м. Если опыт проводится при другой температуре, для расчёта Т(KCl) используют формулу
Т = 298[1 + (T – 298,15) + (T – 298,15)2];
= 0,0163( 0,0174), (36)
где и – температурные коэффициенты электропроводности, зависящие от природы электролита (для сильных кислот = 0,0164; для сильных оснований = 0,0190; для солей = 0,0220).
В чистый сухой стакан наливают 50 мл 0,02 н раствора KCl, отмеренного с помощью пипетки, и измеряют его сопротивление R(KCl). Постоянную ячейки К находят по формуле
К = (KCl) R (KCl). (37)