
- •Часть II
- •Введение
- •Порядок и правила взвешивания
- •Проверка вместимости мерной посуды - колб, пипеток. Проверка калибровки бюретки.
- •Основные этапы работы
- •Лабораторная работа № 2 Кислотно-основное титрование. Метод нейтрализации
- •I. Стандартизация раствора соляной кислоты
- •II. Определение массы щелочи в анализируемом растворе
- •III. Раздельное определение едких щелочей и карбонатов в анализируемой смеси
- •IV. Стандартизация раствора гидроксида натрия (калия)
- •V. Определение массы фосфорной кислоты в растворе
- •Вопросы для контроля усвоения темы
- •Лабораторная работа № 3 Редокс титрование. Перманганатометрия
- •Приготовление стандартного раствора щавелевой кислоты (или оксалата натрия)
- •II. Стандартизация раствора перманганата калия
- •Определение массы железа (II) в растворе соли мора
- •Вопросы для контроля усвоения темы
- •Лабораторная работа № 4 йодометрия и йодиметрия
- •I. Стандартизация раствора тиосульфата натрия
- •II. Определение содержания аскорбиновой кислоты
- •Вопросы для контроля усвоения темы
- •Лабораторная работа № 5 броматометрия
- •Приготовление стандартного раствора бромата калия
- •II. Определение содержания стрептоцида
- •Нитритометрия
- •I. Стандартизация раствора нитрита натрия
- •II. Определение содержания стрептоцида
- •Вопросы для контроля усвоения темы
- •Лабораторная работа № 6 комплексонометрия
- •I. Стандартизация раствора трилона б
- •II. Определение содержания кальция в фармпрепаратах
- •Вопросы для контроля усвоения темы
- •Лабораторная работа № 7 осадительное титрование. Тиоцианатометрия
- •I. Стандартизация раствора тиоцианата аммония или калия
- •II. Определение содержания серебра
- •Вопросы для контроля усвоения темы
- •Приложение коэффициенты распределения стьюдента
- •Значения q для исключения сомнительных результатов
- •Содержание
Лабораторная работа № 6 комплексонометрия
Цель изучения данной темы:
Научится стандартизовать раствор трилона Б. Освоить определение содержания веществ методом комплексонометрического титрования.
Комплексонометрия – метод, основанный на использовании реакций образования комплексных соединений катионов металлов с комплексонами. В титриметрическом анализе наиболее широко применяется комплексон III (двунатриевая соль этилендиаминтетрауксусной кислоты Na2H2Y2H2O, ЭДТА - этилендиаминтетраацетат, трилон Б):
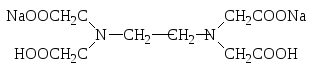
Комплексонометрию используют для количественного определения различных неорганических лекарственных препаратов магния, цинка, кальция, висмута (например, сульфат магния, карбонат и гидрокарбонат магния, оксид цинка, хлорид кальция, нитрат висмута и т.д.). Аналогично определяют кальциевые коли органических кислот (кальция лактат, кальция глюконат, кальция пангамат и др.).
Во всех реакциях 1 моль металла, независимо от степени окисления, всегда связывает 1 моль комплексона III, поэтому молярные массы эквивалентов трилона Б и определяемых металлов соответственно равны молярным массам.
В комплексонометрическом титровании используют металлохромные индикаторы – вещества, образующие с ионами металлов интенсивно окрашенные комплексные соединения, например, мурексид, ксиленоловый оранжевый, эриохром черный Т и др.
В качестве титранта метода применяют водный раствор ЭДТА. Его готовят по точной навеске Na2H2Y2H2O, а затем уточняют молярную концентрацию эквивалента по стандартному раствору сульфата магния или сульфата цинка.
I. Стандартизация раствора трилона б
Материальное обеспечение:
-
Мерные колбы, Vном. = 200 или 250 мл.
-
Мерные пипетки, Vном. = 10 мл.
-
Мерные пипетки, 5 мл.
-
Мерные бюретки, 0-25 мл.
-
Промывалки с дистиллированной водой.
-
Конические колбы для титрования.
-
Химические воронки 40-50 мм.
-
Стаканчики под слив.
-
Фильтровальная бумага.
-
Раствор MgSO4 известной концентрации.
-
Аммиачный буферный раствор (рН 9-10).
-
Раствор трилона Б неизвестной концентрации.
-
Индикатор эриохром черный.
В колбу для титрования помещают пипеткой 10 мл раствора сульфата магния, добавляют 5 мл аммиачного буферного раствора (рН 9-10) и немного индикатора эриохрома черного. Раствор окрашивается в красно-фиолетовый цвет. Титруют раствором трилона Б до перехода окраски в синюю.
По результатам титрования рассчитывают молярную концентрацию эквивалента раствора трилона Б:
![]()
где: С(ЭДТА) – молярная концентрация эквивалента раствора трилона Б, моль/л;
V(MgSO4) - объем раствора сульфата магния, взятый для титрования, мл;
С(MgSO47H2O) - молярная концентрация эквивалента раствора сульфата магния, моль/л;
V(ЭДТА) - эквивалентный объем раствора трилона Б, пошедший на титрование, мл.
II. Определение содержания кальция в фармпрепаратах
Материальное обеспечение:
-
Аналитические демпферные весы с разновесами.
-
Мерные пипетки, Vном. = 10 мл.
-
Мерные пипетки, 5 мл.
-
Мерные бюретки, 0-25 мл.
-
Промывалки с дистиллированной водой.
-
Конические колбы для титрования.
-
Химические воронки 40-50 мм.
-
Стаканчики под слив.
-
Фильтровальная бумага.
-
Порошок фармпрепарата кальция.
-
Аммиачный буферный раствор (рН 9-10).
-
Раствор трилона Б известной концентрации.
-
Индикатор эриохром черный.
0,04-0,06 г порошка фармпрепарата (взвешенного на аналитических весах) растворяют при нагревании в 5 мл воды в колбе для титрования, прибавляют 2 мл аммиачного буферного раствора (рН 9-10) и немного индикатора эриохрома черного. Раствор окрашивается в красно-фиолетовый цвет. Титруют раствором трилона Б до перехода окраски в синюю.
По результатам титрования рассчитывают содержание кальция в исследуемой пробе:
(Cа) = V(ЭДТА)C(ЭДТА)M(Ca)100% / (m1000) , %(масс.)
где: С (ЭДТА) – молярная концентрация эквивалента раствора трилона Б, моль/л;
V (ЭДТА) - эквивалентный объем раствора трилона Б, пошедший на титрование, мл;
M (Ca) – молярная масса эквивалента кальция, равная 40 г/моль;
m – масса навески исследуемого вещества, г.
