
- •1 Оглавление
- •Часть 1
- •Молекулярная физика и термодинамика 84
- •Итоговые задания 130 предисловие
- •В добрый путь, читатель, – удачи!
- •Введение
- •Физическая картина мира
- •Математическое введение Углы
- •Скаляры и векторы
- •Натуральные логарифмы
- •Суммирование
- •Элементы дифференциального исчисления
- •Элементы интегрального исчисления
- •Глава 1 механика
- •Кинематика
- •Механическое движение
- •Вектор перемещения. Путь
- •Скорость
- •Ускорение
- •Равномерное и равнопеременное прямолинейные движения
- •Свободное падение тел
- •Равномерное движение точки по окружности
- •Вращательное движение абсолютно твердого тела вокруг неподвижной оси
- •Динамика движения материальной точки
- •Классическая механика. Границы ее применимости
- •Первый закон Ньютона. Инерциальные системы отсчета
- •Масса и импульс
- •Второй закон Ньютона
- •Третий закон Ньютона
- •Закон сохранения импульса
- •Механический принцип относительности Галилея – Ньютона
- •Силы тяготения
- •Силы упругости
- •Силы трения
- •Элементы динамики вращательного движения абсолютно твердого тела относительно неподвижной оси
- •Момент силы и момент инерции
- •Основной закон динамики вращательного движения
- •Статика
- •Работа и механическая энергия
- •Работа силы при движении материальной точки
- •Механическая энергия
- •Закон сохранения и превращения энергии
- •Мощность
- •Элементы гидроаэромеханики
- •Закон Паскаля
- •Закон Архимеда
- •Давление в движущейся среде
- •Внутреннее трение
- •Основы специальной теории относительности
- •Постулаты Эйнштейна
- •Интервалы длины и времени
- •Закон сложения скоростей
- •Энергия
- •Ответы на вопросы к главе 1
- •Глава 2 молекулярная физика и термодинамика
- •Основы молекулярно-кинетической теории вещества
- •Основные понятия и определения
- •Силы и потенциальная энергия взаимодействия двух молекул
- •О строении газообразных, жидких и твердых тел
- •Молекулярно-кинетическая теория идеальных газов
- •Идеальный газ
- •Распределение Максвелла – Больцмана
- •Распределение Больцмана
- •Средняя длина свободного пробега молекулы
- •Основное уравнение кинетической теории газов
- •Уравнение состояния идеального газа
- •Связь средней кинетической энергии поступательного движения молекул и температуры
- •Реальные газы
- •Свойства жидкостей и твердых тел
- •Поверхностный слой
- •Поверхностное натяжение
- •Лапласово давление
- •Твердое тело
- •Термодинамика
- •Внутренняя энергия системы
- •Внутренняя энергия идеального газа
- •Первое начало термодинамики
- •Калориметрия33
- •Работа газа
- •Цикл Карно. Второе начало термодинамики
- •Некоторые тепловые машины
- •Изменение агрегатного состояния вещества
- •Плавление. Кристаллизация
- •Парообразование. Конденсация. Испарение
- •Свойства паров
- •Кипение
- •Ответы на вопросы к главе 2
- •Итоговые задания
- •Часть 1
- •346500, Г. Шахты, Ростовская обл., ул. Шевченко, 147.
-
Работа газа
Один из возможных способов превращения внутренней энергии в механическую состоит в том, чтобы заставить нагретый газ совершать работу.
Пусть газ находится в цилиндрическом сосуде под поршнем (рис. 2.7) и расширяется, совершая работу, например, против атмосферного давления. Элементарная работа расширения
![]()
равна произведению давления газа на изменение его объема. Конечная работа равна
 .
.
Иначе,
работа процесса, изображенного на
![]() -
диаграмме, равна площади фигуры,
образованной графиком
-
диаграмме, равна площади фигуры,
образованной графиком
![]() ,
осью абсцисс и ординатами начала и
конца процесса (рис. 2.8).
,
осью абсцисс и ординатами начала и
конца процесса (рис. 2.8).
В частности, если процесс изобарный, то
давление можно вынести за знак интеграла,
и работа равна
частности, если процесс изобарный, то
давление можно вынести за знак интеграла,
и работа равна
 .
.
Используя уравнение состояния газа (см. подраздел 2.2.6), преобразуем полученное выражение:
![]() .
.
Следовательно, чтобы газ при изобарном
расширении совершил положительную
работу, необходимо увеличение температуры
![]() ,
т.е. нагревание. Это один из возможных
способов преобразования внутренней
энергии в механическую и он не является
ни единственным, ни лучшим. Как сделать
такое преобразование выгодным и
технически применимым, обсудим ниже.
,
т.е. нагревание. Это один из возможных
способов преобразования внутренней
энергии в механическую и он не является
ни единственным, ни лучшим. Как сделать
такое преобразование выгодным и
технически применимым, обсудим ниже.
-
Г
 аз
нагревают, при этом его температура
увеличивается на
аз
нагревают, при этом его температура
увеличивается на
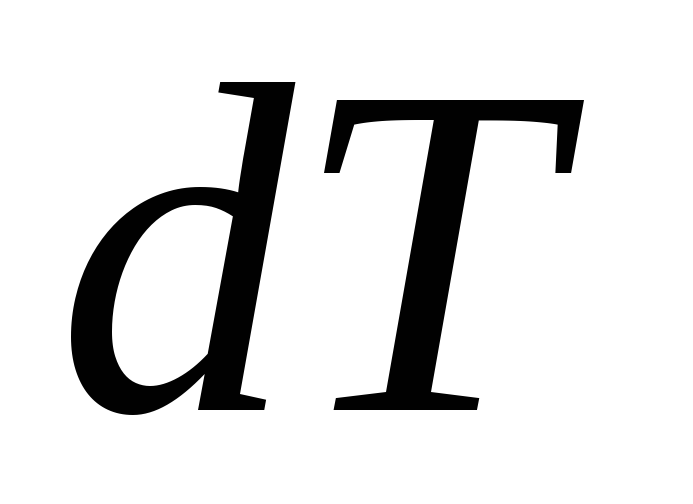 .
Делают это два раза: один раз при
постоянном объеме газа, другой – при
постоянном давлении. Одинаковое ли
количество теплоты надо затратить на
нагревание газа в указанных случаях?
.
Делают это два раза: один раз при
постоянном объеме газа, другой – при
постоянном давлении. Одинаковое ли
количество теплоты надо затратить на
нагревание газа в указанных случаях?
-
Цикл Карно. Второе начало термодинамики
Тепловой машиной называется устройство, в котором хаотическое движение молекул превращается в движение упорядоченное; иначе, внутренняя энергия превращается в механическую. В такой машине должно быть какое-то рабочее вещество (тело), которое в рабочей части машины совершает механическую работу; должен быть нагреватель, где рабочее вещество получает определенную порцию внутренней энергии. Тепловая машина, рассчитанная на более или менее длительный срок работы, должен работать циклично. Пусть рабочее вещество совершает положительную работу, расширяясь от состояния 1 до состояния 2 (рис.2.9). Чтобы замкнуть цикл, есть три возможности:
-
в
 озвратиться
по тому же процессу (через те же
состояния). Но работа равна площади
под кривой процесса. Следовательно,
работа за цикл получится равной нулю,
даже без учета неизбежных потерь;
озвратиться
по тому же процессу (через те же
состояния). Но работа равна площади
под кривой процесса. Следовательно,
работа за цикл получится равной нулю,
даже без учета неизбежных потерь; -
можно возвратиться через состояния, лежащие выше кривой прямого процесса (штрихпунктир). Тогда отрицательная работа станет больше (по абсолютному значению) положительной, и двигателем такая машина быть не может (она является холодильной машиной, ее цикл изображен на рис. 2.11);
-
наконец, можно возвратиться через состояния, лежащие ниже прямого процесса. При этом отрицательная работа численно равна заштрихованной площади (рис. 2.9) и, следовательно, меньше положительной работы прямого процесса.
В
результате такого прямого
цикла достигнуто первоначальное
состояние и совершена положительная
работа, равная площади цикла. Но для
того чтобы пройти через состояния с
теми же объемами и с меньшими давлениями,
необходимо понизить температуру. Для
этого какое-то количество теплоты надо
отнять у рабочего тела, для чего в каждой
тепловой машине необходим холодильник.
Итак, основными частями всякой тепловой
машины являются (рис. 2.10): нагреватель,
сообщающий рабочему телу количество
теплоты
![]() ;
рабочая часть, в которой совершается
механическая работа А;
холодильник, отбирающий у рабочего
тела количество теплоты
;
рабочая часть, в которой совершается
механическая работа А;
холодильник, отбирающий у рабочего
тела количество теплоты
![]() .
Полезно используется, т.е. превращается
в механическую работу, количество
теплоты
.
Полезно используется, т.е. превращается
в механическую работу, количество
теплоты
![]() ,
и коэффициент полезного действия
(к.п.д.) тепловой машины (без учета потерь)
равен
,
и коэффициент полезного действия
(к.п.д.) тепловой машины (без учета потерь)
равен
![]() . (2.13)
. (2.13)
Заставив
машину работать по обратному
циклу (рис. 2.11), мы получили за цикл
отрицательную работу, численно равную
площади цикла. При этом у холодильника
будет отобрано, а нагревателю передано
некоторое количество теплоты. Такую
машину надо приводить в движение извне;
двигателем, как отмечено выше, она не
будет. Но у нее есть две важнейшие
функции. Она является холодильной
машиной,
так как охлаждает холодильник. Кроме
того, она является тепловым
насосом,
так как перекачивает за счет внешней
работы количество теплоты из холодильника
в нагреватель, причем отдает нагревателю
большее количество теплоты, чем получает
из холодильника:
![]() ,
отсюда
,
отсюда
![]() (все члены этого равенства отрицательны).
Поэтому даже с учетом потерь выгодна
идея термодинамического отопления:
вместо обычной печи сжигать топливо в
тепловой машине, ею приводить в движение
тепловой насос, который будет перекачивать
количество теплоты с улицы в помещение.
(все члены этого равенства отрицательны).
Поэтому даже с учетом потерь выгодна
идея термодинамического отопления:
вместо обычной печи сжигать топливо в
тепловой машине, ею приводить в движение
тепловой насос, который будет перекачивать
количество теплоты с улицы в помещение.
Рабочим телом в тепловой машине может быть любое вещество. Какие же процессы наиболее выгодны для тепловой машины?
Если в качестве рабочего тела взять идеальный газ, то его потенциальная энергия равна нулю (нет взаимодействия, зависящего от конфигурации), следовательно, внутренняя энергия равна суммарной кинетической энергии, пропорциональной температуре. Примем без доказательства, что изменение внутренней энергии идеального газа
![]() ,
,
где
![]() удельная
теплоемкость газа при постоянном
объеме.
удельная
теплоемкость газа при постоянном
объеме.
Следовательно,
 .
.
Изменение
внутренней энергии идеального газа
пропорционально разности температур
конечного и начального состояний:
![]() ~
~![]() .
Поэтому изменение внутренней энергии
при изотермическом процессе равно
нулю.
.
Поэтому изменение внутренней энергии
при изотермическом процессе равно
нулю.
Согласно
первому началу термодинамики одним из
наиболее выгодных процессов –
изотермический, так как в этом процессе
все подводимое к системе количество
теплоты равно работе системы
![]() .
Но нельзя осуществить сколь-нибудь
длительный процесс, двигаясь в одну
сторону по определенной изотерме! Зато
можно представить себе еще более
«выгодный» процесс, при котором
.
Но нельзя осуществить сколь-нибудь
длительный процесс, двигаясь в одну
сторону по определенной изотерме! Зато
можно представить себе еще более
«выгодный» процесс, при котором
![]() .
.
Процесс,
при котором нет теплообмена с окружающей
средой, называется адиабатным34.
Кривая такого процесса – адиабата.
При таком процессе механическая работа
совершается за счет уменьшения внутренней
энергии:
![]() .
Разделим это уравнение почленно на
уравнение состояния идеального газа
.
Разделим это уравнение почленно на
уравнение состояния идеального газа
![]() :
:
![]() ,
интегрируем:
,
интегрируем:
 и получаем
и получаем
![]()

логарифмическое уравнение. Следовательно,
логарифмическое уравнение. Следовательно,
 или
или
 ,
,
откуда  и
и
 .
.
Значит
 или
или
![]()
для двух произвольных состояний. Произведение давления данной массы газа на его объем в степени есть величина постоянная в адиабатном процессе:
![]()
уравнение Пуассона,
где
![]() коэффициент
Пуассона (показатель адиабаты).
коэффициент
Пуассона (показатель адиабаты).
Если
изменение внутренней энергии
![]() пропорционально разности температур
пропорционально разности температур
![]() ,
то для получения положительной работы
в адиабатном процессе необходима
отрицательная разность энергий и
температур
,
то для получения положительной работы
в адиабатном процессе необходима
отрицательная разность энергий и
температур
![]() .
.
Следовательно,
адиабатное расширение из некоторого
состояния на
![]() - диаграмме изображается кривой, лежащей
ниже соответствующего изотермического
расширения; иными словами, адиабата
проходит через некоторую точку
(состояние) на
- диаграмме изображается кривой, лежащей
ниже соответствующего изотермического
расширения; иными словами, адиабата
проходит через некоторую точку
(состояние) на
![]() -
диаграмме круче, чем изотерма.
-
диаграмме круче, чем изотерма.
И если нужно найти самый выгодный
циклический процесс, то надо два
изотермических процесса замкнуть двумя
адиабатами (рис.2.12). Такой процесс
предложил французский инженер С. Карно,
он же рассчитал к.п.д. идеальной машины,
работающей по такому циклу.
если нужно найти самый выгодный
циклический процесс, то надо два
изотермических процесса замкнуть двумя
адиабатами (рис.2.12). Такой процесс
предложил французский инженер С. Карно,
он же рассчитал к.п.д. идеальной машины,
работающей по такому циклу.
Удельная теплоемкость при постоянном давлении
![]()
При температуре Т1 (см. рис. 2.12) идеальный газ получает количество теплоты Q1, при температуре Т2 – отдает количество теплоты Q2, причем


Объемы,
стоящие под знаками логарифмов, связаны
изотермами
![]() и
и
![]() и адиабатами
и адиабатами
![]() ;
;
![]() ,
откуда
,
откуда
![]() .
Заменим отношения давлений:
.
Заменим отношения давлений:
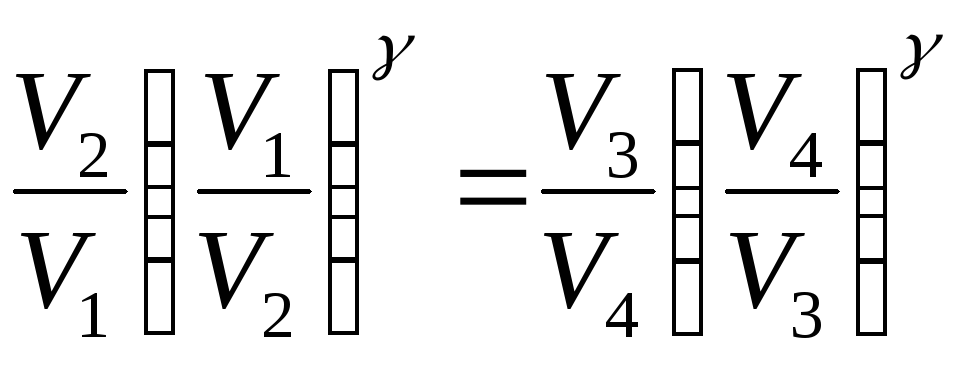 .
.
После
сокращения получим
![]() и
и
![]() .
Значит,
.
Значит,
![]() .
Следовательно, коэффициент полезного
действия цикла Карно (2.13)
.
Следовательно, коэффициент полезного
действия цикла Карно (2.13)

Таким образом,
![]() ,
,
где
![]() и
и
![]() температура
нагревателя и холодильника.
температура
нагревателя и холодильника.
Кроме того, Карно доказал, что к.п.д. реальной машины меньше к.п.д. идеальной машины, работающей между теми же температурами:
![]() ,
,
где знак равенства относится только к идеальной машине. Из последнего равенства легко получить
![]() .
.
Значит, даже
идеальная машина, работающая по циклу
Карно, не может иметь к.п.д., равный
единице, или работать без холодильника,
так как это было бы возможно только при
![]() К
(абсолютный нуль), а такая температура
недостижима. Это связано с различием
двух форм движения: механического –
упорядоченного, и молекулярного –
беспорядочного.
К
(абсолютный нуль), а такая температура
недостижима. Это связано с различием
двух форм движения: механического –
упорядоченного, и молекулярного –
беспорядочного.
Энергия упорядоченного движения
полностью преобразуется в энергию
беспорядочного движения, например, при
неупругом ударе о стенку. Энергия же
беспорядочного движения в тепловой
машине может быть преобразована в
механическую энергию только частично,
некоторая ее часть должна остаться
хаотической и в виде количества теплоты
![]() передается холодильнику.
передается холодильнику.
Итак, к.п.д. тепловой машины не может быть равен единице, машина не может работать без холодильника. Это одна из формулировок второго начала термодинамики.
Другой, не менее важной формулировкой второго начала термодинамики является критерий направленности процессов теплообмена: количество теплоты не может самопроизвольно переходить от тел с меньшей к телам с большей температурой (Клаузиус).
Самопроизвольно процессы идут в определенную сторону. Например, сжатый газ легко выходит из открытого сосуда, но практически никогда не войдет обратно (хотя, на первый взгляд, какая разница, куда молекулам хаотически двигаться – внутрь или наружу?). Нельзя категорически утверждать, что молекулы не могут вновь собраться в сосуде. Просто вероятность этого события ничтожно мала.
Итак, второе начало термодинамики предсказывает, с какой вероятностью процесс пойдет в ту или иную сторону, и этот статистический подход тем обоснование, чем больше частиц в термодинамической системе.
