
- •1 Оглавление
- •Часть 1
- •Молекулярная физика и термодинамика 84
- •Итоговые задания 130 предисловие
- •В добрый путь, читатель, – удачи!
- •Введение
- •Физическая картина мира
- •Математическое введение Углы
- •Скаляры и векторы
- •Натуральные логарифмы
- •Суммирование
- •Элементы дифференциального исчисления
- •Элементы интегрального исчисления
- •Глава 1 механика
- •Кинематика
- •Механическое движение
- •Вектор перемещения. Путь
- •Скорость
- •Ускорение
- •Равномерное и равнопеременное прямолинейные движения
- •Свободное падение тел
- •Равномерное движение точки по окружности
- •Вращательное движение абсолютно твердого тела вокруг неподвижной оси
- •Динамика движения материальной точки
- •Классическая механика. Границы ее применимости
- •Первый закон Ньютона. Инерциальные системы отсчета
- •Масса и импульс
- •Второй закон Ньютона
- •Третий закон Ньютона
- •Закон сохранения импульса
- •Механический принцип относительности Галилея – Ньютона
- •Силы тяготения
- •Силы упругости
- •Силы трения
- •Элементы динамики вращательного движения абсолютно твердого тела относительно неподвижной оси
- •Момент силы и момент инерции
- •Основной закон динамики вращательного движения
- •Статика
- •Работа и механическая энергия
- •Работа силы при движении материальной точки
- •Механическая энергия
- •Закон сохранения и превращения энергии
- •Мощность
- •Элементы гидроаэромеханики
- •Закон Паскаля
- •Закон Архимеда
- •Давление в движущейся среде
- •Внутреннее трение
- •Основы специальной теории относительности
- •Постулаты Эйнштейна
- •Интервалы длины и времени
- •Закон сложения скоростей
- •Энергия
- •Ответы на вопросы к главе 1
- •Глава 2 молекулярная физика и термодинамика
- •Основы молекулярно-кинетической теории вещества
- •Основные понятия и определения
- •Силы и потенциальная энергия взаимодействия двух молекул
- •О строении газообразных, жидких и твердых тел
- •Молекулярно-кинетическая теория идеальных газов
- •Идеальный газ
- •Распределение Максвелла – Больцмана
- •Распределение Больцмана
- •Средняя длина свободного пробега молекулы
- •Основное уравнение кинетической теории газов
- •Уравнение состояния идеального газа
- •Связь средней кинетической энергии поступательного движения молекул и температуры
- •Реальные газы
- •Свойства жидкостей и твердых тел
- •Поверхностный слой
- •Поверхностное натяжение
- •Лапласово давление
- •Твердое тело
- •Термодинамика
- •Внутренняя энергия системы
- •Внутренняя энергия идеального газа
- •Первое начало термодинамики
- •Калориметрия33
- •Работа газа
- •Цикл Карно. Второе начало термодинамики
- •Некоторые тепловые машины
- •Изменение агрегатного состояния вещества
- •Плавление. Кристаллизация
- •Парообразование. Конденсация. Испарение
- •Свойства паров
- •Кипение
- •Ответы на вопросы к главе 2
- •Итоговые задания
- •Часть 1
- •346500, Г. Шахты, Ростовская обл., ул. Шевченко, 147.
Глава 2 молекулярная физика и термодинамика
-
Основы молекулярно-кинетической теории вещества
-
Основные понятия и определения
-
Молекулярно-кинетической теорией называется учение, которое объясняет строение и свойства тел движением и взаимодействием атомов20, молекул21 и ионов, из которых состоят тела. В основе молекулярно-кинетической теории лежат три важнейших положения, которые полностью подтверждены экспериментально и теоретически:
-
Все тела состоят из частиц – молекул, атомов и ионов, в состав которых входят более мелкие элементарные частицы.
-
Атомы, молекулы и ионы находятся в непрерывном хаотическом тепловом движении.
-
Между частицами любого тела существуют силы взаимодействия – притяжения и отталкивания.
Эти исходные положения подтверждаются явлениями диффузии (процесс выравнивания плотностей или концентраций двух веществ при их смешивании друг с другом), броуновского движения (непрерывное хаотичное движение взвешенных в жидкости частиц), особенностями строения и свойствами жидкости и твердых тел, а также исследованиями в области физики элементарных частиц.
-
П
 очему
броуновские частицы должны быть все
же относительно малы? Почему броуновское
движение не наблюдается для заметных
крупиц вещества, например, для чаинок
в стакане?
очему
броуновские частицы должны быть все
же относительно малы? Почему броуновское
движение не наблюдается для заметных
крупиц вещества, например, для чаинок
в стакане?
Атомом называется наименьшая частица одного химического элемента. Каждому химическому элементу соответствуют вполне определенные атомы, сохраняющие химические свойства данного элемента. Атом состоит из положительно заряженного ядра и отрицательно заряженных электронов, движущихся в электрическом поле ядра.
Молекулой называется наименьшая устойчивая частица данного вещества, обладающая его основными химическими свойствами. Молекула состоит из одного или нескольких атомов одинаковых или разных химических элементов.
Атомы соединяются в молекулу за счет химических связей, основанных на различных взаимодействиях внешних (валентных) электронов. Как и атом, молекула электрически нейтральна, т.е. содержит равное количество электрически заряженных частиц противоположного знака.
Количеством вещества называется физическая величина, определяемая числом специфических структурных элементов – молекул, атомов или ионов, из которых состоит вещество. Единицей количества вещества является моль.
Число
атомов (или других структурных единиц),
содержащихся в одном моле вещества,
называется числом
(или постоянной)
Авогадро
![]() моль-1.
моль-1.
Объем
одного моля называется молярным
объемом
![]() :
:
![]() ,
,
где ![]() удельный объем;
удельный объем;
![]() плотность вещества;
плотность вещества;
![]() масса одного моля (молярная масса).
масса одного моля (молярная масса).
При нормальных условиях
![]() молярные объемы всех идеальных газов
одинаковы
молярные объемы всех идеальных газов
одинаковы
![]() .
.
Молярная
масса
![]() ,
где
,
где
![]() масса одного структурного элемента.
масса одного структурного элемента.
-
Силы и потенциальная энергия взаимодействия двух молекул
Между
молекулами любого вещества одновременно
действуют силы взаимного притяжения и
отталкивания (межмолекулярное
взаимодействие). Две молекулы, свободные
от любых воздействий, кроме силы
![]() межмолекулярного взаимодействия, должны
сближаться или удаляться друг от друга
в зависимости от того, какая сила
преобладает – сила притяжения или сила
отталкивания. Лишь при расстоянии
межмолекулярного взаимодействия, должны
сближаться или удаляться друг от друга
в зависимости от того, какая сила
преобладает – сила притяжения или сила
отталкивания. Лишь при расстоянии
![]() между молекулами, на котором
между молекулами, на котором
![]() ,
молекулы находятся в равновесии.
,
молекулы находятся в равновесии.
Потенциальной
энергией
![]() (рис. 2.1) взаимодействия двух молекул
называется часть энергии системы двух
молекул, зависящая от расстояния
(рис. 2.1) взаимодействия двух молекул
называется часть энергии системы двух
молекул, зависящая от расстояния
![]() между их центрами. Величина
между их центрами. Величина
![]() измеряется той работ
измеряется той работ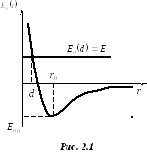 ой,
которая совершается силой
ой,
которая совершается силой
![]() при изменении расстояния между молекулами
от
при изменении расстояния между молекулами
от
![]() до бесконечности, где потенциальная
энергия считается равной нулю
до бесконечности, где потенциальная
энергия считается равной нулю
![]() .
Такой выбор нулевого значения
потенциальной энергии обусловлен тем,
что две молекулы, находящихся на очень
большом расстоянии друг от друга, не
взаимодействуют.
.
Такой выбор нулевого значения
потенциальной энергии обусловлен тем,
что две молекулы, находящихся на очень
большом расстоянии друг от друга, не
взаимодействуют.
Если
две молекулы сближаются на малое
расстояние
![]() под действием сил притяжения
под действием сил притяжения
![]() ,
то система молекул совершает положительную
работу
,
то система молекул совершает положительную
работу
![]() .
Из закона сохранения энергии следует,
что при этом увеличивается
кинетическая энергия молекул, а их
потенциальная энергия уменьшается.
Но при бесконечном удалении молекул
.
Из закона сохранения энергии следует,
что при этом увеличивается
кинетическая энергия молекул, а их
потенциальная энергия уменьшается.
Но при бесконечном удалении молекул
![]() они не взаимодействуют
они не взаимодействуют
![]() .
Поэтому при сближении двух молекул в
области действия сил притяжения
потенциальная энергия их взаимодействия
является величиной отрицательной.
.
Поэтому при сближении двух молекул в
области действия сил притяжения
потенциальная энергия их взаимодействия
является величиной отрицательной.
-
К
 акой
физический смысл «отрицательности»
потенциальной энергии взаимодействия
молекул?
акой
физический смысл «отрицательности»
потенциальной энергии взаимодействия
молекул?
Если
две молекулы сближаются под внешним
воздействием на расстояние
![]() в области, где действуют силы отталкивания
в области, где действуют силы отталкивания
![]() ,
то система совершает отрицательную
работу по преодолению сил отталкивания.
Этот процесс связан с уменьшением
кинетической энергии молекул и
увеличением потенциальной энергии их
взаимодействия. Из выбора начала отсчета
потенциальной энергии следует, что в
области, где действуют силы отталкивания,
,
то система совершает отрицательную
работу по преодолению сил отталкивания.
Этот процесс связан с уменьшением
кинетической энергии молекул и
увеличением потенциальной энергии их
взаимодействия. Из выбора начала отсчета
потенциальной энергии следует, что в
области, где действуют силы отталкивания,
![]() должна быть величиной положительной.
Наибольшее сближение молекул достигается
при расстоянии
должна быть величиной положительной.
Наибольшее сближение молекул достигается
при расстоянии
![]() ,
при котором вся кинетическая энергия
молекул полностью израсходована на
совершение работы против сил отталкивания.
При этом потенциальная энергия
,
при котором вся кинетическая энергия
молекул полностью израсходована на
совершение работы против сил отталкивания.
При этом потенциальная энергия
![]() равна полной энергии Е
системы двух молекул и имеет наибольшее
значение
равна полной энергии Е
системы двух молекул и имеет наибольшее
значение
![]() (рис. 2.1). Величина Е
определяет расстояние
(рис. 2.1). Величина Е
определяет расстояние
![]() ,
которое представляет собой диаметр
(эффективный
диаметр)
молекулы, определяющий линейные размеры
той области, в которую другая молекула
проникнуть не может. Таким образом,
силы отталкивания между молекулами
определяют размеры молекулы.
,
которое представляет собой диаметр
(эффективный
диаметр)
молекулы, определяющий линейные размеры
той области, в которую другая молекула
проникнуть не может. Таким образом,
силы отталкивания между молекулами
определяют размеры молекулы.
При
![]() система двух молекул находится в
состоянии устойчивого равновесия.
Этому соответствует наименьшее значение
потенциальной энергии – в этой точке
кривая
система двух молекул находится в
состоянии устойчивого равновесия.
Этому соответствует наименьшее значение
потенциальной энергии – в этой точке
кривая
![]() имеет минимум
имеет минимум
![]() (рис. 2.1).
(рис. 2.1).
