
- •Санкт-петербургский государственный технологический институт
- •2 Схема лабораторной установки.
- •Содержание
- •1 Аналитический обзор
- •1.1 Водородная энергетика
- •1.2 Микроканальные каталитические реакторы в процессах водородной энергетики
- •1.3 Способы формирования тонкослойных оксидных покрытий
- •1.4 Композиты на основе ZrO2-Al2o3 и перспективы их использования в качестве катализатора
- •1.4.1 Свойства активного оксида алюминия – носителя катализаторов
- •1.4.2 Строение и свойства диоксида циркония
- •1.4.3 Влияние нанокристалловZrO2 на стабилизацию аморфного состояния оксида алюминия в системе ZrO2-Al2o3
- •1.5 Катализаторы на основе закиси никеля и металлического
- •1.6 Патентный поиск
- •2 Цели и задачи работы
- •3 Экспериментальная часть
- •3.1 Исходные материалы, реактивы, приборы и оборудование
- •3.2 Методики получения и исследования свойств образцов суспензий, носителей и катализаторов
- •3.2.1 Методика приготовления суспензии Al2o3-ZrO2
- •3.2.2 Методика формирования тонкослойного оксидного покрытия на пластинчатых носителях
- •3.2.3 Методики исследования свойств синтезированных образцов
- •3.2.3.1Свойства покрывных суспензий
- •3.2.3.2 Определение дисперсности порошка
- •3.2.3.3 Структурно-прочностные характеристики оксидных композитов
- •3.2.4 Рентгенофазовый анализ синтезированных образцов
- •3.2.6 Методики исследования каталитических свойств образцов
- •3.2.6.1 Исследования образцов катализаторов в реакции окисления со
- •3.2.6.2 Исследование образцов катализаторов в реакции окисления водорода
- •3.3 Исследование влияния условий механохимического синтеза на свойства покрывных суспензий
- •3.4 Выбор условий получения базовых покрывных суспензий
- •3.5 Влияние продолжительности измельчения на свойства покрывных суспензий
- •3.6 Приготовление и исследование образцов катализаторов
- •3.7 Испытание образцов катализаторов в реакции окисления со и н2
- •3.8 Результаты ик и рфа
- •4 Стандартизация
- •5 Охрана труда и окружающей среды
- •5.1 Опасные и вредные производственные факторы
- •5.2 Категория помещения по взрывопожароопасности
- •5.2.2 Класс взрывоопасной и пожароопасной зоны
- •5.2.3 Средства тушения пожара
- •5.3 Вентиляционная установка
- •5.4 Освещение помещения, воздух и шум
- •5.5 Аптечка и её содержание
- •5.6 Безопасность выполнения работы
- •5.7 Обеспечение электробезопасности
- •5.8 Анализ технологических операций с точки зрения опасности и вредности их проведения
- •5.9 Меры первой медицинской помощи при случаях травматизма
- •5.10 Охрана окружающей среды
- •6 Выводы по работе
3.2.6.2 Исследование образцов катализаторов в реакции окисления водорода
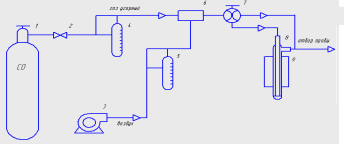
Активность синтезированных образцов катализатора определялась на проточной установке, схема которой приведена на рисунке 6 [27].
Из баллона 1 окись углерода, расход которой регулируется запорным краном 2 и измеряется реометром 4 в соответствии с калибровкой капилляра, поступает в смеситель 6, куда одновременно подается воздух из воздуходувки 3. Расход воздуха регулируется и измеряется реометром 5 в соответствии с калибровкой капилляра. Смесь газов после смесителя проходит через четырехходовой кран и поступает в реактор 8, помещенный в печь 9. При положении четырехходового крана в обход реактора отбирается проба газовой смеси на хроматографический анализ исходной концентрации окиси водорода. При положении четырехходового крана через реактор отбирается проба газовой смеси на хроматографический анализ проскоковой концентрации Н2.
водород
Н2
Рисунок 6 - Схема установки для определения активности катализаторов окисления водорода
1 - баллон с водородом; 2 – кран запорный; 3 - воздуходувка, 4 , 5 – реометры для водорода и воздуха, соответственно; 6 - смеситель водорода и воздуха; 7 – кран четырехходовой ; 8 – реактор, 9 - печь реактора
Условия проведения испытаний:
а) объемная скорость - 0,2 л/мин;
б) концентрация водорода - 2,5-3% об.;
в) температура - 20-4000С;
г) влажность ГВП исходная: 30-40% отн. (прив. к 200С ).
Определение концентрации Н2 в воздухе методом реакционной газовой хроматографии
Определение концентрации водорода в газовоздушной смеси проводили с использованием газохроматографического метода анализа по методике АЮВ.2.840.033 МВИ с диапазоном измеряемых концентраций0,01 - 10% об.
Хроматографический метод анализа [28] основан на различном времени удержания насадкой (сорбентом) хроматографических колонок различных газов (и паров). В связи с этим скорость продвижения газов по делительной колонкеи их поступление в детектор по теплопроводности (ДТП) различны [19]. Электрический сигнал с ДТП хроматографа является результатом разбаланса его мостовой схемы в момент прохождения через ДТП анализируемого газа в смеси с газом-носителем (аргоном). При анализе газовоздушной смеси «водород + воздух» в качестве газа- носителяиспользуется аргон.
Электрический сигнал с ДТП хроматографапоступает на регистрирующий прибор - КСП-4, на диаграммнойленте которого вычерчивается кривая, площадьпод которой (Sпик, мм2) пропорциональна количеству газа, прошедшего через ДТП.
Зависимость площади под кривой на диаграммной ленте от содержания в смеси водорода определяют градуировкой хроматографа по газовой смеси: аргон – водород на основании результатов градуировки.
На полученных хроматограммах измеряют значения Sпик i. Концентрацию веществ в воздухе (С, % об.) определяют по градуировочному графику или вычисляют по формуле;
С = К•Sпик i , (16)
где: К - градуировочный коэффициент,
Sпик i., - приведенное значение площади пика.
Расчет степени окисления водорода XH2 образцами катализатора проводился по формуле:
ХН2=100 (Сисх-Ск)/Сисх (17)
где: ХН2 - степень окисления Н2, %;
Сисх - концентрация Н2 в ГВП исходная, % об.;
Ск - концентрация СО в ГВП на выходе из реактора, % об.;
