
- •Н.В. Лисицын
- •Содержание
- •1 Ресурсы и ресурсосберегающие технологии
- •1.1 Устойчивое развитие, жизненный цикл
- •1.2 Критерии оценки больших систем
- •1.3 Ресурсосбережение
- •2 Основные термодинамические приложения для анализа химико-технологических систем
- •2.1 Энтропия и ее производство
- •2.2 Первый и второй законы термодинамики. Производство энтропии.
- •2.3 Изменение состава систем. Энтропия процессов смешения и химического превращения
- •2.4 Коэффициент полезного действия систем
- •3 Эффективность карно и потери полезной работы систем
- •3.1 Потребление полезной работы
- •3.2 Уравнение Гюи – Стодолы
- •3.3 Задача производства энтропии в общем виде
- •4. Причины и следствия увеличения энтропии систем
- •4.1 Движущие силы и потоки
- •4.2 Феноменологические законы
- •4.3 Принцип симметрии кинетических коэффициентов
- •4.4 Ограниченность применения линейных законов тепло – и массопереноса
- •5. Энергетические потери и неравновесность
- •5.1 Внутренне обратимый двигатель Карно
- •5.2 Принцип равномерного распределения энергии
- •5.3 Прямоточный и противоточный процессы теплообмена
- •6 Эксергия и эксергетический баланс процесса
- •6.1 Эксергия, энергия Гиббса и полезность
- •6.2 Эксергетический баланс
- •6.3 Физическая эксергия. Эксергия смешения
- •6.4 Качество источников энергии
- •7. Физическая и химическая эксергия
- •7.1 Эксергия компонентов воздуха
- •7.2 Химическая эксергия соединений
- •7.3 Энергия Гиббса образования и химическая эксергия
- •8 Эксергетический и энергетический анализ и балансы
- •8.1 Основные недостатки энергетического анализа систем
- •8.2 Уравнения баланса массы, энергии, эксергии и энтропии
- •9 Анализ процессов производства электроэнергии
- •9.1 Основные процессы производства энергии
- •9.2 Сжигание угля и газа
- •9.3 Термодинамическая эффективность газового цикла
- •9.4 Эффективности парового цикла
- •9.5 Эффективность объединенного цикла
- •10 Анализ процессов разделения
- •10.1 Однократная равновесная перегонка бинарной смеси
- •10.2 Термодинамический анализ идеальной дистилляционной колонны
- •10.3 Анализ реальной колонны
- •11 Анализ химико-технологических систем. Основные правила ресурсосбережения
- •11.1 Процедура анализа систем
- •11.2 Эвристические правила экономии материальных и энергетических ресурсов
- •4. Если химическая реакция протекает с выделением тепла, необходимо ее начинать при повышенной (не при пониженной) температуре (рис.49).
- •12 Методические рекомендации по выполнению контрольных работ
- •13 Контрольные работы
- •13.1 Контрольная работа №1
- •13.2 Контрольная работа №2
- •13.3 Контрольная работа №3
- •Кафедра ресурсосберегающих технологий
- •Теоретические основы энерго- и ресурсосбережения
- •190013, Санкт-Петербург, Московский пр., 26
13.2 Контрольная работа №2
Производитель хочет оценить эффективность компрессора. В процессе эксперимента при подъеме давления водорода от Р1 = 500 кПа до Р2 температура газа повышается от t1 = 200С до t2. Считается, что компрессор работает без тепловых потерь в окружающую среду, водород ведет себя как идеальный газ, а его изобарная теплоемкость равна
28.62 кДж/(кмоль·К).
Какова
эффективность компрессора, если она
рассчитывается в соответствии с
выражением:
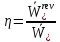
Решение
В любом процессе изменение энтропии 1 моля идеального газа будет равно
s2 -s1=Ср·ln(T2/T1)-R·ln(Р2/Р1).
В обратимом адиабатическом процессе, кроме того, должно выполняться условие s2=s1,
откуда можно определить минимально возможную конечную температуру Т2обр.
Подведенная в эксперименте мощность (на 1 моль) вычисляется по формуле
win=Ср·(Т2-Т1).
Минимальная мощность, необходимая для сжатия газа до давления Р2 в обратимом процессе, равна winобр=Ср·(Т2обр-Т1).
Варианты задания
|
№ варианта |
Буква |
Р2, кПа |
t2, 0С |
№ варианта |
Буква |
Р2, кПа |
t2, 0С |
|
1 |
А, П |
1000 |
107,6 |
8 |
З, Ц |
1350 |
151,1 |
|
2 |
Б, Р |
1050 |
114,4 |
9 |
И, Ч |
1400 |
156,6 |
|
3 |
В, С |
1100 |
121,0 |
10 |
К, Ш |
1450 |
162,0 |
|
4 |
Г, Т |
1150 |
127,4 |
11 |
Л, Щ |
1500 |
167,3 |
|
5 |
Д, У |
1200 |
133,6 |
12 |
М, Э |
1550 |
172,4 |
|
6 |
Е, Ф |
1250 |
139,6 |
13 |
Н, Ю |
1600 |
177,4 |
|
7 |
Ж, Х |
1300 |
145,4 |
14 |
О, Я |
1650 |
182,3 |
13.3 Контрольная работа №3
Поток
водорода с давлением Р3
> 100кПа и температурой t3=200C
разделяется на два равных потока с
давлениями Р1=Р2=100кПа,
заданной температурой t1>t3
и неизвестной t2<t3.
Процесс адиабатический. Газ считать
идеальным, теплоемкость Ср
равна
28.6 кДж/(кмоль·К).

а) Показать, что процесс возможен
б) Оценить эксергетическую
эффективность процесса
Решение
Для 1 моля идеального газа h-h0=Ср·(Т-Т0), s-s0=Ср·ln(T/T0)-R·ln(Р/Р0).
Параметры окружающей среды принимаем равными Р0=100 кПа, Т0=293К (200С).
По условиям задачи процесс адиабатический, поэтому h1+h2=2h3 , откуда находим
T2=2Т3 -Т1.
Вычисляем изменение энтропии s1+s2-2s3 ; если оно положительно, процесс возможен.
Вычисляем эксергии потоков (для 1 моля газа) по формуле ex=h-h0-T0·(s-s0).
Эксергетическую эффективность процесса определяем по формуле (eх1+eх2)/(2eх3).
Варианты задания
|
№ варианта |
Буква |
Р3, кПа |
t1, 0С |
№ варианта |
Буква |
Р3, кПа |
t1, 0С |
|
1 |
А, П |
300 |
50 |
8 |
З, Ц |
400 |
60 |
|
2 |
Б, Р |
400 |
55 |
9 |
И, Ч |
500 |
65 |
|
3 |
В, С |
500 |
60 |
10 |
К, Ш |
600 |
70 |
|
4 |
Г, Т |
600 |
65 |
11 |
Л, Щ |
700 |
50 |
|
5 |
Д, У |
700 |
70 |
12 |
М, Э |
800 |
55 |
|
6 |
Е, Ф |
800 |
50 |
13 |
Н, Ю |
300 |
60 |
|
7 |
Ж, Х |
300 |
55 |
14 |
О, Я |
400 |
65 |
Литература
Лисицын Н.В., Викторов В.К., Кузичкин Н.В. Химико-технологические системы: Оптимизация и ресурсосбережение. – СПб.: Менделеев, 2007. – 312 с.
Лейтес И.Л. Второй Закон и его 12 заповедей. Популярная термодинамика и химическая энерготехнология. – М.: Изд-во МГУ, 2002. – 176 с.
Кудинов В.А. Техническая термодинамика: Учеб. пособие для вузов/В.А.Кудинов, Э.М.Карташов – М.: Высш. шк., 2003. – 261 с.
Пригожин И., Кондепуди Д. Современная термодинамика. От тепловых двигателей до диссипативных структур. – М.: Мир, 2002. – 461с.
Тимофеев В.С. Принципы технологии основного органического и нефтехимического синтеза: Учеб. пособие для вузов/В.С. Тимофеев, Л,А, Серафимов, – М.: Высш. шк., 2003. – 536 с.
de Swaan Arons, J.; van der Kooi; Sankaranarayanan K. Efficiency and Sustainability in the Energy and Chemical Industries; Marcel Dekker, Inc.: New York – Basel, 2004. – 299p.
Szargut J., Morris D. R., Steward F. R. Energy analysis of thermal, chemical, and metallurgical processes: Hemisphere publishing corporation:1988. – 330 p.
Szargut J. Energy Method Technical and Ecological Applications: WIT Press: 2005. – 165 p.
Dincer I.; Rosen M. Exergy: Energy, Enviroment and Sustainable Development; Elsevier: 2004. – 454 p.
HYSYS. Process, version 3.2, documentation: Customization Guide. Cambridge (USA): Aspentech, 2003. – 332 p.
