- •Н.В. Лисицын
- •Содержание
- •1 Ресурсы и ресурсосберегающие технологии
- •1.1 Устойчивое развитие, жизненный цикл
- •1.2 Критерии оценки больших систем
- •1.3 Ресурсосбережение
- •2 Основные термодинамические приложения для анализа химико-технологических систем
- •2.1 Энтропия и ее производство
- •2.2 Первый и второй законы термодинамики. Производство энтропии.
- •2.3 Изменение состава систем. Энтропия процессов смешения и химического превращения
- •2.4 Коэффициент полезного действия систем
- •3 Эффективность карно и потери полезной работы систем
- •3.1 Потребление полезной работы
- •3.2 Уравнение Гюи – Стодолы
- •3.3 Задача производства энтропии в общем виде
- •4. Причины и следствия увеличения энтропии систем
- •4.1 Движущие силы и потоки
- •4.2 Феноменологические законы
- •4.3 Принцип симметрии кинетических коэффициентов
- •4.4 Ограниченность применения линейных законов тепло – и массопереноса
- •5. Энергетические потери и неравновесность
- •5.1 Внутренне обратимый двигатель Карно
- •5.2 Принцип равномерного распределения энергии
- •5.3 Прямоточный и противоточный процессы теплообмена
- •6 Эксергия и эксергетический баланс процесса
- •6.1 Эксергия, энергия Гиббса и полезность
- •6.2 Эксергетический баланс
- •6.3 Физическая эксергия. Эксергия смешения
- •6.4 Качество источников энергии
- •7. Физическая и химическая эксергия
- •7.1 Эксергия компонентов воздуха
- •7.2 Химическая эксергия соединений
- •7.3 Энергия Гиббса образования и химическая эксергия
- •8 Эксергетический и энергетический анализ и балансы
- •8.1 Основные недостатки энергетического анализа систем
- •8.2 Уравнения баланса массы, энергии, эксергии и энтропии
- •9 Анализ процессов производства электроэнергии
- •9.1 Основные процессы производства энергии
- •9.2 Сжигание угля и газа
- •9.3 Термодинамическая эффективность газового цикла
- •9.4 Эффективности парового цикла
- •9.5 Эффективность объединенного цикла
- •10 Анализ процессов разделения
- •10.1 Однократная равновесная перегонка бинарной смеси
- •10.2 Термодинамический анализ идеальной дистилляционной колонны
- •10.3 Анализ реальной колонны
- •11 Анализ химико-технологических систем. Основные правила ресурсосбережения
- •11.1 Процедура анализа систем
- •11.2 Эвристические правила экономии материальных и энергетических ресурсов
- •4. Если химическая реакция протекает с выделением тепла, необходимо ее начинать при повышенной (не при пониженной) температуре (рис.49).
- •12 Методические рекомендации по выполнению контрольных работ
- •13 Контрольные работы
- •13.1 Контрольная работа №1
- •13.2 Контрольная работа №2
- •13.3 Контрольная работа №3
- •Кафедра ресурсосберегающих технологий
- •Теоретические основы энерго- и ресурсосбережения
- •190013, Санкт-Петербург, Московский пр., 26
5.2 Принцип равномерного распределения энергии
В 1987 Тондер и Кваален (Tondeur, Kvaalen), обсуждая перенос теплоты, импульса и вещества, обратили внимание на закономерность, согласно которой при заданной скорости переноса и ее площади общая скорость производства энтропии минимальна, если частные скорости производства энтропии равномерно распределены по всем пространственным и временным переменным процесса. В 1998, Беджан и Тондер (Bejan, Tondeur) придали этому утверждению статус универсального, с помощью которого определяется макроскопическая организация природы, как в неживых, так и в живых системах. Они показали, что оптимальная эффективность системы конечных размеров, обладающей целью, всегда характеризуется равномерным распределением движущих сил или даже вещества, необходимого для организации процесса, например, теплообмена по всему процессу. Эта закономерность получила название принципа равномерного распределения энергии, принципа, во многом свойственному устойчивому состоянию систем,
Для его иллюстрации предположим, что цель некоторого процесса состоит в нагревании потока вещества за конечное время так, чтобы его температура повышалась с увеличением ΔТ. Это требует наличия нагревающего потока, равного
|
|
(17) |
где
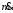 – скорость потока вещества,
– скорость потока вещества, – теплоемкость при постоянном давлении.
Предположим, что процесс проводится в
теплообменнике. Определим между
нагреваемым и нагревающим потоками
локальный тепловой потокj
и соответствующую ему движущую силу
– теплоемкость при постоянном давлении.
Предположим, что процесс проводится в
теплообменнике. Определим между
нагреваемым и нагревающим потоками
локальный тепловой потокj
и соответствующую ему движущую силу
 (рис.22).
(рис.22).
Для простоты предположим также, что между потоком и движущей силой существует линейная связь: j = kx.

Рисунок 22 - Изменение температуры в теплообменнике.
∆Т – увеличение температуры холодного потока.
Локальная
скорость производства энтропии, будет
равна
 .
Теперь вычисляем суммарные величины
потока и энтропии:
.
Теперь вычисляем суммарные величины
потока и энтропии:
|
|
(18) |
и
|
|
(19) |
где величина А соответствует площади теплопереноса и является постоянной (тем самым устанавливается ограничение конечного размера). Для определения оптимального распределения силы х в теплообменнике с помощью вариационного исчисления находим, что x должна быть величиной постоянной:
|
|
(20) |
В
результате j
и
 также остаются постоянными. Это примертермодинамической
оптимизации,
обеспечивающей равномерное распределение
движущей силы процесса с целью наиболее
эффективного действия при заданных
ограничениях.
также остаются постоянными. Это примертермодинамической
оптимизации,
обеспечивающей равномерное распределение
движущей силы процесса с целью наиболее
эффективного действия при заданных
ограничениях.
5.3 Прямоточный и противоточный процессы теплообмена
В качестве подтверждения объективности приведенных результатов сравним скорости энергетических потерь противоточного и прямоточного теплообменников, работающих при одинаковых начальных условиях – с заданными скоростями потоков вещества, теплоты и начальными температурами (рис.23).
 Рисунок
23 - Изменение
температур в прямоточном (а) и противоточном
(b) теплообменниках при одинаковых
начальных температурах
Рисунок
23 - Изменение
температур в прямоточном (а) и противоточном
(b) теплообменниках при одинаковых
начальных температурах
Из рис.23 видно, что прямоточная конфигурация теплообменника производит больше энтропии, что противоточная (величинам энергетических потерь соответствуют заштрихованные области), поскольку для нее (рис.23 а) в отличие от противотока имеется существенный градиент движущей силы по направлению течения рабочей жидкости. Отсюда следует вывод, который имеет существенное значение для инженеров – технологов: противоточный теплообменник намного более эффективен, чем прямоточный.
Одна и та же площадь поверхности теплообмена в противоточном теплообменнике обеспечивает больший рост температуры нагреваемой жидкости, чем в прямоточном теплообменнике. При одном и том же количестве переданной теплоты прямоточный теплообменник требует использования большей площади поверхности теплообмена, чем противоточный. Использование прямоточных процессов допустимо лишь в том случае, если температура стенок теплообменника должна быть снижена или же если необходимо получить быстрое изменение температур потоков.
Выполним конкретные расчеты. Пусть прямоточный и противоточный теплообменники при одинаковых начальных и конечных температурах обменивающихся теплотой жидкостей. Будем считать, что нагревающая жидкость имеет начальную и конечную температуры 500 и 150 0С, а нагреваемая, соответственно, – 80 и 130 0С. Для сравнительной оценки эффективности теплообмена вычислим логарифмическую среднюю разность температур (Δср = (Δ2 – Δ1)/ln(Δ2/Δ1)), которая составляет 180,2 К в случае противоточного и 131,4 К – прямоточного теплообменника. Несложные вычисления позволяют сделать вывод, что прямоточный теплообменник требует использования на 37% большей площади поверхности теплообмена, чем противоточный теплообменник.
Безусловно, в инженерной практике сложно организовать идеально равномерное распределение сил и потоков. Но, тем не менее, принцип равномерного распределения энергии служит критерием верного направления поиска эффективного решения.
В
заключении следует отметить, что
устойчивое состояние систем постоянно
встречается в природе и часто является
предпочтительным состоянием в ходе
промышленных операций. Оно может
рассматриваться как «стабильное
состояние» неравновесной термодинамики,
аналогичное равновесному состоянию
обратимой термодинамики. Конечно,
последнее характеризуется величиной
 ,
в то время как первое – минимальным
значением
,
в то время как первое – минимальным
значением ,
превышающим нулевое значение. Нарушение
этого стабильного и динамичного состояния
вызывает рост скорости производства
энтропии уже только для того, чтобы
вновь вернуться к минимальному значению.
Условие стабильности,
следовательно,
таково:
,
превышающим нулевое значение. Нарушение
этого стабильного и динамичного состояния
вызывает рост скорости производства
энтропии уже только для того, чтобы
вновь вернуться к минимальному значению.
Условие стабильности,
следовательно,
таково:
|
|
(21) |
Таким образом, идеальное, нереалистичное, предельное значение термодинамической эффективности процесса состоит в том, что в обратимом процессе вся полезная работа, участвующая в нем, доступна и после окончания процесса. Энергия передается от одного носителя другому. Движущие силы бесконечно малы и процесс свободен от сил трения: отсутствуют какие бы то ни было препятствия. В результате – отсутствуют как производство энтропии, так и потери полезной работы. Необходимые условия проведения процесса можно вычислить, используя термодинамические функции равновесных состояний, через которые проходит процесс.
Для анализа реального процесса, а не идеализированного его представления, необходимо учитывать скорости передачи вещества, теплоты, импульса и химической энергии. В этом случае при ограничениях во времени и пространстве можно определить оптимальные условия проведения процесса, а именно – с наименьшими (но ненулевыми!), производством энтропии и «потерями» энергии. Оптимальные условия характеризуется универсальным принципом: равномерным распределением движущих сил во времени и пространстве.