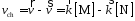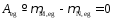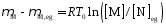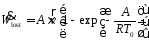- •Н.В. Лисицын
- •Содержание
- •1 Ресурсы и ресурсосберегающие технологии
- •1.1 Устойчивое развитие, жизненный цикл
- •1.2 Критерии оценки больших систем
- •1.3 Ресурсосбережение
- •2 Основные термодинамические приложения для анализа химико-технологических систем
- •2.1 Энтропия и ее производство
- •2.2 Первый и второй законы термодинамики. Производство энтропии.
- •2.3 Изменение состава систем. Энтропия процессов смешения и химического превращения
- •2.4 Коэффициент полезного действия систем
- •3 Эффективность карно и потери полезной работы систем
- •3.1 Потребление полезной работы
- •3.2 Уравнение Гюи – Стодолы
- •3.3 Задача производства энтропии в общем виде
- •4. Причины и следствия увеличения энтропии систем
- •4.1 Движущие силы и потоки
- •4.2 Феноменологические законы
- •4.3 Принцип симметрии кинетических коэффициентов
- •4.4 Ограниченность применения линейных законов тепло – и массопереноса
- •5. Энергетические потери и неравновесность
- •5.1 Внутренне обратимый двигатель Карно
- •5.2 Принцип равномерного распределения энергии
- •5.3 Прямоточный и противоточный процессы теплообмена
- •6 Эксергия и эксергетический баланс процесса
- •6.1 Эксергия, энергия Гиббса и полезность
- •6.2 Эксергетический баланс
- •6.3 Физическая эксергия. Эксергия смешения
- •6.4 Качество источников энергии
- •7. Физическая и химическая эксергия
- •7.1 Эксергия компонентов воздуха
- •7.2 Химическая эксергия соединений
- •7.3 Энергия Гиббса образования и химическая эксергия
- •8 Эксергетический и энергетический анализ и балансы
- •8.1 Основные недостатки энергетического анализа систем
- •8.2 Уравнения баланса массы, энергии, эксергии и энтропии
- •9 Анализ процессов производства электроэнергии
- •9.1 Основные процессы производства энергии
- •9.2 Сжигание угля и газа
- •9.3 Термодинамическая эффективность газового цикла
- •9.4 Эффективности парового цикла
- •9.5 Эффективность объединенного цикла
- •10 Анализ процессов разделения
- •10.1 Однократная равновесная перегонка бинарной смеси
- •10.2 Термодинамический анализ идеальной дистилляционной колонны
- •10.3 Анализ реальной колонны
- •11 Анализ химико-технологических систем. Основные правила ресурсосбережения
- •11.1 Процедура анализа систем
- •11.2 Эвристические правила экономии материальных и энергетических ресурсов
- •4. Если химическая реакция протекает с выделением тепла, необходимо ее начинать при повышенной (не при пониженной) температуре (рис.49).
- •12 Методические рекомендации по выполнению контрольных работ
- •13 Контрольные работы
- •13.1 Контрольная работа №1
- •13.2 Контрольная работа №2
- •13.3 Контрольная работа №3
- •Кафедра ресурсосберегающих технологий
- •Теоретические основы энерго- и ресурсосбережения
- •190013, Санкт-Петербург, Московский пр., 26
4.4 Ограниченность применения линейных законов тепло – и массопереноса
Как было отмечено ранее, феноменологические законы представляют собой линейные зависимости. Условие линейности, как хорошо известно, справедливо для определенной области. Область применения линейных зависимостей тепло – и массопереноса ограничивается условиями законов Фурье и Фика.
Рассмотрим особенности применения линейных зависимостей при проведении химических реакций. Для простоты будем считать, что имеется идеальный раствор, в котором молекулы М и N участвуют в реакции:
|
|
(24) |
а
концентрации веществ таковы, что
химическое сродство, определяемое
уравнением (4)
 ,
положительно. Скорость реакции
,
положительно. Скорость реакции будет
также положительна и задается уравнением:
будет
также положительна и задается уравнением:
|
|
(25) |
 ,
,
 –
мольные скорости превращения вещества
М в N и, соответственно, N в М.
–
мольные скорости превращения вещества
М в N и, соответственно, N в М.
Скорость изменения потерь, связанных с необратимыми процессами (уравнения (6) и (11)) равна:
|
|
(26) |
Будем
считать для простоты, что
 и, следовательно:
и, следовательно:
|
|
(27) |
Определим
соотношение между скоростью химической
реакции
 и ее движущей силой А. Поскольку:
и ее движущей силой А. Поскольку:
|
|
(28) |
Для состояния равновесия:
|
|
(29) |
Принимая, что М и N существуют в идеальном растворе, воспользуемся известной зависимостью для определения химического потенциала:
|
|
(30) |
Аналогичное выражение можно записать и для N. В результате несложных преобразований в итоге получим:
|
|
(31) |
В
состоянии равновесия скорость химической
реакции
 равна нулю и
равна нулю и .
.
Это позволяет записать:
|
|
(32) |
Подставляя последнее выражение в уравнение (31), получим:
|
|
(33) |
Из уравнения (33) следует:
|
|
(34) |
Помня, что
|
|
(35) |
и
подставляя уравнение (34) в (35), получим
зависимость между
 и А:
и А:
|
|
(36) |
Из
уравнения (36) следует, что, если
 ,
то величина
,
то величина линейна по отношению кА:
линейна по отношению кА:
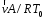 .
При увеличении
.
При увеличении скорость химической реакции быстро
приближается к предельному значению
скорость химической реакции быстро
приближается к предельному значению ,
, ,
как можно видеть из рисунка 15.
,
как можно видеть из рисунка 15.
 Рисунок
15 - Скорость
химической реакции как функция химического
сродства
Рисунок
15 - Скорость
химической реакции как функция химического
сродства
Скорость изменения потерь, связанных с необратимостью процесса, исходя из уравнений (27) и (36), будет равна:
|
|
(37) |
Для ее изучения введем безразмерные величины:
|
|
(38) |
|
|
(39) |
и преобразуем уравнение (37) к виду:
|
|
(40) |
Эта хорошо знакомая из курса математики экспоненциальная зависимость имеет два предела (рис.16).

Рисунок 16 - Изменение скорости энергетических потерь в зависимости от химического сродства.
Анализ
функции показывает, что в окрестности
химического равновесия, при х→0,
скорость реакции зависит от сродства
линейно, а потери, связанные с необратимостью
процесса, –
от его квадрата .
При
.
При , т.е. для чрезвычайно самопроизвольной
и необратимой реакции,
, т.е. для чрезвычайно самопроизвольной
и необратимой реакции,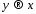 ,
имеет место линейная зависимость
энергетических потерь от сродства.
,
имеет место линейная зависимость
энергетических потерь от сродства.
Рассмотрим более общий случай. Допустим, что существует возможность превратить М в N путем некоторого количества n последовательных сопряженных реакций, для которых принимаем равные значения констант скоростей:
|
|
(41) |
Общее сродство А остается неизменным, но каждый i-ый шаг теперь имеет сродство, равное в среднем Ai=A/n для каждого i. В стабильном состоянии скорость химической реакции будет определяться выражением:
|
|
(42) |
где
|
|
(43) |
В свою очередь, выражение для скорости энергетических потерь, связанных с неравновесностью, в понятиях суммарного сродства в безразмерных величинах будет иметь вид:
|
|
(44) |
Графики зависимостей (44) для различных величин n представлены на рисунке 17.
Если принять. х=4, то скорость потерь y для самопроизвольной одностадийной реакции превращения М в N также примерно равен 4 (при n=1). Однако, при n=4, т.е. при наличии трех промежуточных состояний (существования между М и N трех промежуточных молекул), величина y падает до значения 2,5 или примерно на 40%.
На основании приведенных рассуждений можно сделать следующий вывод: самопроизвольные реакции дорогостоящи и энергетически неэффективны.

Рисунок 17 - Скорость энергетических потерь, как функция химического сродства и числа последовательных сопряженных реакций