
- •Н.В. Лисицын
- •Содержание
- •1 Ресурсы и ресурсосберегающие технологии
- •1.1 Устойчивое развитие, жизненный цикл
- •1.2 Критерии оценки больших систем
- •1.3 Ресурсосбережение
- •2 Основные термодинамические приложения для анализа химико-технологических систем
- •2.1 Энтропия и ее производство
- •2.2 Первый и второй законы термодинамики. Производство энтропии.
- •2.3 Изменение состава систем. Энтропия процессов смешения и химического превращения
- •2.4 Коэффициент полезного действия систем
- •3 Эффективность карно и потери полезной работы систем
- •3.1 Потребление полезной работы
- •3.2 Уравнение Гюи – Стодолы
- •3.3 Задача производства энтропии в общем виде
- •4. Причины и следствия увеличения энтропии систем
- •4.1 Движущие силы и потоки
- •4.2 Феноменологические законы
- •4.3 Принцип симметрии кинетических коэффициентов
- •4.4 Ограниченность применения линейных законов тепло – и массопереноса
- •5. Энергетические потери и неравновесность
- •5.1 Внутренне обратимый двигатель Карно
- •5.2 Принцип равномерного распределения энергии
- •5.3 Прямоточный и противоточный процессы теплообмена
- •6 Эксергия и эксергетический баланс процесса
- •6.1 Эксергия, энергия Гиббса и полезность
- •6.2 Эксергетический баланс
- •6.3 Физическая эксергия. Эксергия смешения
- •6.4 Качество источников энергии
- •7. Физическая и химическая эксергия
- •7.1 Эксергия компонентов воздуха
- •7.2 Химическая эксергия соединений
- •7.3 Энергия Гиббса образования и химическая эксергия
- •8 Эксергетический и энергетический анализ и балансы
- •8.1 Основные недостатки энергетического анализа систем
- •8.2 Уравнения баланса массы, энергии, эксергии и энтропии
- •9 Анализ процессов производства электроэнергии
- •9.1 Основные процессы производства энергии
- •9.2 Сжигание угля и газа
- •9.3 Термодинамическая эффективность газового цикла
- •9.4 Эффективности парового цикла
- •9.5 Эффективность объединенного цикла
- •10 Анализ процессов разделения
- •10.1 Однократная равновесная перегонка бинарной смеси
- •10.2 Термодинамический анализ идеальной дистилляционной колонны
- •10.3 Анализ реальной колонны
- •11 Анализ химико-технологических систем. Основные правила ресурсосбережения
- •11.1 Процедура анализа систем
- •11.2 Эвристические правила экономии материальных и энергетических ресурсов
- •4. Если химическая реакция протекает с выделением тепла, необходимо ее начинать при повышенной (не при пониженной) температуре (рис.49).
- •12 Методические рекомендации по выполнению контрольных работ
- •13 Контрольные работы
- •13.1 Контрольная работа №1
- •13.2 Контрольная работа №2
- •13.3 Контрольная работа №3
- •Кафедра ресурсосберегающих технологий
- •Теоретические основы энерго- и ресурсосбережения
- •190013, Санкт-Петербург, Московский пр., 26
10.2 Термодинамический анализ идеальной дистилляционной колонны
Сначала вспомним некоторые положения из анализа Карно.
В
процессе дистилляции энергия потребляется
в виде теплоты. Максимальное количество
работы, которое можно получить от
источника теплоты Q
при
 ,
где
,
где – температура окружающей среды, задается
уравнением:
– температура окружающей среды, задается
уравнением:
|
|
(17) |
Если
источники теплоты имеют разные
температуры:
 и
и ,
причем выполняется неравенство:
,
причем выполняется неравенство: ,
то
наибольшая работа, которая может быть
совершена при первой из них, равна
,
то
наибольшая работа, которая может быть
совершена при первой из них, равна
 ,
в то время как при второй:
,
в то время как при второй: .
Величина потерь энергии, которая могла
бы пойти на совершение полезной работы,
будет равна разности между величинами
этих работ:
.
Величина потерь энергии, которая могла
бы пойти на совершение полезной работы,
будет равна разности между величинами
этих работ:
|
|
(18) |
В
случае, если теплота от источника с
температурой
 должна перейти к потребителю с температурой
должна перейти к потребителю с температурой ,
то минимальная работа, которую для этого
необходимо совершить, будет равна:
,
то минимальная работа, которую для этого
необходимо совершить, будет равна:
|
|
(19) |
Теперь приступим к анализу дистилляционной колонны.
Согласно
уравнения Клапейрона–Клаузиуса для
идеального газа следует, что, если
теплота испарения
 не зависит от температурыТ
(для узкого диапазона температур), наклон
кривой давления насыщенных паров
определяется уравнением:
не зависит от температурыТ
(для узкого диапазона температур), наклон
кривой давления насыщенных паров
определяется уравнением:
|
|
(20) |
где
R
– универсальная газовая постоянная, а
 – давление насыщенных паров. Идеальная
относительная летучесть разделяемых
жидкостей, имеющих близкие точки кипения
(например, пропана и пропилена) определяется
выражением:
– давление насыщенных паров. Идеальная
относительная летучесть разделяемых
жидкостей, имеющих близкие точки кипения
(например, пропана и пропилена) определяется
выражением:
|
|
(21) |
Из уравнений (20) и (21) следует, что для температурного диапазона дистилляции можно записать:
|
|
(22) |
где
 и
и обозначают температуры в основании и
на верху колонны. Еще раз заметим, что
рассматривается идеальная смесь и
энтальпия испарения для обоих веществ
одна и та же. В действительности
относительная летучесть
обозначают температуры в основании и
на верху колонны. Еще раз заметим, что
рассматривается идеальная смесь и
энтальпия испарения для обоих веществ
одна и та же. В действительности
относительная летучесть от идеальной величины будет отличаться.
от идеальной величины будет отличаться.
Упрощенная схема разделения идеальной эквимолярной смеси представлена ниже на рисунке 45.
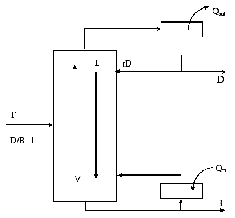
Рисунок 45 - Схема процесса дистилляции
В
систему подается жидкая смесь, вводимая
в точке, где жидкость имеет один и тот
же состав и постоянную температуру.
Исходя из эквимолярности этой смеси,
количество дистиллята D
и кубового продукта (остатка) на моль
питающего потока F,
,
будет равно по одной второй. Если
флегмовое число равно r
= L/D,
то число молей жидкости
L,
поступающей наверх колонны будет равно,
L
= rD
=
 молей
(выше точки ввода питания). Поток пара,
соответственно, будет равен
молей
(выше точки ввода питания). Поток пара,
соответственно, будет равен
 .
Для выработки этого пара к основанию
колонны должно быть передано количество
теплоты:
.
Для выработки этого пара к основанию
колонны должно быть передано количество
теплоты:
|
|
(23) |
Будем считать, что теплота испарения приблизительно равна одной и той же величине для обоих веществ, и что разность температур вдоль колонны пренебрежимо мала. Из этого следует, что
|
|
(24) |
где
 – охлаждающая мощность холодильника.
Общее разделение не требует энергии:
количество Джоулей теплоты, поступающее
в колонну, равно числу Джоулей теплоты,
покидающей колонну, что соответствует
первому закону термодинамики. Однако,
«качество» этих тепловых потоков или,
что одно и то же, наибольшая работа,
которую они могут совершить, не одно и
то же.
– охлаждающая мощность холодильника.
Общее разделение не требует энергии:
количество Джоулей теплоты, поступающее
в колонну, равно числу Джоулей теплоты,
покидающей колонну, что соответствует
первому закону термодинамики. Однако,
«качество» этих тепловых потоков или,
что одно и то же, наибольшая работа,
которую они могут совершить, не одно и
то же.
Наименьшее количество энергии, которое должно поступать в колонну для разделения идеальной смеси на составляющие ее компоненты, задается уравнением (рис.46):
|
|
(25) |
Для эквимолярной смеси будем иметь:
|
|
(26) |

Рисунок 46 - Структура материальных и тепловых потоков процесса дистилляции
С другой стороны в соответствии с уравнением (19) величина наименьшей работы, необходимой для передачи тепла от низа колонны к верху, равна:
|
|
(27) |
Эта работа идет на разделение. Поэтому:
|
|
(28) |
Согласно (23) для совершения минимальной работы требуется подвести минимально необходимое количество тепла:
|
|
(29) |
Уравнения (22), (26), (27) и (29) могут быть объединены, что позволяет получить формулу:
 (30)
(30)
и рассчитать минимальный расход флегмы.
|
|
|













