- •Н.В. Лисицын
- •Содержание
- •1 Ресурсы и ресурсосберегающие технологии
- •1.1 Устойчивое развитие, жизненный цикл
- •1.2 Критерии оценки больших систем
- •1.3 Ресурсосбережение
- •2 Основные термодинамические приложения для анализа химико-технологических систем
- •2.1 Энтропия и ее производство
- •2.2 Первый и второй законы термодинамики. Производство энтропии.
- •2.3 Изменение состава систем. Энтропия процессов смешения и химического превращения
- •2.4 Коэффициент полезного действия систем
- •3 Эффективность карно и потери полезной работы систем
- •3.1 Потребление полезной работы
- •3.2 Уравнение Гюи – Стодолы
- •3.3 Задача производства энтропии в общем виде
- •4. Причины и следствия увеличения энтропии систем
- •4.1 Движущие силы и потоки
- •4.2 Феноменологические законы
- •4.3 Принцип симметрии кинетических коэффициентов
- •4.4 Ограниченность применения линейных законов тепло – и массопереноса
- •5. Энергетические потери и неравновесность
- •5.1 Внутренне обратимый двигатель Карно
- •5.2 Принцип равномерного распределения энергии
- •5.3 Прямоточный и противоточный процессы теплообмена
- •6 Эксергия и эксергетический баланс процесса
- •6.1 Эксергия, энергия Гиббса и полезность
- •6.2 Эксергетический баланс
- •6.3 Физическая эксергия. Эксергия смешения
- •6.4 Качество источников энергии
- •7. Физическая и химическая эксергия
- •7.1 Эксергия компонентов воздуха
- •7.2 Химическая эксергия соединений
- •7.3 Энергия Гиббса образования и химическая эксергия
- •8 Эксергетический и энергетический анализ и балансы
- •8.1 Основные недостатки энергетического анализа систем
- •8.2 Уравнения баланса массы, энергии, эксергии и энтропии
- •9 Анализ процессов производства электроэнергии
- •9.1 Основные процессы производства энергии
- •9.2 Сжигание угля и газа
- •9.3 Термодинамическая эффективность газового цикла
- •9.4 Эффективности парового цикла
- •9.5 Эффективность объединенного цикла
- •10 Анализ процессов разделения
- •10.1 Однократная равновесная перегонка бинарной смеси
- •10.2 Термодинамический анализ идеальной дистилляционной колонны
- •10.3 Анализ реальной колонны
- •11 Анализ химико-технологических систем. Основные правила ресурсосбережения
- •11.1 Процедура анализа систем
- •11.2 Эвристические правила экономии материальных и энергетических ресурсов
- •4. Если химическая реакция протекает с выделением тепла, необходимо ее начинать при повышенной (не при пониженной) температуре (рис.49).
- •12 Методические рекомендации по выполнению контрольных работ
- •13 Контрольные работы
- •13.1 Контрольная работа №1
- •13.2 Контрольная работа №2
- •13.3 Контрольная работа №3
- •Кафедра ресурсосберегающих технологий
- •Теоретические основы энерго- и ресурсосбережения
- •190013, Санкт-Петербург, Московский пр., 26
6.4 Качество источников энергии
Итак, первый закон термодинамики оперирует количественными величинами энергии, в то время, как второй – с ее работоспособностью, а значит с качеством. Изучая одновременно систему и ее окружение, мы видим, что первый закон выражает мысль о том, что для реального процесса общее количество Джоулей энергии, вовлеченной в процесс, остается неизменным. Второй закон свидетельствует о том, что их качество падает. Общее количество эксергии – полезной работы – рассеивается в каждом процессе в связи с элементами необратимости. Очевидно, что каждый вид энергии имеет свое качество. Его следует определить, понимая под качеством энергии ту ее часть (часть Джоулей энергии), которая связана с полезной работой. Это «качество» q имеет размерность Дж/Дж и очевидно принимает значение от нуля до единицы: 0 < q < 1.
Рассмотрим ранее представленный на рисунке 12 процесс и запишем еще раз известные формулы:
|
|
(29) |
или
|
|
(30) |
Последняя зависимость выражает физический смысл того, что общая энергия, переданная системе, вероятно, сохраняется в ней в виде энтальпии. Следовательно, ΔН представляет собой энергию системы, участвующую в ее взаимодействии с окружающей средой.
Уравнение (30) может быть преобразовано, если зависимости, соответствующие первому и второму законам, объединить:
|
|
(31) |
Ранее
на основании этого уравнения определялось
наименьшее количество энергии, необходимое
для перевода системы из состояния 1 в
состояние 2 с
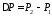 и
и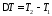 и, следовательно, ее термодинамические
свойства
и, следовательно, ее термодинамические
свойства и
и :
:
|
|
(32) |
Реальное количество энергии превышает это значение на величину:
|
|
(33) |
Уравнение
(32) позволяет определить эксергию, если
в качестве состояния 1 выбирается любое
произвольное состояние, в том числе –
например,
 и
и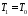 .
.
В
общем случае при изменения состояния
системы от
 ,
, доР,
Т
суммарное поступление энергии равно:
доР,
Т
суммарное поступление энергии равно:
|
|
(34) |
тогда как потенциальное значение доступной энергии будет иным:
|
|
(35) |
Из этого следует, что каждый джоуль энергии системы, имеет качество, определяемое как
|
|
(36) |
В таблице 3 представлены значения качества энергии для различных энергоносителей, от воздуха окружающей среды до энергии продуктов окисления.
Таблица
3 - Качество различных источников энергии,
Дж/Дж,
 =288,15
К
=288,15
К
---------------------------------------------------------------------
Химическая ~1
Газообразные продукты окисления 0,6-0,8
Тепловые отходы 0,2-0,3
Печные газы 0,2
Горячая вода (100ºС) 0,12
Теплая вода (50 ºС) 0,06
---------------------------------------------------------------------
Рассмотрим пример, поясняющий понятие качества. На рисунке 27 изображена схема процесса, в котором электростанция работает на природном газе. Продукты окисления газа используются в работе сложного цикла, состоящего из газовой турбины и паровой энергоустановки. Электростанция одновременно производит электричество и тепло.
Предположим,
что энергия, поступающая в
систему, представлена химической
энергией метана, и пусть изначально
имеется 10 Дж этой энергии, т.е.
 = 10 Дж. Предположим также, что из этих 10
Дж 5 Дж идут на производство электричества,
а 4 Дж – на горячую воду. Один Джоуль
теряется в печной трубе.
= 10 Дж. Предположим также, что из этих 10
Дж 5 Дж идут на производство электричества,
а 4 Дж – на горячую воду. Один Джоуль
теряется в печной трубе.
Допустим, что системе имеется тепловой насос, благодаря которому из 5 Дж, идущих на производство электричества, можно получить 15 Дж горячей воды, направляемой к потребителям.
 Рисунок
27
- Схема энергетической установки для
одновременного производства электричества
и горячей воды
Рисунок
27
- Схема энергетической установки для
одновременного производства электричества
и горячей воды
Для расчета качества энергии вместо уравнения (36) воспользуемся его упрощенным видом:
|
|
(37) |
который
выводится из уравнения (36), если
 считать постоянной.
считать постоянной.
По определению, качество энергии электричества равно единица, так как теоретически все электричество может быть полностью превращено в работу. Качество энергии природного газа также близко к единице; печных газов и горячей воды, соответственно, – 0,2 и 0,12 (они рассчитываются по уравнения (37). Эффективность одновременного производства электричества и тепла равна: (19·0,12)/(10·1)=0,23, где мы пренебрегаем эксергией печных газов, так как они не используются при нагреве воды. Для сравнения эффективность производства горячей воды напрямую при сжигании природного газа (например, в бойлере), равна: (9·0,12)/(10·1)=0,11, поскольку 10 Дж энергии топлива могут быть преобразованы в 9 Дж энергии горячей воды, а 1 Дж энергии уходит в печную трубу (рис.28).

Рисунок 28 - Показатели качества работы энергетической установки
Эффективность стадии сгорания топлива была рассчитана по уравнению (36) и составила 78%. Эксергическая эффективность второй стадии – одновременного производства – равна (5·1+4·0,12)/(10·0,78)=0,70 или 70%. Здесь считается, что содержание эксергии печных газов теряется. Термодинамическая эффективность целого завода по одновременному производству составляет величину 0,78·0,7=0,55 или 55% – результат, достигаемый лишь на наиболее современных энергетических установках. Термодинамическая эффективность теплового насоса равна: (15·0,12)/(5·1)=0,36.
Эксергическая
эффективность процесса одновременного
производства, включая тепловой насос,
 = 0,23, оказывается более, чем вдвое,
превышающей эффективность для процесса
прямого сжигания,
= 0,23, оказывается более, чем вдвое,
превышающей эффективность для процесса
прямого сжигания, = 0,11. Заметим, что эффективность теплового
насоса составляет 0,36.
= 0,11. Заметим, что эффективность теплового
насоса составляет 0,36.
Если качественный аспект энергии не рассматривать, всю энергия считать одинаковой (что соответствует истине в численном, но не в качественном выражении!), эффективность теплового насоса окажется равной 15/5, или 300%, что является грубой ошибкой.
Следовательно, эксергия и качество теплоты являются совокупными инструментами правильного понимания истинных связей между структурными составляющими ХТС, вовлеченными в процесс и взаимодействующими друг с другом.